
覚えておきたいポイント!
麻酔
・TCI(target controlled infusion)機能を用いて投与可能な製剤がある
集中治療
・小児等には禁忌
・プロポフォール注入症候群(propofol infusion syndrome:PRIS)に注意
共通
・導入・覚醒が速やかで調節性がよい
・催眠作用・鎮静作用・抗不安作用があるが、
鎮痛作用や筋弛緩作用はない
・舌根沈下や血圧低下、徐脈などの呼吸循環動態の抑制がある
・プロポフォールを主体とした全静脈麻酔は
吸入麻酔薬使用時よりも術後悪心・嘔吐の発生率が低い
・大豆、卵、ヤシ油やココナッツにアレルギーのある
患者への使用は注意が必要
・脂肪乳剤であり、12時間ごとにラインの交換が必要
・注入時に血管痛を生じることがある


ご使用にあたっては各製品の電子添文をご確認ください。
※イラストはイメージです。
- ■禁忌
-
- ・本剤または本剤の成分に対し過敏症の既往歴のある患者
- ・小児等(集中治療における人工呼吸中の鎮静)
調節性がよい全身麻酔・鎮静用剤
作用機序
作用機序は解明されていませんが、プロポフォールは脳内の5量体(αサブユニット2個、βサブユニット2個、γサブユニット1個)で構成されたGABAA受容体のうち、サブユニットのα1とβ2に結合してイオンチャネルを開口させ、CIイオンが細胞内に流入すると過分極となり、神経細胞の興奮性が低下し、催眠を誘導するという報告2)があります。
効能・効果
・全身麻酔の導入および維持
・集中治療における人工呼吸中の鎮静
使用頻度の高い手術について
- 全身状態が安定しているASA-PS1~2の手術麻酔患者さんの導入時には、2.0〜2.5mg/kgの単回投与を用いることがあります。
- 術後悪心・嘔吐のリスクを有する患者さん(女性、腹腔鏡手術、術後悪心・嘔吐の既往、非喫煙者)では、麻酔導入および維持に用いる全身麻酔薬としてプロポフォールが選択されます3)。
使用方法
投与経路
用法・用量
全身麻酔の導入および維持
■導入
成人
通常、本剤を0.05mL/kg/10秒(プロポフォールとして0.5mg/kg/10秒)の速度で、患者の全身状態を観察しながら、就眠が得られるまで静脈内に投与します。なお、ASA3および4の患者には、より緩徐に投与してください。
通常は、本剤0.20〜0.25mL/kg(プロポフォールとして2.0〜2.5mg/kg)で就眠が得られます。高齢者は、より少量で就眠が得られる場合があります。就眠後は必要に応じて適宜追加投与してください。
目標制御注入法(target controlled infusion:TCI)を用いる場合には、効果部位濃度3.0〜5.0μg/mLを目標とし、投与を開始してください。
※ディプリフューザーTCI機能を用いる投与方法の詳細については、電子添文をご確認ください。
■維持
成人
通常、酸素投与下に、本剤を静脈内に投与します。適切な麻酔深度が得られるように患者の全身状態を観察しながら、投与速度を調節してください。
通常は、本剤0.4〜1.0mL/kg/時(プロポフォールとして4〜10mg/kg/時)の投与速度で適切な麻酔深度が得られます。
また、鎮痛剤(麻薬性鎮痛剤、局所麻酔剤など)を併用してください。なお、局所麻酔剤併用時には通常より低用量で適切な麻酔深度が得られます。
TCIは脳波モニターを参考に目標効果部位濃度になるように調整してください。
| 導入後の時間 | 0〜10分 | 10〜20分 | 20〜30分 | 30分〜 |
|---|---|---|---|---|
| 投与速度 | 1.0mL/kg/時 (プロポフォールとして10mg/kg/時) |
0.8mL/kg/時 (プロポフォールとして8mg/kg/時) |
0.6mL/kg/時 (プロポフォールとして6mg/kg/時) |
全身状態をみながら調節する |
集中治療における人工呼吸中の鎮静
成人(高齢者を含む)
0.03mL/kg/時(プロポフォールとして0.3mg/kg/時)の投与速度で、持続注入にて静脈内に投与を開始し、適切な鎮静深度が得られるように患者の全身状態を観察しながら、投与速度を調節します。
通常は本剤0.03〜0.30mL/kg/時(プロポフォールとして0.3〜3.0mg/kg/時)の投与速度で適切な鎮静深度が得られます。なお、疾患の種類、症状の程度を考慮して、必要とする鎮静深度に応じて投与速度を増減してください。また、必要に応じて鎮痛剤を併用してください。
| 時間 | 0〜5分 | 5分〜 |
|---|---|---|
| 投与速度 | 0.03mL/kg/時 | 0.03〜0.30mL/kg/時 (全身状態を観察しながら適宜増減) |
集中治療における人工呼吸中の鎮静に関する注意
・本剤は、持続注入により投与し、急速投与は行わないでください。
・本剤は、通常、7日を超えて投与しないでください。ただし、鎮静効果が認められ、7日を超えて本剤投与による鎮静が必要な場合には、患者の全身状態を引き続き慎重に観察してください。
肥満患者さんへの投与量はどう計算したらよいですか?
理想体重?それとも実体重?
麻酔導入時に速やかな効果発現を得るため、実体重が用いられることがあります。一方、脂肪組織の血流は限定的であり、分布容積への影響が少ないため、実体重に基づくと過剰投与となる可能性があります。麻酔維持期は、TCIを用いる場合、術中覚醒を避けるためには実体重での投与が望ましいとされています。その理由は、肥満にともなう肝血流量増加によりクリアランスが増加するためです4~6)。
導入および維持期を通じて適切な麻酔深度を得るためには、脳波モニターを指標とした投与が推奨されています。
投与の準備
薬剤調製時の注意
- 使用前にアンプルまたはバイアルを振盪してください。
- エマルジョンに分離を認めた場合には使用しないでください。
- 投与前に本剤を5%ブドウ糖注射液以外の薬剤と混合しないでください。本剤を5%ブドウ糖注射液(ガラス製容器)で希釈する時の希釈率は5倍(プロポフォール濃度2mg/mL以上)を超えないようにしてください。希釈は投与直前に無菌的に行い、6時間以内に使用してください。なお、本剤の希釈液の投与速度の設定には注意してください。
- ポリ塩化ビニル製の輸液セットなどを使用した場合、可塑剤であるDEHP[di-(2-ethylhexyl)phthalate;フタル酸ジ-(2-エチルヘキシル)]が製剤中に溶出することが報告されているので、DEHPを含まない輸液セットなどを使用することが望まれます。
薬剤投与時の注意
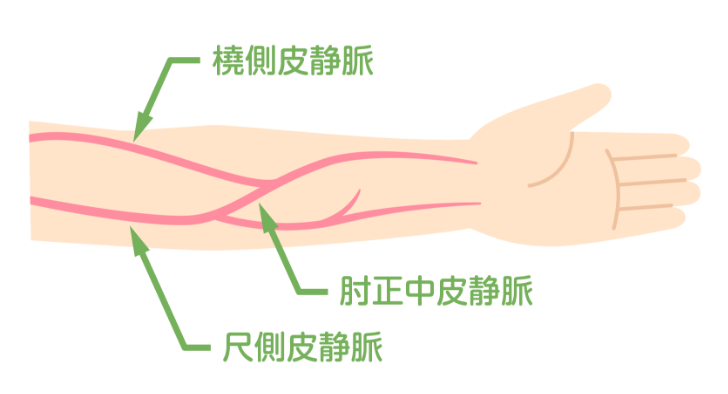
- 本剤は静脈内のみに投与してください。注射時にみられる血管痛は、前腕、前肘窩の比較的太い静脈へ注射することにより、最小限に抑えることができます。
- 注射部位の近位で三方活栓を介して、乳酸リンゲル液、5%ブドウ糖注射液、生理食塩液、ブドウ糖加乳酸リンゲル液とともに本剤を投与することが可能です。
なお、本剤は脂肪乳剤を含有しているため、ポリカーボネート製の三方活栓や延長チューブなどを使用した場合、そのコネクター部分にひび割れが発生し、血液および薬液漏れ、空気混入などの可能性があります。その場合、必要な投与量が確保されず、麻酔覚醒などが生じる可能性があるので注意してください。 - 持続投与する場合は、投与速度を調節するため、シリンジポンプなどを使用してください。
- エマルジョンが破壊されることがあるので、微生物ろ過フィルターを用いて投与しないでください。
- 本剤は防腐剤を使用しておらず、また脂肪乳剤のため汚染されると細菌が増殖し、重篤な感染症が起こるおそれがあるので以下の点に注意してください。
(1) 開封後、無菌的に取り扱い、直ちに使用を開始してください。
(2) 本剤の投与に使用するチューブ類なども無菌的に取り扱ってください。
(3) 1アンプルまたは1バイアルを複数の患者に使用しないこと。1人の患者に対し、1回のみの使用とし、残液は廃棄してください。
(4) 本剤の投与に使用した注射器、チューブ類および本剤の残液は、手術終了時または投与開始12時間後のいずれか早い時点で廃棄してください。また、12時間を超えて投与する場合は、新たな注射器、チューブ類および本剤を使用してください。
5%ブドウ糖注射液で希釈できますが、当院では希釈せずに原液で使用しています。
薬物動態
- 半減期7)
プロポフォールの体内動態は3-コンパートメントモデルに適合し、全血中濃度は3相性に減衰します。
日本人健康成人男子6例に1.0、2.0および2.5mg/kgを単回静脈内ボーラス投与したとき、各相の半減期は2.6分(t1/2α)、51.0分(t1/2β)および365分(t1/2γ)でした。 - 分布8)
患者にプロポフォールを2.5mg/kg用量で単回静脈内ボーラス投与したとき、投与後10分および120分後の蛋白結合率は約97~99%でした(外国人データ)。 - 代謝・排泄9)
主に肝臓で代謝されます。大部分がグルクロン酸抱合や硫酸抱合を受けて、腎から尿中に排泄されます。
プロポフォールの主代謝物には麻酔作用は認められていません。
作用発現時間・作用持続時間
意識消失までの時間:平均46秒(プロポフォール平均就眠量:2.21±0.39mg/kg)10)。
開眼までに要した時間:6.5分(麻酔維持:亜酸化窒素非併用群、投与速度7.0±2.3mg/kg/時)11)。
使用時の流れ:全静脈麻酔の場合
麻酔の導入から維持まで、麻酔の3要素である鎮静・鎮痛・筋弛緩に関係する薬剤を、静脈内投与のみで行う方法を全静脈麻酔といいます。
全身麻酔では導入で静脈麻酔薬、その後の維持では吸入麻酔薬のように組み合わせて使用したり、このTIVAで行ったりするのが一般的ですが、この他にも導入・維持を吸入麻酔薬で行う麻酔法(volatile induction and maintenance of anesthesia:VIMA)も存在します。
小児等や静脈路確保が困難な患者ではVIMAが選択されます。VIMAでは、気道刺激性が低く、導入にも使用できるセボフルランが主に用いられます。
-
モニター類の装着(脳波モニター、筋弛緩モニターなど)
-
前酸素化
-
パルスオキシメータでSpO2、カプノメータでEtO2の適正値までの上昇を確認
-
オピオイド(鎮痛薬)などを適宜投与
-
プロポフォールとして0.5mg/kg/10秒の速度、
またはTCI3.0〜5.0μg/mLで、就眠が得られるまで静脈内に投与
-
プロポフォール投与後、血圧低下に注意が必要です。
-
呼名反応消失、脳波モニターを確認

- 意識消失を確認
- ロクロニウム(筋弛緩薬)などを投与
- 脳波モニター、筋弛緩モニターを確認
-
BIS値40〜60や睡眠紡錘波の出現により入眠を確認、
TOF 0により十分な筋弛緩であることを確認します。 -
気管挿管
- 麻酔の維持へ
脳波モニターを指標にプロポフォール持続投与量の調整を行う -
鎮静薬は麻薬性鎮痛薬と相乗作用があるため麻薬性鎮痛薬を増減した場合は、鎮静深度を適宜確認します。
※手術麻酔については、こちらで全体の流れをご覧いただけます。
使用する上での重要な注意点
効能共通
- 投与にあたっては、原則としてあらかじめ絶食させてください。
- 投与にあたっては、気道確保、酸素吸入、人工呼吸、循環管理を行えるよう準備しておいてください。
- 本剤を使用する場合、一般の全身麻酔剤と同様、麻酔開始より患者が完全に覚醒するまでは、麻酔技術に熟練した医師が専任で患者の全身状態を注意深く監視してください。集中治療の鎮静に利用する場合においても、集中治療に熟練した医師が本剤を取り扱ってください。
- 投与中は気道を確保し、血圧の変動に注意して呼吸・ 循環に対する観察・対応を怠らないでください。
- 投与中は、適切な麻酔または鎮静深度が得られるよう患者の全身状態を観察しながら、投与速度を調節してください。
- 本剤の影響が完全に消失するまでは、自動車の運転など危険をともなう機械の操作に従事しないよう患者にご説明をお願いします。
- 麻酔深度が深すぎると、覚醒遅延を生じる可能性があるため、脳波モニターを用いて最適な麻酔深度となるよう投与量を調整してください。
- 投与中は、鎮静レベルおよび中枢神経系機能の評価を必要に応じて行い、鎮静に必要な投与速度を定めてください。
- 投与中は、気管挿管による気道確保を行ってください。
- 人工呼吸からの離脱の過程では、患者の観察を継続し、必要に応じて人工呼吸を行ってください。
全身麻酔の導入および維持
集中治療における人工呼吸中の鎮静
このような患者さんでは、投与量および投与方法について慎重に検討した上で使用することが重要です。
※ディプリフューザーTCI機能を用いる投与方法の詳細については、電子添文をご確認ください。
副作用
重大な副作用
詳細やその他の副作用については各製品の電子添文をご確認ください。
プロポフォール持続投与中に突然の治療抵抗性徐脈を発現し、心不全に至る致死的合併症です。
- 症状
高脂血症、肝肥大または脂肪肝、顕著な代謝性アシドーシス、高カリウム血症、CK上昇、横紋筋融解症、ミオグロビン尿症などの突然発症が特徴です。 - 発現条件
4mg/kg/時を超える投与速度での48時間を超える持続投与で発症リスクが高まるという報告12)がありますが、4mg/kg/時以下の投与でも発症の報告13)があります。
比較的長期間(>48時間)の高用量投与(5mg/kg/時)時に、とくに注意が必要です14)。
プロポフォールはミトコンドリアのエネルギー代謝に抑制的に作用することで、PRISを生じると考えられています。ミトコンドリア機能障害を合併している患者さんや横紋筋融解症の既往を有する患者さんでは使用を避ける必要があります。
併用薬
併用禁忌
併用注意
- 相互に作用を増強する薬剤
ベンゾジアゼピン系薬物(ジアゼパム、ミダゾラム等)、バルビツール酸系薬物、全身麻酔剤(亜酸化窒素等)、局所麻酔剤、中枢神経系抑制剤(麻薬性鎮痛剤等)、アルコール、降圧剤、抗不整脈剤(β1遮断剤(エスモロール塩酸塩、ランジオロール塩酸塩等))
拮抗薬
取り扱い・管理
習慣性医薬品は、向精神薬と同様に管理(鍵付きの施設内に貯蔵するなど)することが望ましい15)とされています。
1) ロナルド D.ミラー:ミラー麻酔科学,2007:251-8.
2) 小田切 徹太郎:麻酔薬の作用機序.麻酔,2007;56増刊:S1-S5(Ⅲ)
3) Gan TJ,et al.:Anesthesia&Analgesia.2020:131(2):411-48.(PMID:32467512)
4) Ingrande J,Lemmens H J M:Br J Anaesth;2010;105(1):i16-23.(PMID:21148651)
5) Liu N,et al.:Br J Anaesth.2015;114(4):605-14.(PMID:2550068)
6) Eman A,et al.:IJPMR.2016;4(2).
7) 新宮 興 他:麻酔,1990;39:219および685.
8) Kay NH,et al.:Br.J.Anaesth.1986;58:1075-9.
9) 中尾 正和 他:麻酔と蘇生,1993;29(1):77-81.
10) 風間 富栄 他:麻酔と蘇生,1993;29(1):11-21.
11) 盛生 倫夫 他:麻酔と蘇生,1993;29(1):45-56.
12) Bray RJ:Paediatr Anaesth 1998;8(6):491-9.
13) Michel-Macías C,et al.:Oxf Med Case Reports.2018;2018(6):omy023.
14) Vasile B,et al.:Intensive Care Med.2003;29(9):1417-25.
15) 「病院・診療所における向精神薬取り扱いの手引き:平成24年2月」(厚生労働省)
https://www.mhlw.go.jp/bunya/iyakuhin/yakubuturanyou/dl/kouseishinyaku_01.pdfを編集して作成.

