プロスタルモン®・F注射液1000・2000
医療関係者向情報サイト
製品情報
プロスタルモン®・F注射液1000・2000
各種コード
| 容量 | |
|---|---|
| 容量 | 2mLX10A(販売中止) |
| 薬価基準収載医薬品コード | 個別医薬品(YJ)コード | レセプト電算処理コード | |||
|---|---|---|---|---|---|
| 薬価基準収載医薬品コード | 2499401A3065 | 個別医薬品(YJ)コード | 2499401A3065 | レセプト電算処理コード |
銘柄別 640454040 統一名 000000000 |
| HOT番号 | JANコード | 統一商品コード | |||
|---|---|---|---|---|---|
| HOT番号 | 1055412020101 | JANコード | 4987211351212 | 統一商品コード | 211-351212 |
| GS-1コード | ||||||
|---|---|---|---|---|---|---|
| 調剤包装単位コード | 販売包装単位コード | 元梱包装単位コード | ||||
| GS-1コード | 調剤包装単位コード | (01)04987211451219 | 販売包装単位コード | (01)14987211351219 | 元梱包装単位コード | (01)24987211351216 |
お知らせ文書NEWS
- 2024年03月13日
- 経過措置
- 経過措置移行品目のご案内
- 2024年03月13日
- 2023年11月20日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2023年11月20日
- 2023年09月19日
- 販売中止・流通状況
- プロスタルモン®・F注射液2000 販売中止のお知らせ
- 2023年09月19日
- 2022年12月12日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2022年12月12日
- 2022年04月26日
- 販売中止・流通状況
- プロスタルモン・F注射液1000 1mL×50A 販売中止のお知らせ
- 2022年04月26日
- 2022年01月05日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2022年01月05日
- 2020年12月07日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2020年12月07日
- 2020年06月25日
- 使用上の注意
- プロスタルモン®・F注射液1000・2000 使用上の注意改訂のお知らせ
- 2020年06月25日
- 2019年12月02日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2019年12月02日
- 2019年10月25日
- 包装・表示
- プロスタルモン®・F注射液1000(1mL×50A)・2000(2mL×10A) 包装変更のお知らせ
- 2019年10月25日
- 2019年01月23日
- 包装・表示
- 可変表示対応済み個装箱を掲載しました。(Lot;8Z041~)
- 2019年01月23日
- 2019年01月16日
- 包装・表示
- プロスタルモン®・F注射液1000 1mL×10A 包装変更のお知らせ
- 2019年01月16日
- 2018年12月20日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2018年12月20日
- 2018年12月03日
- 新発売
- 製造販売承認の承継に関するご案内 2018年11月
- 2018年12月03日
- 2023年11月20日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2023年11月20日
- 2022年12月12日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2022年12月12日
- 2022年01月05日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2022年01月05日
- 2020年12月07日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2020年12月07日
- 2020年06月25日
- 使用上の注意
- プロスタルモン®・F注射液1000・2000 使用上の注意改訂のお知らせ
- 2020年06月25日
- 2019年12月02日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2019年12月02日
- 2018年12月20日
- その他の安全性
- プロスタルモン®・F注射液1000・2000「適正使用」に関するお願い
- 2018年12月20日
よくあるご質問FAQ
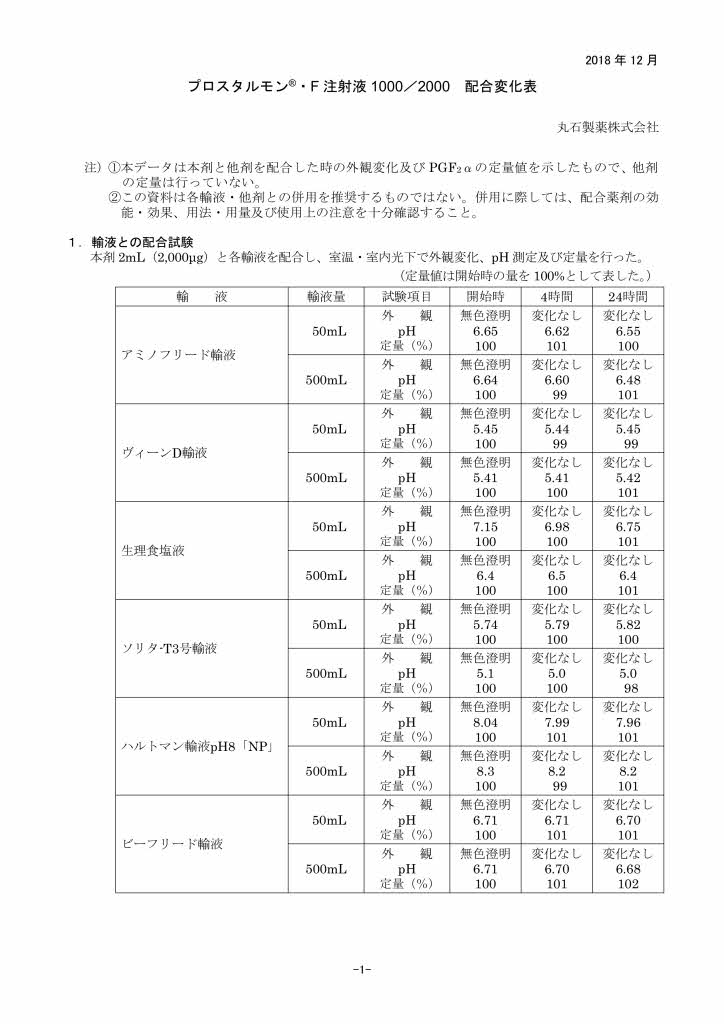
配合変化表はありますか?
ございます。こちらからダウンロードしていただけます。
輸液量を減らして使用できますか?
本剤は刺激性に問題がない1)ため、輸液量を減らすことは可能ですが、投与速度を正確に調節できる輸液量で使用してください。
参考文献
1)インタビューフォーム:Ⅸ.非臨床試験に関する項目 2.毒性試験
投与中に遮光する必要はありますか?
投与中に遮光する必要はありません。使用期限(3年)の品質保持のため貯法は「遮光、室温保存」1)ですが、使用する際の遮光は不要です。2)
参考文献
1)添付文書:貯法
2)インタビューフォーム:Ⅳ.製剤に関する項目 5.製剤の各種条件下における安定性
輸液フィルターの通過性に関するデータはありますか?
本剤は微量含有製剤であり、持続静脈内投与を行うため、特殊な性能を持つフィルター(エンドトキシン除去性能を持つフィルター)を使用すると吸着することがあります。
なお、フィルター通過性試験試験は行っており、本剤のインタビューフォームに掲載しております。
詳細はインタビューフォームをご覧ください。
参考資料
インタビューフォーム:Ⅳ.製剤に関する項目 7.他剤との配合変化
(腸管蠕動亢進での使用)効果の判定に必要な期間は?
3日間です。
3日間投与しても効果が認められない場合は直ちに投与を中止し、他の治療に切り替えてください。
<用法用量 抜粋>
(2) 腸管蠕動亢進には
3) 3日間投与しても効果が認められないときは直ちに投与を中止し他の療法にきりかえる。
参考文献
添付文書:【用法・用量】
喘息患者に使用しても良いか?
気管支喘息又はその既往歴のある患者への使用は禁忌です。
本剤は気管支平滑筋の収縮作用を有しています。気管支喘息のように既に気道が狭くなっている患者には、PGF2αの投与により更に肺抵抗が上昇し1)、症状が悪化する可能性があります。
<添付文書>2)
<禁忌>
気管支喘息又はその既往歴のある患者〔気管支を収縮させ気道抵抗を増加し、喘息発作を悪化又は誘発するおそれがある。〕
<重要な基本的注意>
(1) 心室細動、心停止、ショック、気管支収縮があらわれることがあるので、投与中は循環・呼吸器に対する観察を行い、異常が認められた場合には投与を中止し、適切な処置を行うこと。
<重大な副作用>
(2) 呼吸困難
喘鳴、呼吸困難等(頻度不明※)があらわれることがあるので、このような場合には投与を中止すること。
※:頻度不明は自発報告による。
参考文献
1)SMITH A.P.:Clinical Science 1973;44:17-25.【PGF0730001】
2)添付文書:【禁忌】、【使用上の注意】(2)重要な基本的注意
お役立ちツールUSEFUL TOOL
各コンテンツ(動画・PDF等)は、ご自由にダウンロードしてお使いください。
なお、編集・改変等はご遠慮ください。(一部ポスターは除く)
2018年12月01日
2020年12月02日
2020年12月07日
ツールNo:113410