腸内細菌目細菌(Enterobacteriales)
■細菌学的特徴
腸内細菌と腸内細菌目がしばしば混同されて使われているので、先に区別しておきます(図1)。腸内細菌は、腸内にいる細菌(特に常在菌)全般を指す用語です。腸内細菌目の細菌も含まれますが、多くはそれ以外の嫌気性菌です。腸内細菌目は、大腸菌の仲間で、詳細は省きますが、通性嫌気性グラム陰性桿菌のうち、いくつかの共通点を有する細菌の分類で、必ずしも腸内にいるとは限りません。なお、腸内細菌科細菌は、科の上位分類である腸内細菌目(Enterobacterales)の意味としても使われることがあります。なお、腸内細菌科細菌(Enterobacteriaceae)は、腸内細菌目(Enterobacterales)の下位分類です。
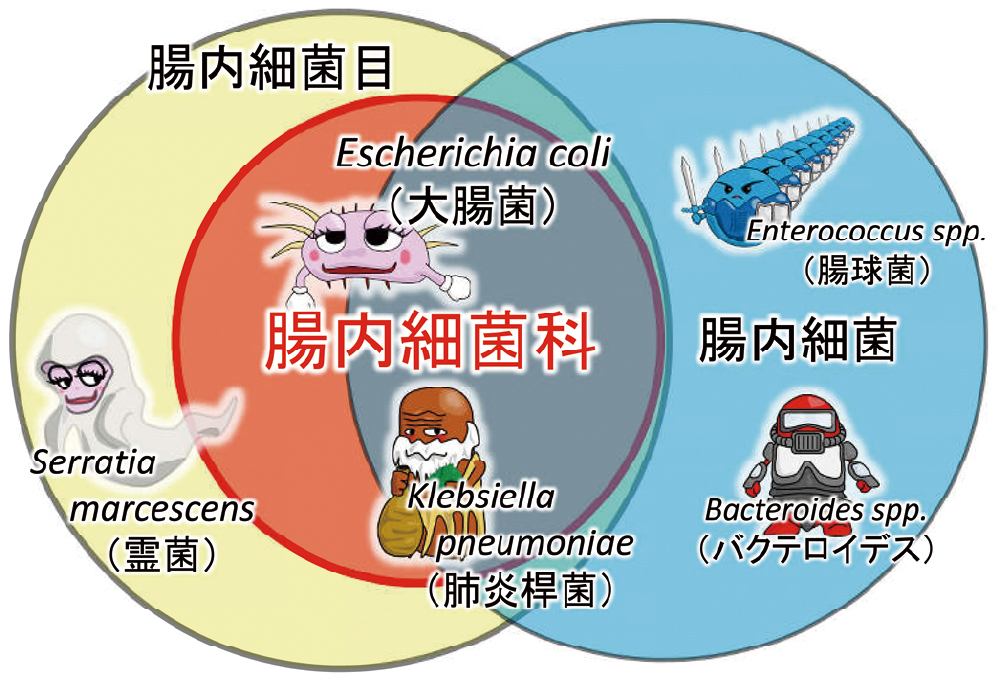
腸内細菌目と腸内細菌科は学術的な分類の科の名称で、目が科の上位にあたります。一方、腸内細菌は腸内にいる常在菌の総称です。一部は重複しています。腸内細菌科の代表が大腸菌、肺炎桿菌です。腸内細菌科以外の腸内細菌目として霊菌などが、腸内細菌目以外の腸内細菌として腸球菌やバクテロイデスなどがあります。
通性嫌気性というのは、酸素を用いる好気的な条件(呼吸)、酸素を用いない嫌気的条件(発酵)の両方でブドウ糖を分解し、エネルギーを得る能力を持っていることを意味します(図2)。食事(エネルギー源やビタミンなど)にはあまりこだわりがないため、普通の培地でもよく育つというのが特徴の一つで、腸内だけではなく、環境中でもしばらくは生息することができます。ブドウ球菌と同様、院内感染しやすい細菌です。
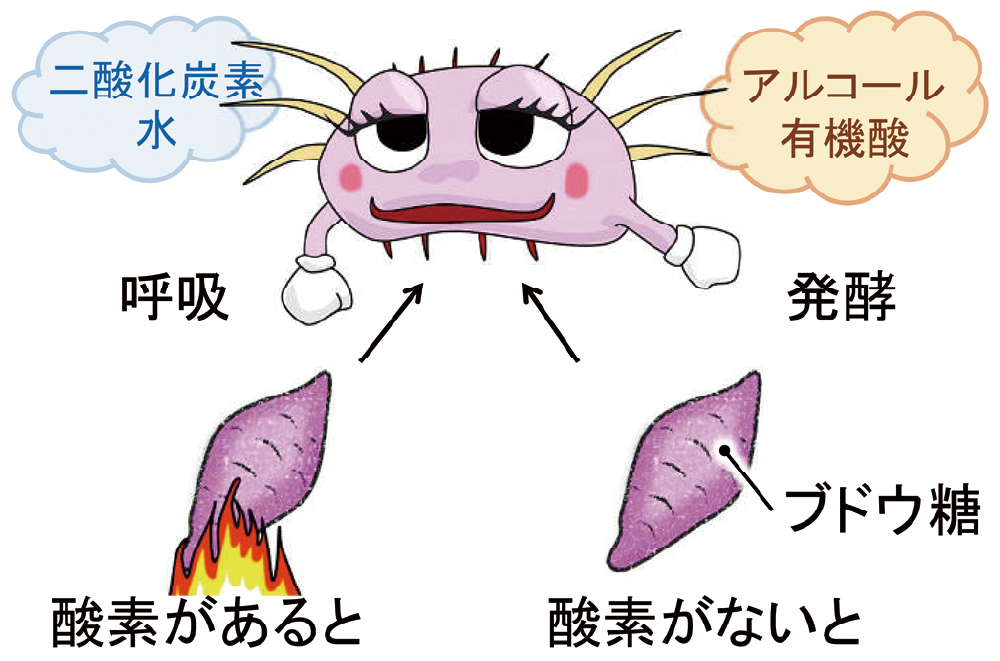
酸素があるときには呼吸により、ないときには発酵により、ブドウ糖を利用することができる性質です。
呼吸では完全燃焼するため二酸化炭素と水が、発酵ではアルコールか有機酸が発生します。
腸内細菌目に含まれる菌種は非常に多く、列挙しきれません。代表的な属名は、Escherichia、Klebsiella、Salmonella、Shigella、Citrobacter、Enterobacterですが、中でも、Escherichia coli(大腸菌)とKlebsiella pneumoniae(肺炎桿菌)が重要です(図3)。
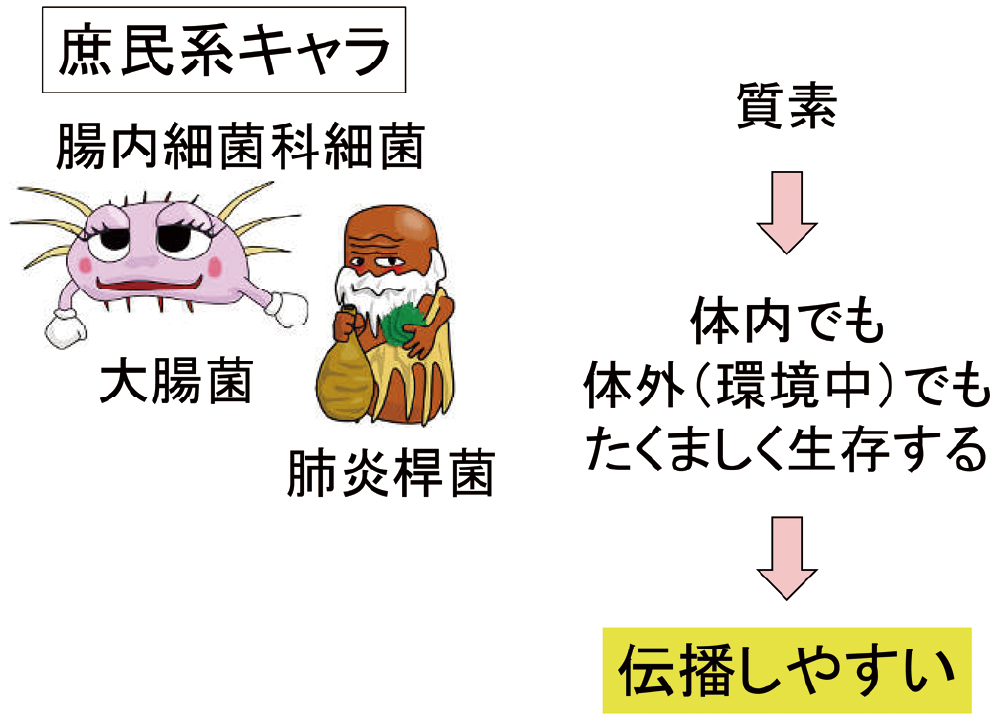
黄色ブドウ球菌と同様、大腸菌や肺炎桿菌は庶民系でとても質素です。そのため、体内だけではなく、栄養が少ない過酷な環境下でもたくましく生存することができます。そのような特徴が、伝播しやすさと関連している可能性があります。
なお、本題と関係ありませんが、肺炎桿菌は、大酒家に大葉性肺炎を起こすことが古くから報告されており、とっくりと大葉を持っています。
■大腸菌(Escherichia coli)
腸内常在菌の一つですが、尿路感染症や感染性胃腸炎の代表的な菌種です。また、血液からの分離が最も多い菌種でもあります。大腸菌も、起こしやすい病気の種類によって、尿路病原性大腸菌や腸管病原性大腸菌(広義)などに分類されます。新生児の髄膜炎の原因菌としても、B群溶連菌(group BStreptococcus,GBS)に並んで有名です。
□尿路病原性大腸菌
尿路感染症を起こしやすい大腸菌は、尿路病原性大腸菌(UropathogenicE. coli, UPEC)として知られています。大腸菌は、尿路感染症の原因菌として、ぶっちぎりの第一位です。特に、女性の場合、肛門と外尿道孔が近いため、腸内常在菌が膀胱炎を起こしやすいことが知られています。
□腸管病原性大腸菌(広義)
腸管病原性大腸菌の中で最も有名なのが、腸管出血性大腸菌(EnterohemorrhagicE. coli, EHEC)で、私のキャラでは、「ベロダシ」というベロを出した大腸菌として描いています(図4)。ご存知かもしれませんが、ベロ毒素(Verotoxin, VT)という腸管毒素を産生するというダジャレです。VTは細胞傷害性の毒素で、大腸の血管内皮を傷害することで、血便の原因となります。EHECよりも、O157(オー・イチ・ゴ・ナナ)の方が聞きなじみがあるかもしれませんが、大腸菌につけられた背番号の様なもので、O1から順番につけられています。特定の背番号の大腸菌がEHECであることが分かっています。もっと厳密に述べると、O157:H7など、Hも組み合わせて分類します。ちなみに、Oはリポ多糖(lipopolysaccharide, LPS)、Hは鞭毛の抗原性で、他にKという莢膜の抗原も知られています。新生児の髄膜炎を起こしやすいのはK1と呼ばれており、強そうな名前にビビってしまいそうです。

ベロ毒素を産生する大腸菌のキャラ名です。腸管出血性大腸菌(EHEC)とも呼ばれます。
腸管病原性大腸菌としてはEHEC以外の、狭義の腸管病原性大腸菌(EnteropathogenicE. coli, EPEC)、腸管毒素原性大腸菌(EnterotoxigenicE. coli, ETEC)などがあります。ETECによる感染症はコレラに類似した症状を示し、旅行者下痢症の原因としてもよく知られています。
腸管病原性大腸菌の多くは、ヒトの常在菌ではなく外部からの侵入によるものです。特に、EHECの場合には、牛由来がほとんどと考えられます。
■肺炎桿菌(Klebsiella pneumoniae)
属名の語尾が-ellaとなっていますが、-ellaがつくものはグラム陰性菌です。つまり、「裸族」(正確には「え裸族」)は陰性菌です。クレブシエラ属は、大腸菌よりやや大型で、鞭毛を持ちません。Klebsiella pneumoniaeが代表的ですが、K. oxytocaなどもしばしば臨床的に分離されます。K. pneumoniaeの和名は肺炎桿菌ですが、名前の割に市中肺炎の原因菌となることは少なく、肺炎での分離頻度は大腸菌や緑膿菌と同程度です。衛生状態などが改善されたために以前よりも減ったのかもしれません。アルコール中毒者の大葉性肺炎では注意すべき細菌の一つであるということで、キャラには、「とっくり」と「大葉」を持たせています(図3)。大腸菌と同様、菌血症や尿路感染症など多彩な感染症の原因となりうる細菌で、胆道感染症もよく知られています。また、多量のムコ多糖を産生する高粘稠性の菌株が高病原性と関連しているとされており、近年注目を集めています。
カルバペネム耐性腸内細菌目細菌(Carbapenem-resistantEnterobacterales, CRE)
カルバペネマーゼ産生腸内細菌目細菌(Carbapenemase-producingEnterobacterales, CPE)
日本では頻度は低いながら、治療に難渋することのある細菌で、赤の大関に位置付けています。CREとCPEでは、状況によってインパクトが異なりますが、重複する部分もありますので併せて説明します。
■菌滅のカルバに抵抗する鬼
菌滅のカルバこと、カルバペネム系薬が開発された結果、どうなったでしょう。そう、カルバペネム耐性菌が誕生しました。モンスター系によく効く抗菌薬というのは、腸内の先住民ともいえる大腸菌や肺炎桿菌などの「腸民」にもよく効きます。つまり、モンスター系の感染症を治療しようとした結果、腸民が犠牲になってしまいます(図5)。もちろん、腸民もやられっぱなしではありません。反乱を起こし、鬼と化しました(図6)。これが、CREやCPEと呼ばれるようになりました。CRE感染症は5類全数の対象となっています(表1)。

「モンスターが出現しました。今から、カルバペネムを投下します」もし、あなたが腸民だったらどうでしょう。カルバペネム系薬は、モンスターによく効くだけではなく、先住民を犠牲にするということをお忘れなく。
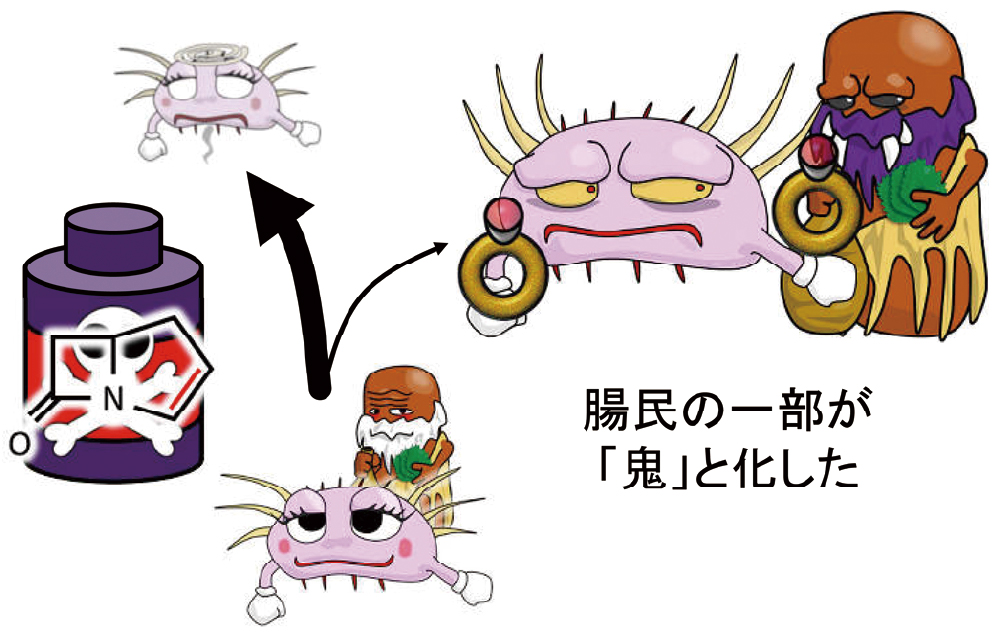
多くの腸内細菌は死滅しますが、一部の腸内細菌が生き残りました。これが、CREやCPEという鬼になりました。

CREの判断は、上記の基準に沿えばよいため、比較的簡単です。難しいのは、CPEの方です。ここで、CREとCPEの相違について、簡単に説明しておきます。CREとCPEは完全には重複していません。図7に示すように、一部重複していますが、耐性の有無とカルバペネマーゼの有無で分けると4つに分類できます。
カルバペネム系薬とCRE/CPEの概要が分かったところで、次にカルバペネマーゼの解説に進みたいと思います。
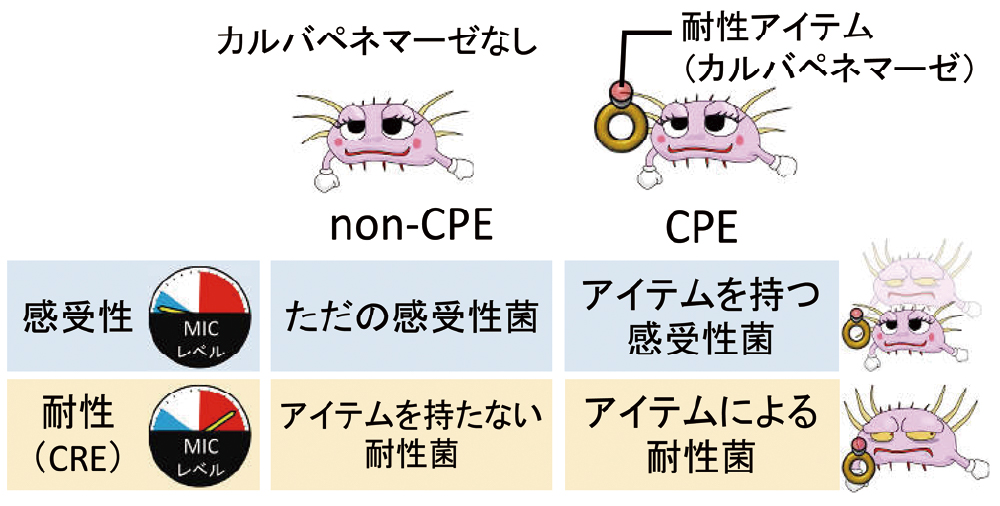
カルバペネマーゼを持たず、カルバペネムに感受性の場合、ただの感受性菌です。カルバペネマーゼを持っている耐性菌は、CPEかつCREです。この2つだけなら話は簡単ですが、アイテムを持たない耐性菌、アイテムを持つ感受性菌がいます。ただし、アイテムを持つ感受性菌は、検査上の感受性なので注意が必要です。
■意味もなくビアードパパにメロメロだ
「なんのこっちゃ」と言われそうですが、抗MRSA薬に引き続き、カルバペネム系薬の覚え方です。抗MRSA薬のようにおいしそうなにおいがします。こちらは、教え子の一人が考えてくれた覚え方です。この場を借りて感謝申し上げます。
現在、注射用のカルバペネム系薬として日本で利用できるのはたったの5つしかないので覚えてしまおうという作戦です。意味もなく(
イミペネム)、
ビアー
ドパ
パに(
ビアペネム、
ドリペネム、
パニペネム)、
メロメロだ(
メロペネム)(図8)。どうですか。ちなみに、内服のカルバペネム系薬として、テビペネム-ピボキシルがあります。また、海外ではエルタペネムも使えます。ファロペネムは、ペネム系薬で、カルバペネム系薬ではありませんが、スペクトルはカルバペネム系薬に近く、内服可能な広域抗菌薬です。尚、β-ラクタム系薬は、語尾または語頭を見れば、ほぼ系統が分かります。-シリンがつけばペニシリン、セフ-もしくは-セフがつけばセフェム系薬、-ペネムがつけばほとんどがカルバペネム系薬です。

抗菌薬をすべて覚えるのは大変ですが、5つしかない注射用カルバペネム系薬ですので、語呂で「おいしく」身につけましょう。
■カルバペネムを分解する「BAD」な輩
カルバペネマーゼは、β-ラクタマーゼの一種ですが、種類が多く、分類上はやや複雑です。今回は、CPEに関連したカルバペネマーゼに絞ってご紹介します。
Ambler分類は避けて通れませんので、簡単に説明しておきます。最も代表的なβ-ラクタマーゼの分類で、活性中心の構造の類似性により大きくA~Dの4つに分類されます。活性中心の構造は、分解する基質ともある程度関連しており、例えば、Class Aが分解できるのは主にペニシリン系薬であるのに対し、Class Bはカルバペネム系薬を含むほとんどのβ-ラクタム系薬を分解します。しかしながら、Class AやClass Dの中にもカルバペネム系薬まで分解できる酵素が知られています。したがって、カルバペネム系薬を分解するβ-ラクタマーゼは、Class B、A、Dで、「BAD」です(図9)。これらのβ-ラクタマーゼは、腸内細菌目細菌だけではなく、緑膿菌を代表とするブドウ糖非発酵菌やバクテロイデスを代表とする嫌気性菌など、他のグラム陰性桿菌も保有しています。本稿では、特に、腸内細菌目でよく知られているカルバペネマーゼとして、OXA-48とIMPを中心にいくつかご紹介します(図10)。
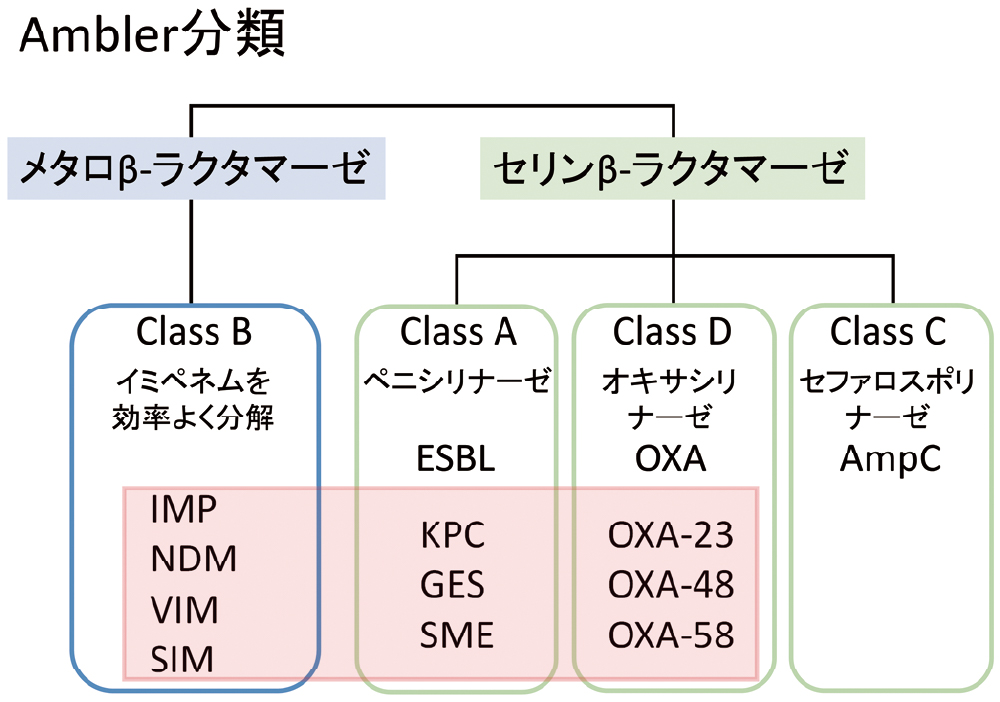
Ambler分類で、カルバペネマーゼとして最も代表的なのは、Class Bのメタロ型と呼ばれるものですが、Class AとDの中の一部もカルバペネマーゼです。つまり、「BAD」なカルバペネマーゼです。

日本で最も多いCPEは、IMP-6と呼ばれるClassBのカルバペネマーゼを持つ大腸菌や肺炎桿菌です。また、ClassDのカルバペネマーゼとしてよく知られているのはOXA-48です。
■OXA-48のセンターは悪女のセリン
アイドルグループのような名称ですが、OXA(オキサ)型と呼ばれるβ-ラクタマーゼの一種で、カルバペネム系薬を分解する能力を備えています。OXA型は、オキサシリン(
oxacillin)を効率よく分解することに由来します。Ambler分類ではClass Dに属します。アイドルグループばりに、不動のセンターが存在します。その名は「セリン」。魅了されそうな名前ですが、ご存知の通りアミノ酸残基です。センター(活性中心)がセリンであるタイプをセリン型β-ラクタマーゼと呼びます。
OXA型は200以上のバリアント(亜型)が知られていますが、全てがカルバペネマーゼ活性を持つわけではなく、23、48、58が代表的なカルバペネマーゼです。48に類似した181などもカルバペネマーゼ活性を持ちます。
セリン型β-ラクタマーゼは、真核生物で見られるセリン型プロテアーゼの親戚のような酵素で、活性中心のセリンは、側鎖がヒドロキシメチル基(‒CH2OH)という構造をしており、末端のOHの部分がβ-ラクタム環と反応します(図11)。
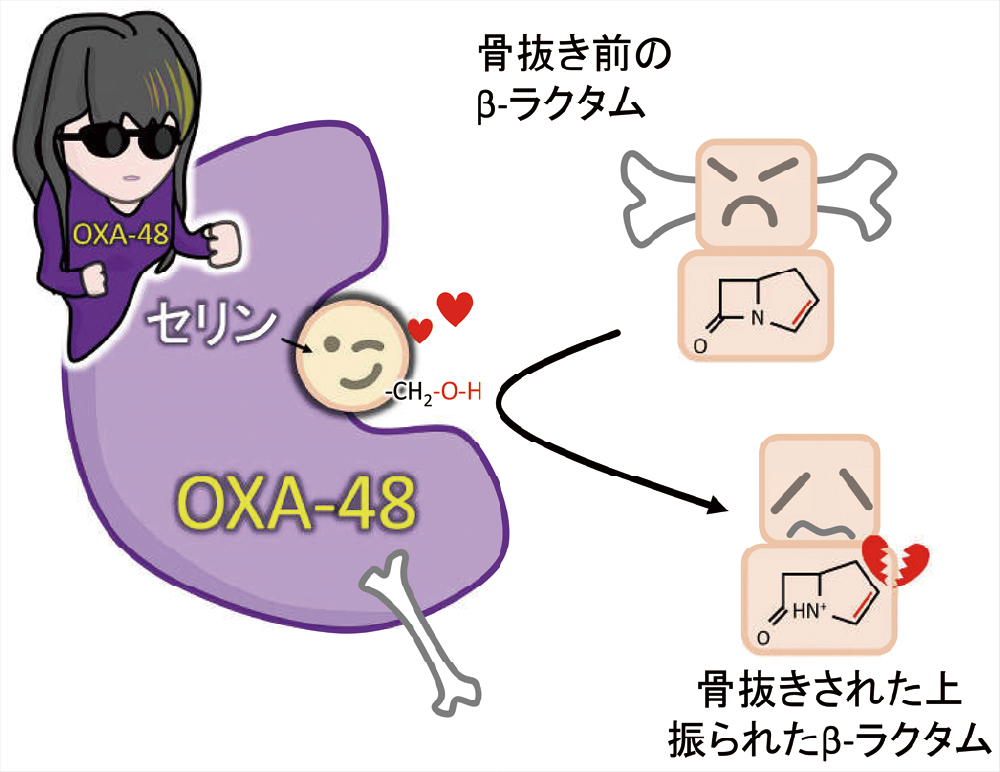
活性中心にあるセリンの側鎖(-CH2-OH)がβ-ラクタム環と反応し、β-ラクタム系薬を骨抜きにします。セリンという魅力に取りつかれたβ-ラクタム系薬は、骨抜きにされた上、振られてしまいます。
実は、β-ラクタム系薬の標的であるペニシリン結合蛋白(PBP)も同様にセリンが活性中心にあり、β-ラクタム系薬が結合することでPBPの本来の機能である細胞壁の合成が阻害され、細菌が死に至ります(図12)。PBPの場合には、セリンとβ-ラクタム系薬は結ばれたまま添い遂げますが、β-ラクタマーゼの場合には、β-ラクタム系薬がセリンに惹きつけられ、骨抜きにされた後、放り出されます。つまり、振られてしまうわけですね。悪女です。
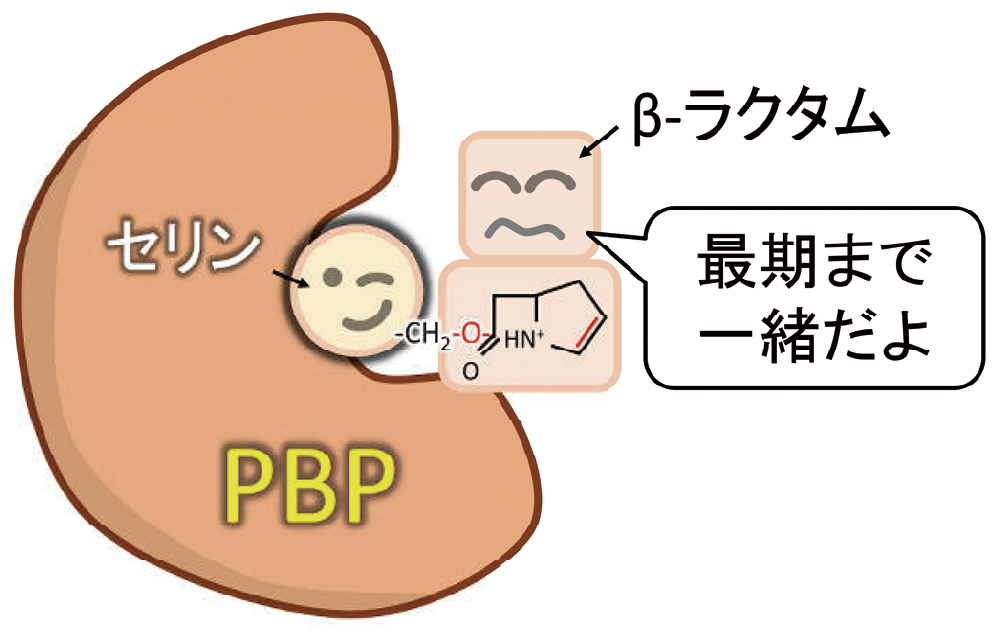
β-ラクタマーゼと同じ構造
PBPも活性中心にセリンを持ち、β-ラクタム系薬と結合することでPBPの本来の機能である細胞壁の合成が阻害されます。ただし、β-ラクタマーゼと異なり、PBPのセリンとβ-ラクタム系薬は結ばれたまま、最期まで添い遂げます。
■ゲスなカルバペネマーゼ
腸内細菌目が産生する他のセリン型カルバペネマーゼとしては、Class AのKPC型とGES型がよく知られています。KPCは Klebsiella pneumoniae carbapenemaseの略で、名前の通り、肺炎桿菌から検出され、欧米に多いカルバペネマーゼです。日本ではほとんど報告がありません。GES型は Guiana extended- spectrumの略で、特に、GES-5産生株が比較的多く検出されます。
■IMPはヘビメタの小悪魔
IMPは、イミペネム(
imi
penem)の略に由来しますが、奥が深い裏の意味も隠されています。imp(インプ)という西洋で知られる体調10cmほどの小さな悪魔です。カルバペネマーゼのIMPもある意味「悪魔」ですからね。Ambler分類ではClass Bに属します。Class Bは、活性中心に亜鉛イオンなどの金属イオンを持ち、メタロ型β-ラクタマーゼとも呼ばれます。
セリン型β-ラクタマーゼと同様、メタロ型β-ラクタマーゼは真核生物で見られるメタロ型プロテアーゼの仲間です。セリン型のセリンの代わりに、金属イオンがβ-ラクタム環と反応し、加水分解します(図13)。一般に、セリン型よりも基質が広く、強力です。そのため、ペニシリン系薬からカルバペネム系薬まで、効率よく分解することができます。まるで人を魅了するかのように、ほとんど全てのβ-ラクタム系薬を惹きつけ、骨抜きにします。まさに、ヘビメタの小悪魔です(図13)。
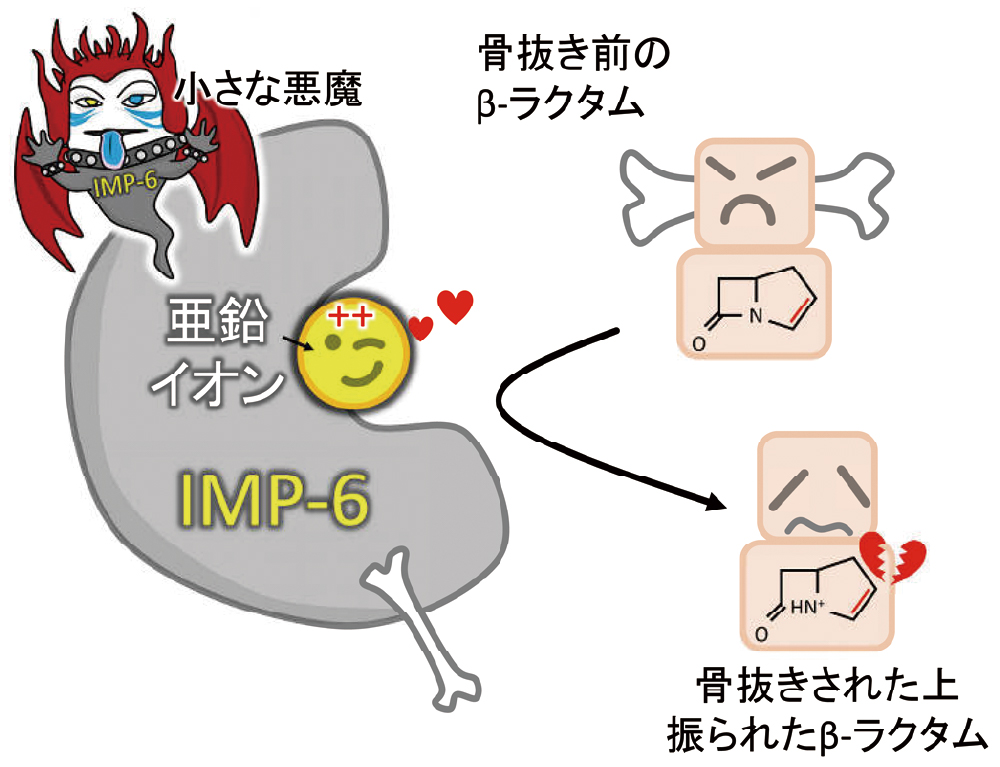
セリン型のセリンと同様、活性中心の亜鉛イオンがβ-ラクタム系薬を骨抜きにしますが、その力は一般にセリン型よりも強力です。ほとんどのβ-ラクタム系薬を魅了する小悪魔です。ちなみに、imp(インプ)には小さな悪魔という意味があります。
腸内細菌目が産生する他のメタロ型カルバペネマーゼとしては、NDM型とVIM型がよく知られています。NDMは
New
Dehli
metalobetalacatamaseの略で、最初に分離された都市(インドのニューデリー)の名称にちなんでいます。従来、メタロ型と言えば、ほとんどが環境菌である緑膿菌などのブドウ糖非発酵菌が保有しているというイメージでしたが、NDM-1は常在菌である腸内細菌目細菌が保有しているということで、世界的に大きな衝撃となりました。VIM型は、
V
erona
im
ipenemaseの略で、こちらも最初に分離された都市(イタリアのベローナ)の名称にちなんでいます。
NDM型やVIM型は、欧米ではKPCに次いで多くみられますが、日本では比較的稀です。日本のCPEが持つカルバペネマーゼはほとんどがIMP-6ですが、グローバル化によって、勢力図は変わるかもしれません。IMP-6は、日本に多いというだけではなく、後述のように「隠れ鬼」としての特徴を持っています。
■普通の腸民のふりをしている隠れ鬼~ステルス型CPE
CREは、カルバペネムに耐性を示す腸内細菌目細菌です。カルバペネムに耐性を示すということは、「β-ラクタム系薬が全て使えない」ということとほぼ同義です。したがって、CREは菌滅のカルバさえも返り討ちにする最強の鬼と化した腸民と言えるでしょう。しかし、もっと怖いのは、普通の腸民のふりをして、知らないうちに近づく「隠れ鬼」の存在です(図14)。

ステルス型とは、CPEなのにCREではない、カルバペネマーゼというアイテムを持つ感受性菌です(図7参照)。検査上、感受性を示しますが、臨床的にはカルバペネムが効かない「隠れ鬼」的存在です。
OXA型同様に、KPC、GES、IMP、NDM、VIMも、アミノ酸の一部が変異したバリアントがいくつも見つかっています。IMPの場合、特にIMP-1とIMP-6がよく分離されます。IMP-6産生株は、検査上、カルバペネムに耐性と判定されないことがしばしばあります。臨床的にも耐性でなければ問題ありませんが、治療上は耐性を示すことが問題です。しかも、密かに広がっている可能性があります。このように、CREの基準を満たさないCPEのことを「ステルス型CPE」と呼んでいます。日本独自の呼び方です。
ステルス型CPEは検査上での課題でもあります。特に、近年増加している基質特異性拡張型β-ラクタマーゼ(extended-spectrumβ-lactamase, ESBL)産生菌との鑑別です。ESBL産生菌はペニシリン系薬とセフェム系薬に耐性を示しますが、カルバペネム系薬に感受性を示します。ただ、ステルス型CPEと異なり、ESBL産生菌は治療上もカルバペネム系薬に感受性を示します。ESBLは、セフェム系薬のうちセファロスポリン系薬を分解しますが、セファマイシン系薬は分解できません。つまり、ESBL産生菌は原則としてセファマイシン系薬に感受性を示します。一方、ステルス型CPEは、検査上カルバペネム系薬に感受性を示しますが、ほとんどの場合セファマイシン系薬に耐性を示します。したがって、ESBL産生菌とステルス型CPEのセファマイシン系薬に対する感受性の相違が、ステルス型CPEを疑う契機となります(表2)。
腸内細菌目の耐性菌は、ESBLやCRE/CPEだけではなく、多様化、複雑化して増加しています。今後の動向にも引き続き注意が必要な耐性菌の一つです。
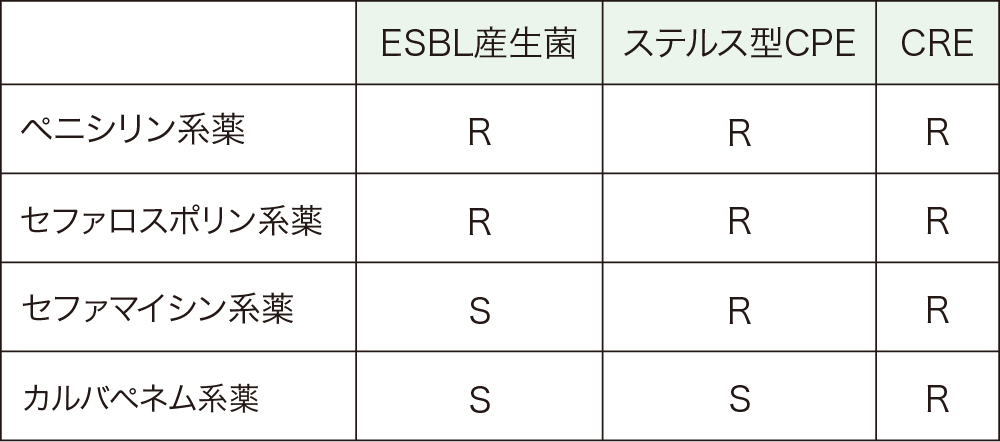 ※R:耐性、S:感受性
※R:耐性、S:感受性
基質特異性拡張型β-ラクタマーゼ(extended-spectrumβ-lactamase, ESBL)産生菌
赤の関脇である基質特異性拡張型β-ラクタマーゼ(ESBL)産生菌をご紹介します。
ESBL産生菌には複数の菌種が含まれますが、前述のCRE/CPEと同様、ほとんどが腸内細菌目細菌、特に、大腸菌と肺炎桿菌です。AMRの中でも、ESBLは最も複雑です。できるだけ噛み砕いて説明するため、若干厳密性に欠ける部分がありますことをご容赦ください。
■β-ラクタム系薬のスペクトルとβ-ラクタマーゼの関係
β-ラクタム系薬は、抗菌薬の中でも最も種類の多いグループで、大まかに、ペニシリン系薬、セフェム系薬、カルバペネム系薬に細分化されます。構造上の相違もさることながら、臨床的に重要な相違はスペクトルとβ-ラクタマーゼに対する安定性です。一部の例外はありますが、ペニシリン系薬<セフェム系薬<カルバペネム系薬の順にスペクトルが広くなり、かつ、β-ラクタマーゼにも安定になります。
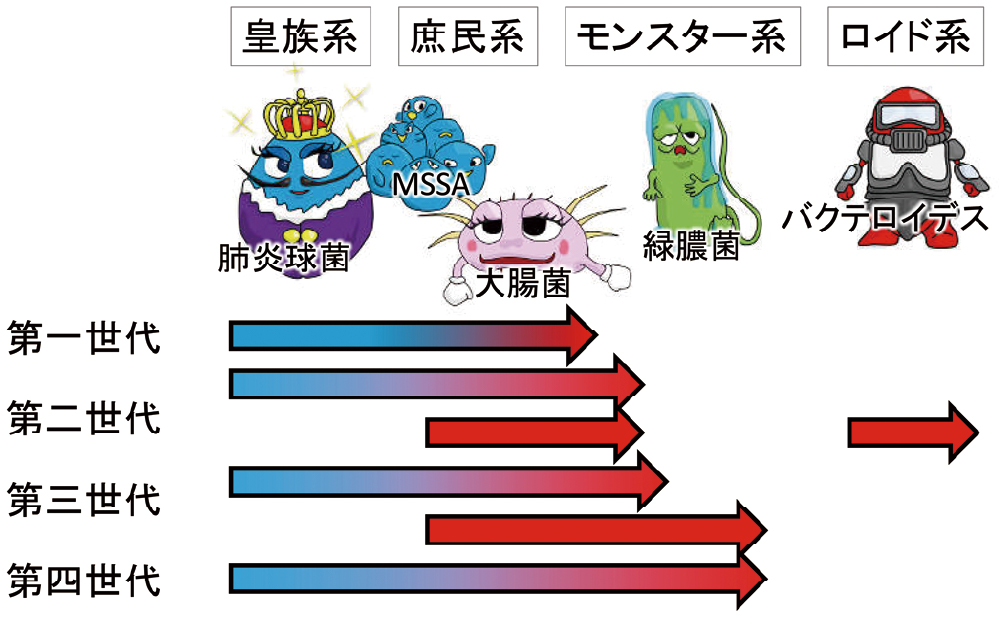
おおよそのスペクトルを理解するには、代表的な細菌をイメージするとよいでしょう。ペニシリン系薬は主に皇族系(特に肺炎球菌)、セフェム系薬は庶民系(特に腸内細菌目)、カルバペネム系薬はモンスター系(緑膿菌など)とロイド系(バクテロイデスなどの嫌気性菌)までカバーする、といった感じです(図15)。
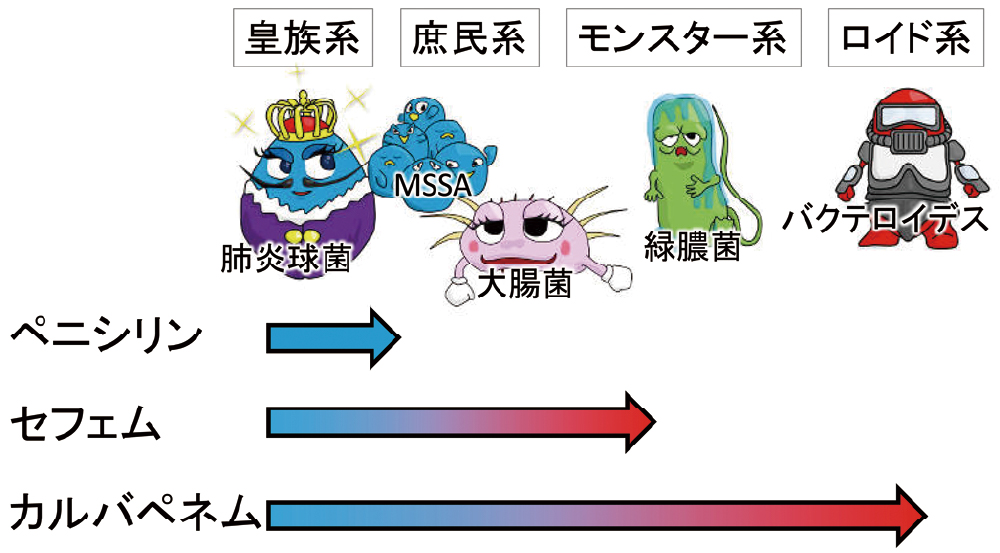
β-ラクタム系薬のスペクトルを理解しやすくするために、まず、肺炎球菌、MSSA、大腸菌、緑膿菌、バクテロイデス(嫌気性菌の代表)の5つを指標にしてみましょう。ペニシリン系薬は肺炎球菌、セフェム系薬は肺炎球菌から大腸菌まで(一部は緑膿菌まで)、カルバペネム系薬は全てをカバーするイメージになります。図では表していませんが、ペニシリン系薬の一部は、緑膿菌や嫌気性菌をカバーします。
β-ラクタマーゼは、基質特異性の観点から、ペニシリナーゼ、セフェマーゼ、カルバペネマーゼの3つに分類することができます。ペニシリナーゼはペニシリン系薬のみを分解します。セフェマーゼはペニシリン系薬とセフェム系薬を分解できますが、カルバペネム系薬を分解できません。カルバペネマーゼはペニシリン系薬~カルバペネム系薬まで、ほとんど全てのβ-ラクタム系薬を分解することができます。
今回のトピックスであるESBLは、セフェマーゼと同一とは言わないまでも、臨床的に問題になっているセフェマーゼのほとんどはESBLです。では、ESBLとは何者なのか、もう少し詳しくご紹介します。
■ESBLはペニシリナーゼがセフェマーゼに進化したもの
厳密に説明すると異なりますが、元々はペニシリナーゼであったものが、突然変異によりセフェマーゼに進化したものである、と言えます(図16)。特に、ESBLが発見された当初はそのように認識されていました。ESBLは、多くの型と亜型を含み、非常に複雑です。代表的なESBLとして、TEM、SHV、CTX-Mが知られ、しかも、それぞれ200~250程度の亜型があり、さらに増え続けています。
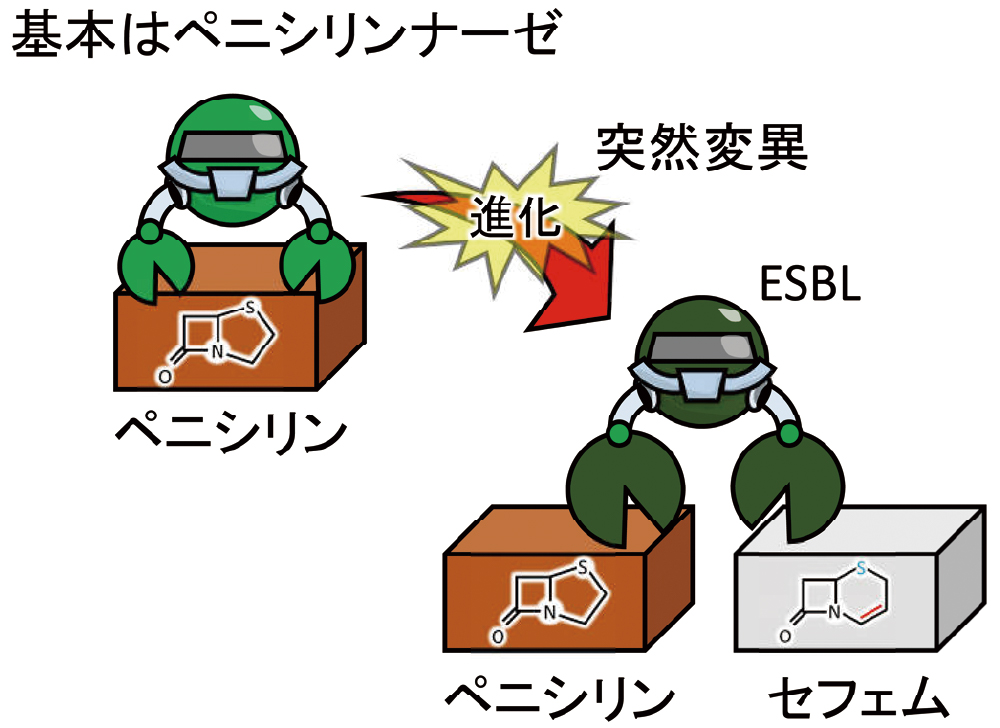
ESBLとは、元々ペニシリン系薬のみ分解していた酵素が、突然変異により、基質を拡張しセフェム系薬まで分解できるように進化したものです。
ESBLの理解を助けるために、基質であるセフェム系薬についてももう少し説明しておきます。セフェム系薬は、β-ラクタム系薬の中でも種類が多く、構造と活性の相違から、セファロスポリン系薬とセファマイシン系薬に分類されます*。また、世代によっても分類され、第一~四世代に分かれます。
*厳密にはオキサセフェム系薬もありますが、ここでは取り上げません。
セフェム系薬の特徴として、以下の2点は押さえておきたいところです。
- □ 腸球菌、リステリアには元々無効である。
- □ セファロスポリン系薬は嫌気性菌に弱い。
一般にペニシリン系薬よりもセフェム系薬の方がスペクトルは広いのですが、以上の2点においてはセフェム系薬の方がペニシリン系薬に劣る場合があります。
また、モンスター系である緑膿菌に対する作用は、第三世代の途中で分かれています。つまり、第一・二世代は抗緑膿菌作用なし、第四世代は抗緑膿菌作用ありですが、第三世代は、ないものとあるものが混ざっています(表3、図17)。
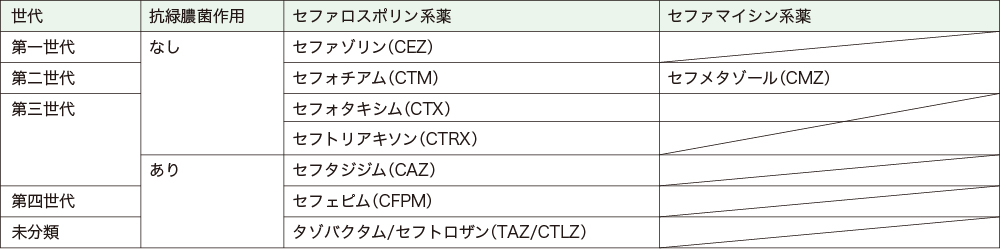
セフェム系薬は、世代によってスペクトルが異なるため、もう少し細かく分けてみます。第一~二世代は緑膿菌に対する効果(抗緑膿菌作用)がありません。第三世代は、抗緑膿菌作用があるものとないものがあり、抗緑膿菌作用があるものは、肺炎球菌などのグラム陽性菌をカバーできなくなります。第四世代は、第一世代と第三世代の良いところを足し合わせたスペクトルとなります。ただし、第二世代のセフメタゾールを除き、セフェム系薬は嫌気性菌が苦手です。
ESBLに話を戻すと、より正確にはESBLはセフェマーゼではなくセファロスポリナーゼです。なぜなら、ESBLはセファマイシン系薬の分解活性がほとんどないためです。このような理由から、ESBL産生菌に対して、セファマイシン系薬を使用するという選択肢も出てきます。
もう少し詳細なセフェム系薬の分類とスペクトルをご紹介しておきます(表4)。
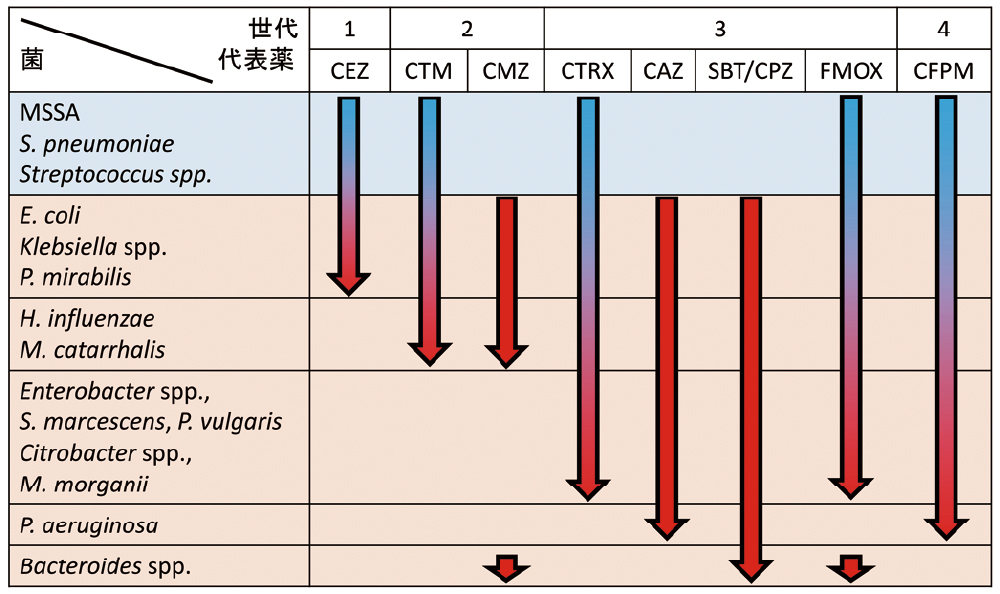 略語は表3と本文を参照
略語は表3と本文を参照
全体を見て分かるのは、セフェム系薬はいずれも一般に、Proteus mirabilis、Escherichiacoli、Klebsiella spp.をカバーしていることです。頭文字をとって、PEKとも呼ばれますが、主に尿路感染症の原因菌となるような腸内細菌目の菌種です。
第二世代では、PEKに加えて、インフルエンザ菌やモラクセラにもスペクトルが拡大します。特に、モラクセラが産生するβ-ラクタマーゼはペニシリナーゼですが、第一世代セファロスポリン系薬までは分解し、第二世代以降は分解されにくくなるためです。
第三世代になると、ほとんどの腸内細菌目をカバーします。前述のように、抗緑膿菌作用の有無はポイントの一つですが、表3で出てこなかったセフェム系薬として、スルバクタム/セフォペラゾン(SBT/CPZ)とフロモキセフ(FMOX)があります。SBT/CPZのうち、SBTはβ-ラクタマーゼ阻害薬で、CPZが抗菌活性の本体です。FMOXはオキサセフェムと呼ばれるもので、硫黄(S)が酸素(O)に置き換わったものです。双方ともバクテロイデスまでスペクトルが拡大しており、SBT/CPZはCAZ+CMZ、FMOXはCTRX+CMZを組み合わせた感じのスペクトルになっています。
ただし、実際の使用に際しては、スペクトルだけではなく、組織移行性や半減期などの薬物動態も考慮する必要があります。
■ESBLの変遷~TEM型からCTX-M型へ
ESBLをもう少し理解するために、β-ラクタマーゼの代表的な分類法であるAmbler分類について復習しておきます(図9)。活性中心の構造により、クラスA~Dに分類されます。クラスA、C、Dは、活性中心がセリンになっており、セリン型と呼ばれます。クラスBの活性中心はセリンではなく、活性中心に亜鉛イオンなどの金属イオンを含んでいます。そのため、メタロ型もしくはメタロβ-ラクタマーゼ(MBL)とよばれます。活性中心の構造は、好適な基質にも影響し、クラスAは主にペニシリン系薬を分解するのでペニシリナーゼです。クラスAは、クラブラン酸やスルバクタム、タゾバクタムなどのβ-ラクタマーゼ阻害薬によって阻害されやすいという特徴を持ちます。ESBLのほとんどがクラスAに属します。
歴史的な変遷も理解の助けになります。ESBL産生菌の最初の報告は、1983年で、ヨーロッパで分離されたKlebsiella pneumoniaeから検出されたTEM型のESBLです。ただし、当時はまだESBLという言葉は使われていませんでした。続々とTEM型のセファロスポリナーゼが報告される中で、extended broad-spectrum beta-lactamases(EBS-Bla)という呼称を経て、extended spectrum beta-lactamases(ESBL)と呼ばれるようになったようです。
TEM型は、Ambler分類のクラスAに属するβ-ラクタマーゼで、以前から、ペニシリン系薬に加え、第一・二世代セファロスポリン系薬の一部を分解する活性が知られていました。しかし、第三・四世代の分解活性は当初ありませんでした。1983年に報告されたTEM型は、TEM-3で、第三世代セファロスポリン系薬であるセフォタキシム(CTX)を分解する活性を有していました。まだ、カルバペネム系薬が登場する以前のことですから、大きな問題となったことが分かります。なお、TEM-3は、CTXを分解するという意味で、別名CTX-1とも呼ばれますが、CTX-M-1とは異なります。
日本では、東邦大学の石井らが1995年に初めてESBLを報告しました。これが、現在ESBLの主流となっているCTX-M型の最初の報告例でもあります。ただし、報告当時はToho-1と呼ばれていました。2007年にCTX-M-1が報告され、後にβ-ラクタマーゼが体系化される中で、Toho-1はCTX-M型に含まれることが判明し、CTX-M型に分類され、現在はCTX-M-44と呼ばれるようになりました。
CTX-M型は、それまでに報告のあったTEM型やSHV型とは大きくアミノ酸配列が異なっていましたので、少なくともそれらが変異したものではないことは明らかでした。また、CTX-M型には、TEM型やSHV型のような進化前のペニシリナーゼが知られていません。つまり、CTX-M型は最初からセファロスポリナーゼであったということになります。したがって、これまでの定義から厳密にいうと、ESBLではなく、クラスAのセファロスポリナーゼと呼ぶべきですが、スペクトルの共通性からESBLとして扱われています(表5)。以上の背景から、ESBLとは次のようなものであると認識されるようになりました。
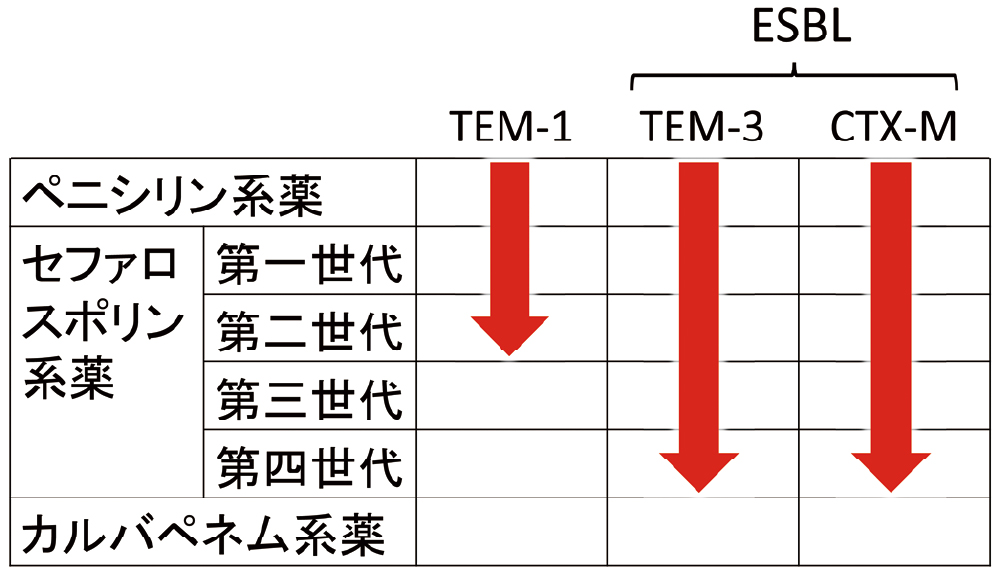
- □ Ambler分類のクラスAに属する。
- □ ペニシリン系薬から第三・四世代のセファロスポリン系薬までを分解する。
なお、クラスAのうち、カルバペネム系薬まで分解できるGES-5やKPCのような酵素はESBLとは呼ばれません。
■β-ラクタマーゼ阻害薬により、セファロスポリン系薬が再び有効になる
CTX-Mとセファロスポリン系薬およびβ-ラクタマーゼ阻害薬の関係について整理してみましょう。まず、CTX-Mの活性中心にあるセリンがセファロスポリン系薬を魅了し、惹きつけます(図18A)。セリンの水酸基とセファロスポリン系薬のβ-ラクタム環が結合し、セファロスポリン系薬は骨抜き(β-ラクタム環が切断、開環)になります(図18B)。骨抜きになったセファロスポリン系薬は用済みとなり、骨抜きのまま放り出されます(図18C)。このようにして、CTX-Mによってセファロスポリン系薬は次々に骨抜きにされてしまいます。
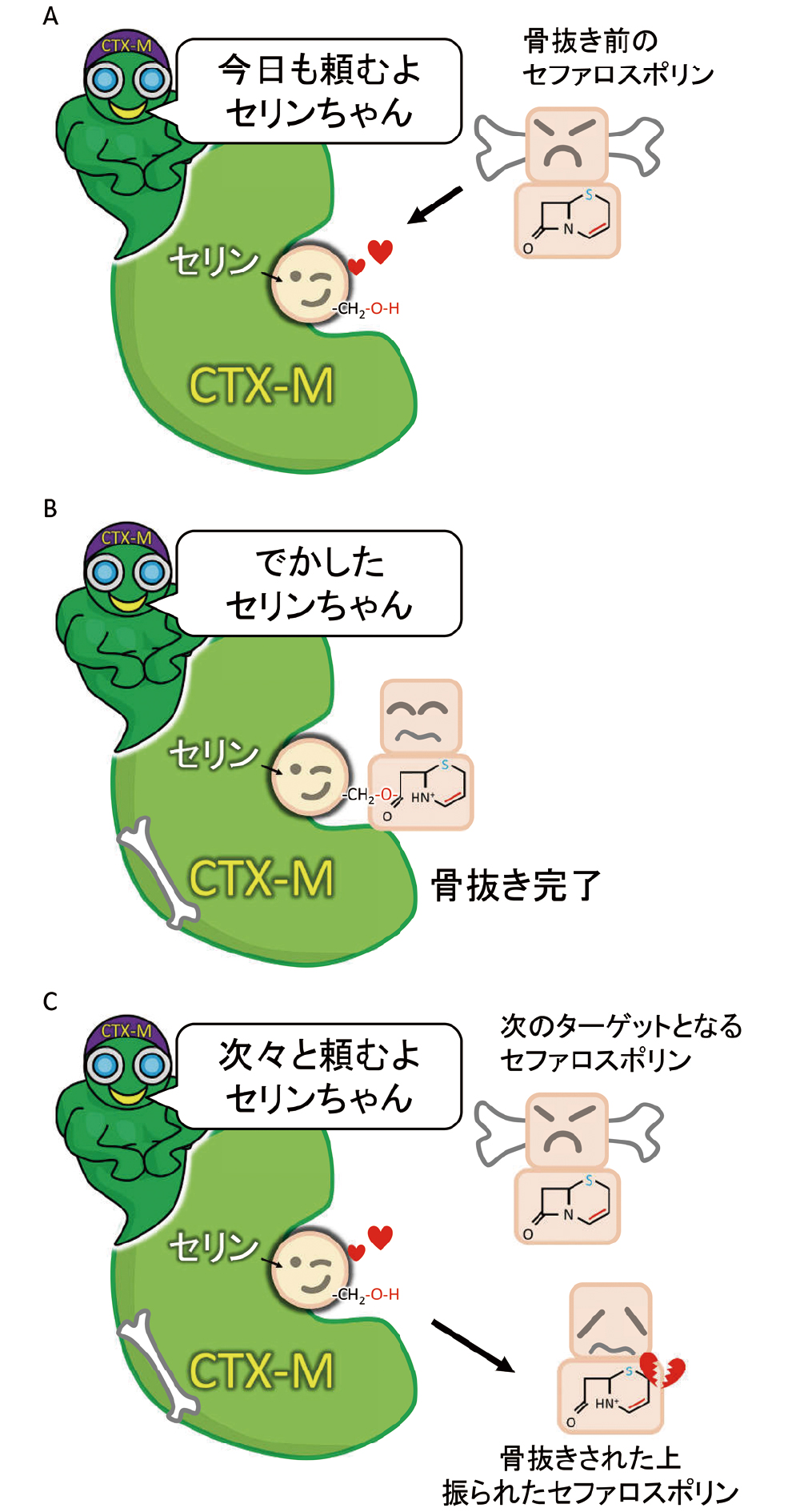
セファロスポリン系薬を骨抜きにする
A CTX-Mの活性中心にあるセリンがセファロスポリン系薬を魅了し、惹きつけます。B セリンの水酸基とβ-ラクタム環が結合し、骨抜き(β-ラクタム環が切断、開環)になります。C 骨抜きになってしまったセファロスポリン系薬は、用済みとなり、放り出されます。セリンの目は、すでに、次のセファロスポリン系薬に向かっています。
ところが、CTX-Mの活性中心にあるセリンは、セファロスポリン系薬よりも、β-ラクタマーゼ阻害薬が大好きです。β-ラクタマーゼ阻害薬も骨抜きになりますが、セファロスポリン系薬のときと異なり、セリンはβ-ラクタマーゼ阻害薬を放り出すことができません。β-ラクタマーゼ阻害薬がセリンと結合したままなので、セファロスポリン系薬は難を逃れます。そして、セファロスポリン系薬は本来のターゲットであるPBPの活性中心にあるセリンに近づき、一生結ばれます(図19)。
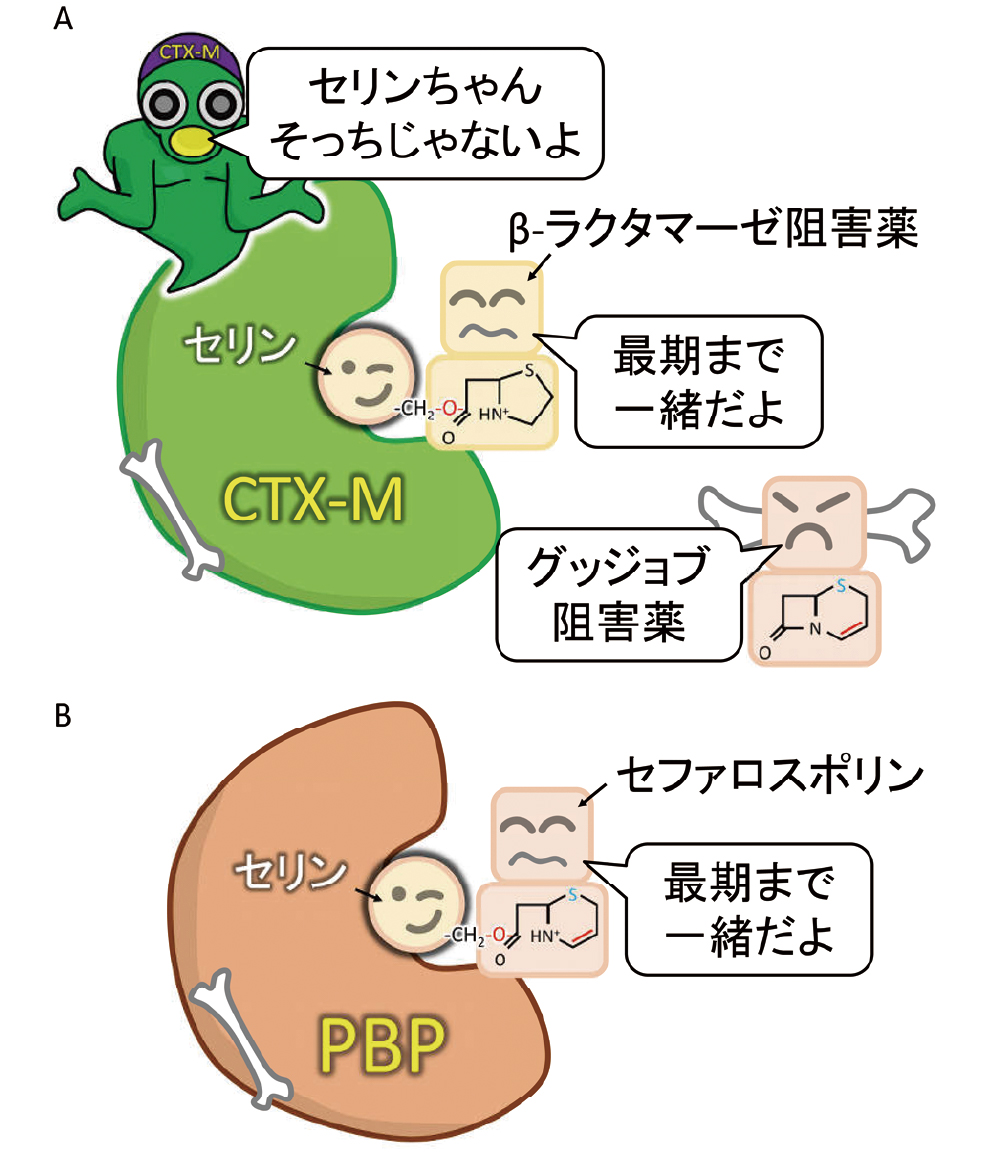
A CTX-Mの活性中心にあるセリンは、β-ラクタマーゼ阻害薬と結合し離れません。したがって、セファロスポリン系薬は難を逃れます。B 難を逃れたセファロスポリン系薬は、PBPの活性中心にあるセリンに近づき、本来の役割を果たすことができます。
このように、ESBL産生菌に対しては、β-ラクタマーゼ阻害薬配合のβ-ラクタム系薬も有効性が期待できます。ESBL産生菌に対して、カルバペネム系薬がしばしば使われますが、以下のような選択肢も考えられます。ただし、臨床的にはカルバペネム系薬の方が確実で、組織移行性や重症度を加味して選択することになります。
- □ タゾバクタム/ピペラシリン(TAZ/PIPC)
- □ タゾバクタム/セフトロザン(TAZ/CTLZ)
- □ セフメタゾール(CMZ)
■CTX-M-9Gはお手頃価格で増えていく
β-ラクタマーゼは、1アミノ酸違いでも亜型に分かれるため、CTX-Mは250以上の亜型が知られていますが、ある程度一括りに編成することができます。そのような大きな一括りをグループやサブファミリーと呼んでいます。例えば、CTX-M-9-likeという表記はサブファミリーの名称で、その一括りをグループとしてCTX-M-9Gと呼んだりします。CTX-Mの場合には、1G、2G、8G、9Gの4つのグループに分けることができます(表6)*。
中でも、近年増加しているのが、9Gです。
 *25Gを8Gとは別にして5つに分類することもあります。
*25Gを8Gとは別にして5つに分類することもあります。
ESBLはプラスミド伝達性で、同種もしくは近縁種間での受け渡しが可能です。耐性遺伝子は、当然ながら、抗菌薬存在下では、保有している方が保有していない場合に比べて有利です(図20)。しかし、プラスミドを持つにはそれなりの維持費がかかりますので、なくても何不自由なく暮らしている大腸菌にとって、プラスミドは不要です。むしろ維持費がかかる分、どちらかというと邪魔な存在です(図21)。微生物が環境などに適応するために必要な経費をフィットネスコストとも呼びますが、プラスミドを持つことは通常フィットネスコストが高く、不要になった場合、生存にとって不利に働きます。そのため、選択圧がない環境では、プラスミドを持たない大腸菌の方が増えやすくなり、徐々にプラスミドを持つ大腸菌の割合は減少するはずです。ところが、特定の大腸菌と特定の耐性遺伝子は相性が良いことが知られており、ST131という遺伝子型とCTX-M-9Gの組み合わせでは、フィットネスコストが低く抑えられています。つまり、ST131はCTX-M-9Gをお手頃価格で入手し、維持することができるということになります(図22)。MLSTのST131という遺伝子型の大腸菌では、70%がCTX-M-9Gを保有していることが報告されています。中でも、fimH30という線毛をもつST131は、CTX-M-27との相性が良いと言われています。しかも、キノロン耐性に関与する遺伝子に変異があり、キノロン耐性も多く含まれます(図23)。
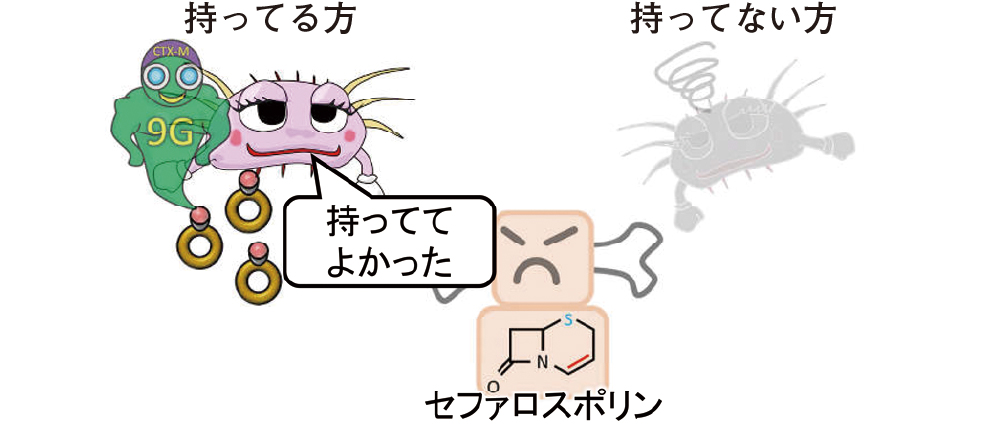
ESBLを持っていない大腸菌は、セファロスポリン系薬によって死滅させられます。一方、ESBLを持っている大腸菌は、セファロスポリン系薬による攻撃に耐え、生き残ることができます。
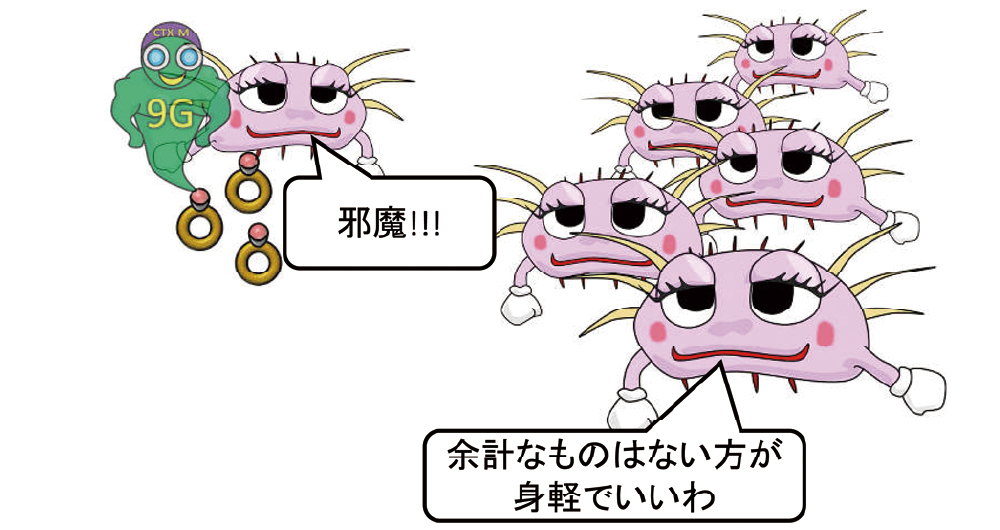
プラスミドの保有には維持費がかかります。なくても何不自由なく暮らしている大腸菌にとって、プラスミドは邪魔な存在です。そのため、プラスミドを持たず、身軽な大腸菌の方が増殖しやすくなります。
大腸菌の遺伝子型ST131とESBLの耐性因子CTX-M-9Gの組み合わせは、フィットネスコストが低く、お手頃価格でやり取りできるため、ST131の間で流行しています。
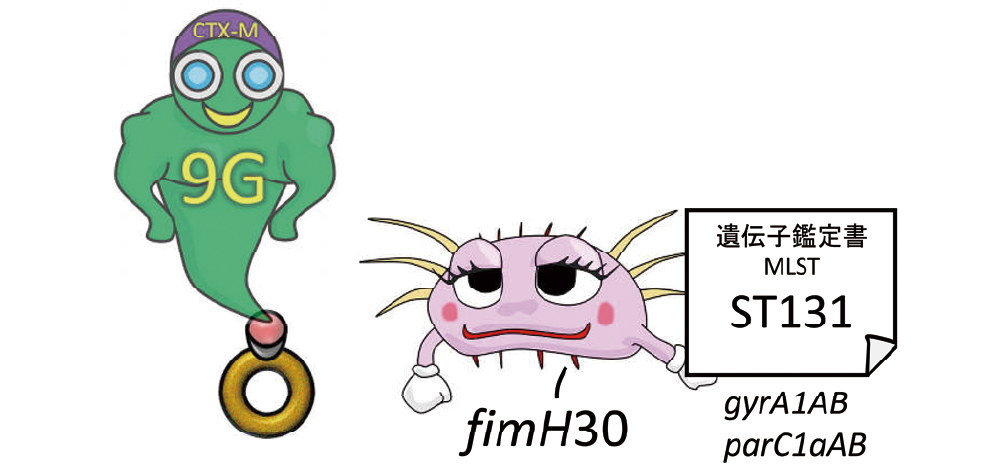
ST131の中でも、fimH30という線毛をもつ大腸菌は、CTX-M-9Gの一つであるCTX-M-27との相性が良いと言われています。しかも、キノロン耐性が多く含まれます。
fimH30:線毛の種類
gyrA1AB、parC1aAB:キノロン耐性に関連する遺伝子の変異
■耐性の腸内細菌目細菌の動向と課題
耐性の腸内細菌目細菌の動向を図24に示します。CREは低いところでほぼ横ばいですが、キノロン耐性、第三世代セファロスポリン耐性は年々増加傾向にあることが分かります。厳密にESBLを全ての株で調査しているわけではありませんが、第三世代セファロスポリン耐性のほとんどはESBL産生菌であると考えられます。腸内細菌目細菌は、名前の通りに腸内に定着し、増殖しやすいことから、ESBL産生菌も一旦定着すると排除されにくい可能性が考えられます。また、グラム陽性の黄色ブドウ球菌同様、腸内細菌目細菌も庶民系のため質素で栄養がない環境中でもたくましく生存することができます。このような特徴が、院内での伝播に関係していると考えられます。先の説明のように、抗菌薬による選択圧がなくても、耐性遺伝子を保有しやすくなっていることが、ESBL産生菌が増加しやすい理由の一つかもしれません。
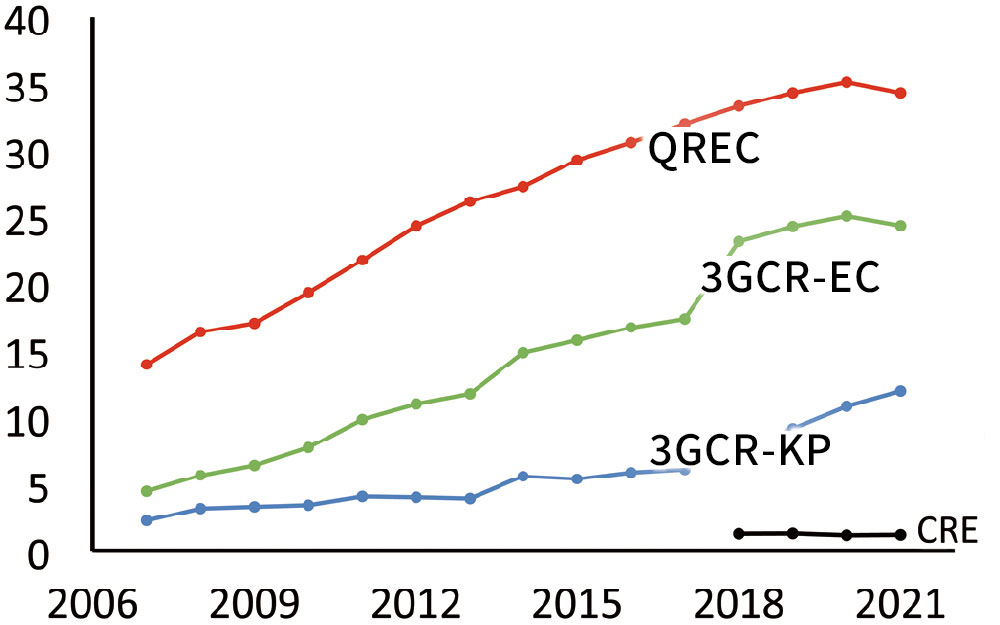
COVID-19の影響か、2021年は一部低下傾向にありますが、キノロン耐性、第三世代セファロスポリン耐性は年々増加傾向にあります。第三世代セファロスポリン耐性のほとんどがESBL産生菌であると考えられます。
QREC:キノロン耐性大腸菌
3GCR-EC:第三世代セファロスポリン大腸菌
3GCR-KP:第三世代セファロスポリン肺炎桿菌
CRE:カルバペネム耐性腸内細菌目細菌
薬剤耐性菌全般に関して、今後の動向が気になるところですが、最近の話題として、COVID-19の他の感染症への影響が報告されています。日本人はマスクの着用にあまり抵抗がなく、また、多くの方が医療現場でなくともこまめな手指のアルコール消毒を継続されているようです。そのため、飛沫や接触で感染するインフルエンザが減少したことは実感されていると思います。もちろん、インフルエンザの流行がそれだけで説明できるわけではありませんが、薬剤耐性菌の動向にも変化があり、COVID-19が影響しているようです。ただし、その影響は正も負もあります。例えば、MRSAやペニシリン耐性肺炎球菌(penicillinresistantStreptococcus pneumoniae,PRSP)は減っている一方、増加している耐性菌もあります。JANISのデータによると、COVID-19の影響か、2021年のキノロン耐性大腸菌や第三世代セファロスポリン耐性大腸菌は減少に転じましたが、これは見かけだけの可能性があります。なぜなら、検査数自体が減っていて適切に検出できていない可能性もあるためです。一方、第三世代セファロスポリン耐性肺炎桿菌は明らかに増加し続けています(図25)。同じ腸内細菌目であっても、その動向はやや異なるようです。このことは、増加の原因が、大腸菌と肺炎桿菌とで異なる可能性を示しているのかもしれません。抗菌薬の使用量や感染対策など、様々な要因が考えられますが、正確な理由はよくわかっていません。いずれにしても、今後も動向には注意が必要でしょう。
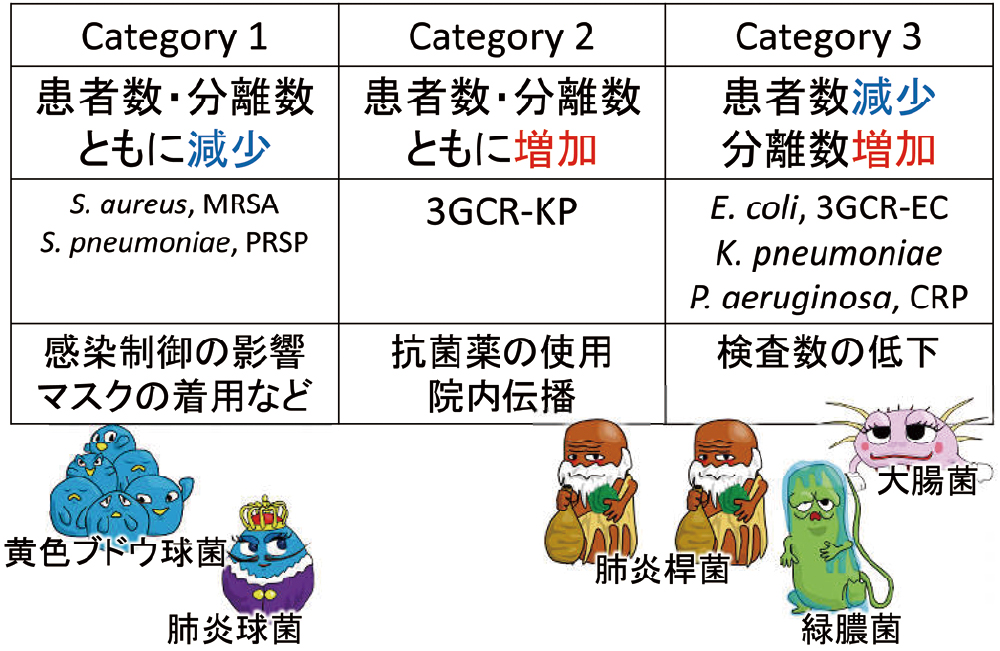
理由が解明されたわけではありませんが、COVID-19が薬剤耐性菌に正にも負にも影響しているようです。感染対策の徹底やマスクの着用が功を奏したのか、MRSAやPRSPは減っている一方、第三世代セファロスポリン耐性の大腸菌や肺炎桿菌は増加しています。
PRSP:ペニシリン耐性肺炎球菌
3GCR-KP:第三世代セファロスポリン耐性肺炎桿菌
3GCR-EC:第三世代セファロスポリン耐性大腸菌
CRPA:カルバペネム耐性緑膿菌


