黄色ブドウ球菌(Staphylococcus aureus)
■細菌学的特徴
最初に、細菌学的な特徴を理解するために、グラム陽性球菌の臨床検査上の分類を家系図風に説明したいと思います。まず、グラム陽性球菌一派は、ブドウ球菌系(cluster)とレンサ球菌系(chain)に分かれます。ブドウ球菌系とレンサ球菌系は、形状のみならず、カタラーゼという酵素でも分類することができます。団子のように固まって「みんなで語ろうぜ」ということで、カタラーゼを持っている方がブドウ球菌系、持っていない方がレンサ球菌系です(図1)。カタラーゼは、菌にとって有害な活性酸素の1つである過酸化水素(H2O2)を、水(H2O)と酸素(O2)に分解して無毒化する酵素です。爪楊枝の先に菌をとり、過酸化水素水につけて確かめます。ブドウ球菌の場合には、酸素の泡が出てきます。カタラーゼだけに「ブツブツ」と語っているようですね。
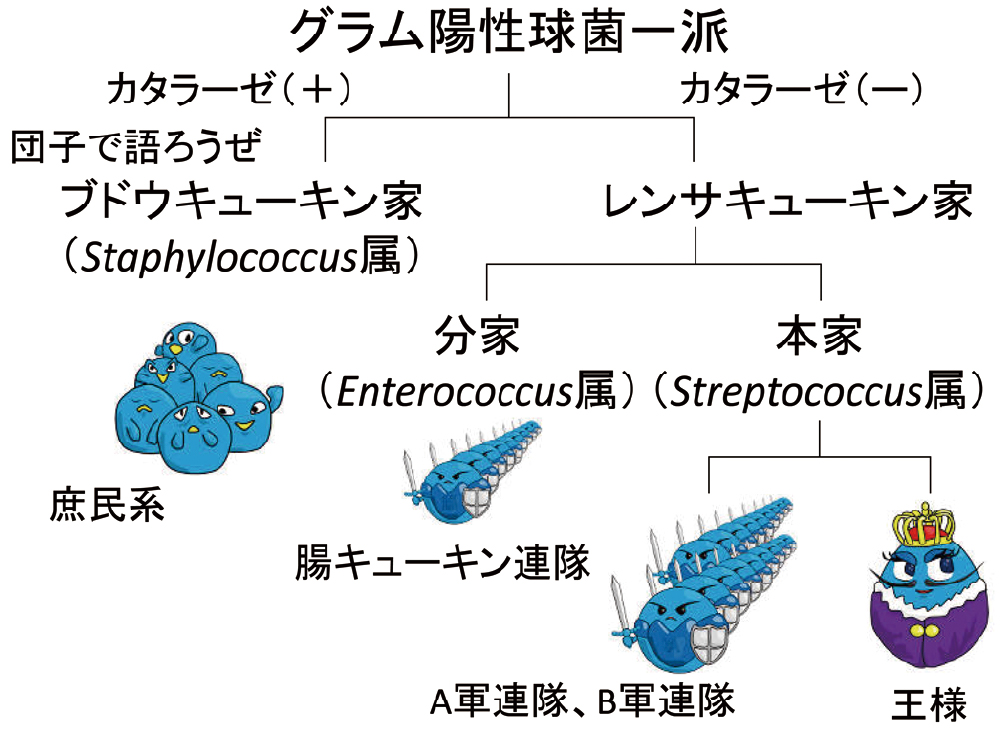
ブドウ球菌は形状のみではなく、カタラーゼを持つことでも判別できます。
ブドウ球菌の属名(Staphylococcus)は、「ブドウの房状の」という意味の“staphylo-”と「球菌」を意味する“-coccus”を合成したものです。また、黄色ブドウ球菌の種名の“aureus”は「黄金」という意味で、金の元素記号Auと同じ語源です。なお、レンサ球菌系は、本家(Streptococcus属)と分家(Enterococcus属)に分かれ、本家はさらに、王様である肺炎球菌(Streptococcus pneumoniae)と、A軍、B軍などの連隊である溶血性レンサ球菌(A群はStreptococcus pyogenes、B群はStreptococcus agalactiae)などに分かれます。
ブドウ球菌属は、一般に肺炎球菌などと比べて栄養要求性の低い細菌が多く、乾燥にも強いので、環境中でも比較的長期に生存可能です。手指を介して接触感染で広がりやすく、しばしば院内感染などの原因になる細菌の代表格です。特に耐性菌として、後ほどご紹介するメチシリン耐性黄色ブドウ球菌(MRSA)は病院で働いていれば、ほぼ必ず遭遇する重要な細菌です。
■ブドウ球菌の分類
ブドウ球菌は、コアグラーゼの有無によって分類され、コアグラーゼ陽性のブドウ球菌は、ほぼ黄色ブドウ球菌と同義です。一方、コアグラーゼ陰性のブドウ球菌は、文字通り、coagulase negativeStaphylococcusと呼び、しばしばCNSと略します。CNSは、コンビでたとえると、「じゃない方」ということになりますが、複数の菌種を含んでおり、その代表格が表皮ブドウ球菌(S. epidermidis)です(図2)。
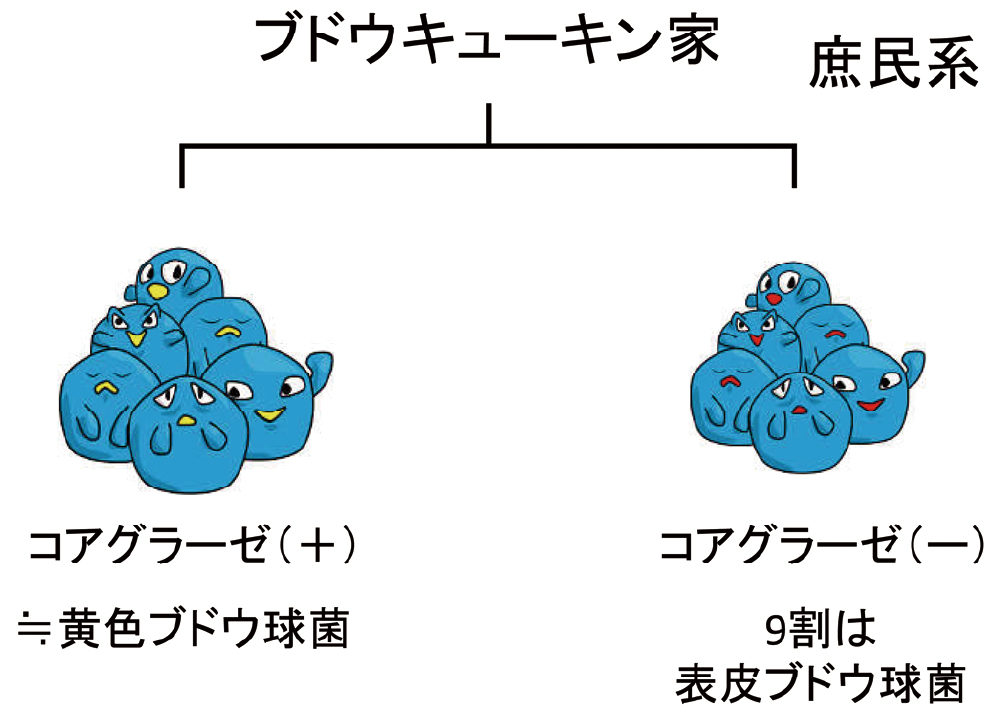
コアグラーゼ陽性はほぼ黄色ブドウ球菌と同義です。コアグラーゼ陰性のブドウ球菌はCNSと呼ばれ、その9割は表皮ブドウ球菌です。
コアグラーゼは血漿を凝固(coagulation)させる病原因子で、試験管内で菌液と血漿を混合したあと、試験管を横にしても流れなければ、コアグラーゼ陽性と判断します(図3)。コアグラーゼを持っていると、より団結力が強化され、菌の塊がさらに大きな塊になり、毛細血管に引っかかりやすいため、膿瘍形成などを促進します。黄色ブドウ球菌の方がCNSよりも病原性が高い理由の一つであり、血液などから分離されたときの臨床的意義も高くなります。
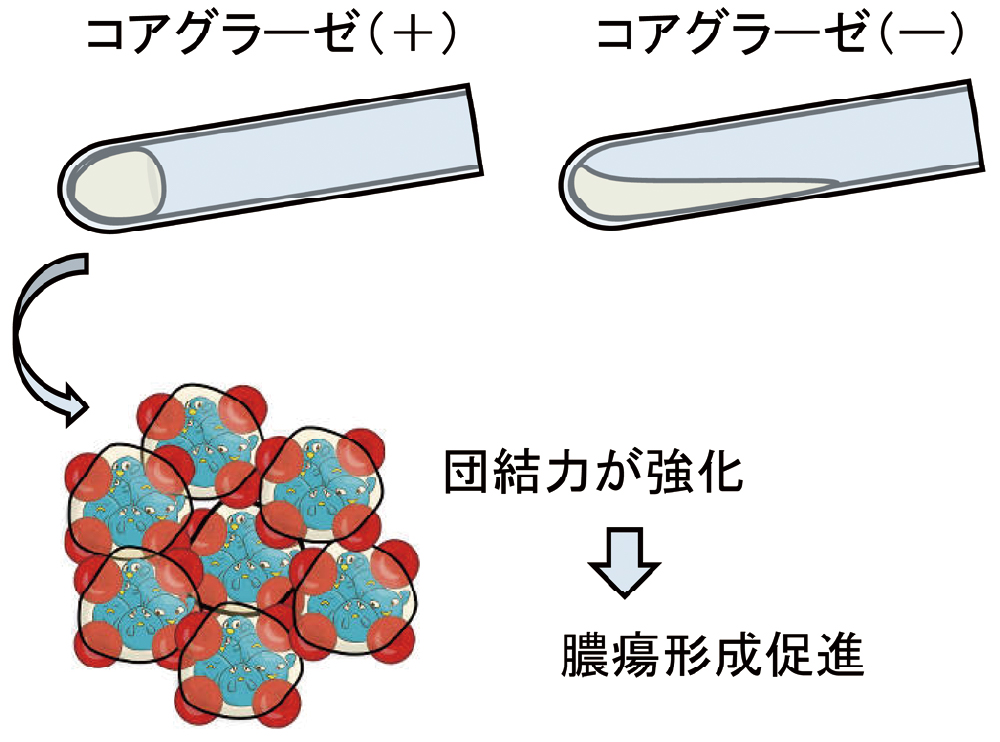
ウサギの血漿に菌液を加えます。コアグラーゼがあれば、血漿が固まり、横にしても流れません(左)。コアグラーゼがないと、血漿が固まらないのでさらっと流れます(右)。コアグラーゼを持っていると、団結力が強化され、より大きな塊を作りやすくなり、膿瘍形成などを促進します。
■臨床的な特徴
ブドウ球菌属の多くは、皮膚や鼻腔等、体の表面に常在しています。この点は、同じ庶民系でも、腸内に常在することが多い大腸菌などとは異なる点です。病気の成り立ちとも関連する特徴です。例えば、黄色ブドウ球菌による食中毒は、お手製のおにぎりなどが原因となります。素手でおにぎりを握るのは、手の表面にいる黄色ブドウ球菌をおにぎりにくっつけることを意味します。黄色ブドウ球菌に食事を与えているようなものなので、おにぎりの表面ですくすくと増えていきます。黄色ブドウ球菌の場合、食塩耐性(10%NaCLでも生存)なので、人が食べられないほどの塩辛さでもへっちゃらです。菌は熱に弱いので、電子レンジなどで加熱すれば死滅しますが、黄色ブドウ球菌が産生するエンテロトキシンという毒素は、100℃でも失活しませんので、しばらく放置してエンテロトキシンに汚染された食物は、加熱しても食中毒を起こします。
皇族系の肺炎球菌やインフルエンザ菌は、尿や便からは分離されませんが、黄色ブドウ球菌は感染部位を選びません。あらゆる部位の感染症を起こします。ただし、皮膚に常在しているため、皮膚軟部組織の感染症は起こりやすい感染症の一つです。とびひのような比較的軽症のものから、蜂窩織炎、壊死性筋膜炎などの重症の感染症まであります。特に、トキシックショック症候群毒素-1(toxic shock syndrome toxin 1,TSST-1)という毒素を持っている場合には、トキシックショック症候群(toxic shock syndrome, TSS)という劇症型の感染症を起こすことがあります。
血液からの分離は、大腸菌に次いで多く、カテーテルなどの医療用デバイスの使用によって起こる血流感染症が典型的です。そのほか、肺炎(特に肺化膿症)、腹膜炎、髄膜炎、腸炎、前立腺炎などを起こすので、これらの感染症では原因菌として想起すべき細菌の一つです。
■治療
日本ではメチシリンが使用できないため、メチシリン感受性黄色ブドウ球菌(methicillin-susceptibleStaphylococcus aureus, MSSA)に対してはセファゾリンなどの第一世代セファロスポリンが使用されます。一方、MRSAに対しては、2023年現在、4系統、6種類の抗菌薬があり、抗MRSA薬という括りで分類されます。特定抗菌薬の一種です。バンコマイシン、テイコプラニン、アルベカシン、リネゾリド、テジゾリド、ダプトマイシンがあります。6つもあって覚えにくいと思いますので、覚え方をご紹介します。「マルシェ(MRSA)には、リゾット(リネゾリド)あるのが(アルベカシン)定番(テイコプラニン・バンコマイシン)だって(ダプトマイシン・テジゾリド)」。いかがでしょうか(図4)。

抗菌薬をすべて覚えるのは大変ですが、抗MRSA薬は重要なので、語呂で身につけましょう。
メチシリン耐性黄色ブドウ球菌(methicillin-resistantStaphylococcus aureus, MRSA)
■MRSAは青の横綱
代表的な薬剤耐性菌の番付をご覧ください。私の独断と偏見により、代表的な耐性菌を幕内力士に見立ててみました。東・西の代わりに、青・赤に分けました。むろん、グラム染色の分類で、青は陽性、赤は陰性を表しています。MRSAは、青の横綱に位置付けました(図5)。ガイドラインや総説なども多く、グラム陽性菌の中で最も有名な耐性菌であるというのが主な理由です。厚生労働省院内感染対策サーベイランス事業(JANIS)の調査でも、2022年薬剤耐性菌による新規感染症発症患者15,595人中、MRSAは14,790人(94.84%)と、他を圧倒しています。また、同年のデータでは、JANISに参加する200床以上の医療機関1386施設中、MRSAが分離されなかった医療機関はなく、「MRSAに遭遇しない方が稀」というほどです。これほど日本ではお馴染みの薬剤耐性菌ですので、よくご存知かもしれませんが、MRSAとはどんな耐性菌なのか、今一度、一緒に考えてみたいと思います。

グラム陽性菌を青、グラム陰性菌を赤として、代表的な耐性菌を青と赤の横綱と大関に位置付けてみました。
MRSA:メチシリン耐性黄色ブドウ球菌
VRE:バンコマイシン耐性腸球菌
CRE:カルバペネム耐性腸内細菌目細菌
CPE:カルバペネマーゼ産生腸内細菌目細菌
■MRSAは多剤耐性
methicillin-resistantStaphylococcus aureusの略で、文字通り、メチシリンに耐性を示す黄色ブドウ球菌です(図6)。しかしながら、MRSAはメチシリンに耐性であるのみならず、多剤に耐性を示します。後述しますが、メチシリン耐性は、ペニシリン結合蛋白質(penicillin binding protein, PBP)の変異によるものです*。肺炎球菌やインフルエンザ菌でも、PBPの変異によるペニシリン耐性が知られていますが、ペニシリン系薬以外のβ-ラクタム系薬(セファロスポリン系薬やカルバペネム系薬)には感受性を示すのが一般的です。しかしながら、MRSAの場合には、β-ラクタム系薬全般に耐性を示します。また、一部の例外を除き、キノロン系薬など、β-ラクタム系薬以外の抗菌薬にも耐性を示します。MRSAの「M」は、multidrugの「M」であると勘違いされることもあるほどです。メチシリン耐性の本体は、mecAという遺伝子によるものですが、MRSAの多くは、mecAを含む複数の耐性遺伝子をセットで獲得するために多系統に耐性となります。おそらく、MRSAがメチシリンに耐性を示すだけであれば、ここまで厄介な耐性菌にはならなかったと思います。なお、黄色ブドウ球菌が持つ遺伝子セット(遺伝子領域)を、Staphylococcal cassette chromosome(SCC)と呼び、メチシリン耐性遺伝子を含む領域は、SCCmecと呼ばれます。SCCmecは、MRSAの型別にも応用されるほど重要なキーワードです。
*厳密には、PBPの変異ではなく、ペニシリン低親和性PBPであるPBP2'(=PBP2a)の獲得によるもの。
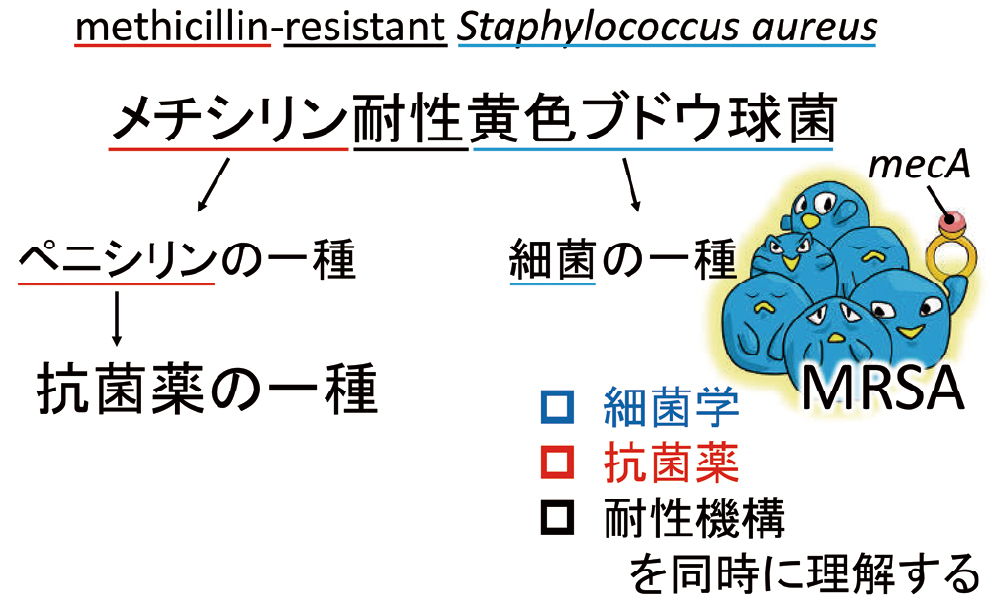
MRSAは、メチシリン耐性黄色ブドウ球菌の略です。日本で最も有名な耐性菌であり、臨床的に重要であることはもちろん、細菌学、抗菌薬、耐性機構を理解するのにうってつけの題材でもあります。
■MRSAの出現
MRSAは、日本で最も多い耐性菌として、臨床的に重要であるばかりではなく、細菌学、抗菌薬、耐性機構を同時に学ぶ題材としても最適です(図6)。私の中では、元祖耐性菌のイメージです(表1)。

では、メチシリンとはなんでしょう。語尾に-cillinがつくことからわかる通り、ペニシリンの一種です。黄色ブドウ球菌は元々ペニシリン感受性でしたが、ペニシリンが本格的に使用されるようになった数年後には、ペニシリン耐性菌が出現しました。最初に出現したペニシリン耐性は、PC1というペニシリナーゼ(ペニシリン分解酵素)によるものでした(図7)。元祖ペニシリンの1つであるペニシリンGは、PC1によって分解、不活化されることで、抗菌薬としての機能を失います。そこで、ペニシリナーゼで分解されないよう、従来型のペニシリンを改良し、特殊加工を施した「メチシリン」を開発しました(図8)。ペニシリナーゼ耐性ペニシリンとも呼ばれます。なお、日本では、メチシリンは市販されなかったため、メチシリンの代わりに、第一世代セファロスポリン系薬のセファゾリンが使用されます。
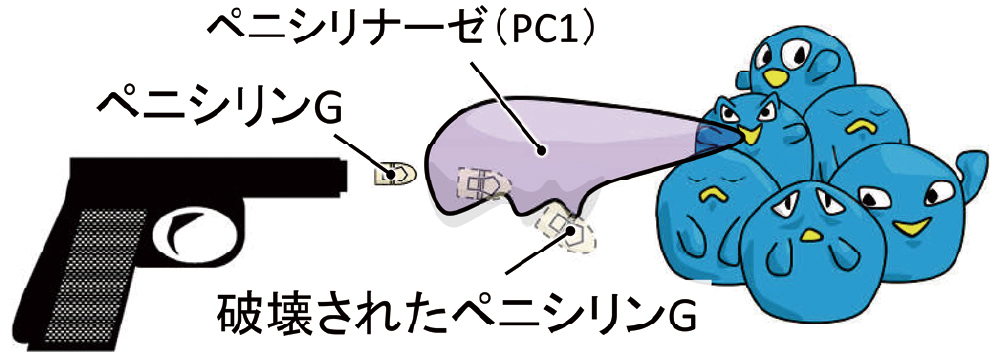
ペニシリンGを破壊
最初は黄色ブドウ球菌にもペニシリンGが効いていましたが、ペニシリンが使用されて間もなく、PC1というペニシリナーゼ(ペニシリン分解酵素)をゲットし、ペニシリンが効かなくなりました。
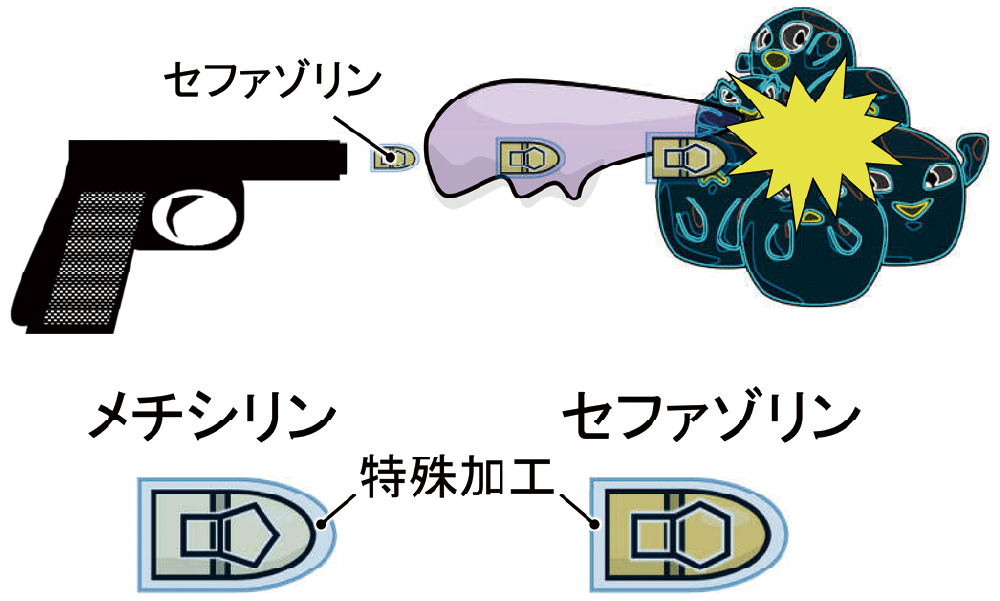
メチシリンやセファゾリンを開発
ペニシリナーゼで破壊されないよう特殊加工されたペニシリナーゼ耐性のペニシリンがメチシリンです。ただし、メチシリンは、日本では使えないため、メチシリンの代わりに、第一世代セファロスポリン系薬のセファゾリンを使っています。
*特殊加工の表現は、分かりやすくイメージしたもので、実際の加工とは異なります。
ところが、メチシリンが使用されるようになると、今度は、mecAというメチシリンに対する耐性遺伝子を手に入れた黄色ブドウ球菌が現れました(図9)。ついにMRSAの出現です。mecAは、ペニシリン低親和性PBPであるPBP2'(=PBP2a)をコードする遺伝子で、先述のペニシリン耐性機構であるペニシリナーゼとは全く異なる機序による耐性遺伝子です。
さて、MRSAのおおよそのイメージがついたところで、β-ラクタム系薬の作用機序も含めて、もう少し詳細な分子機構に迫りたいと思います。
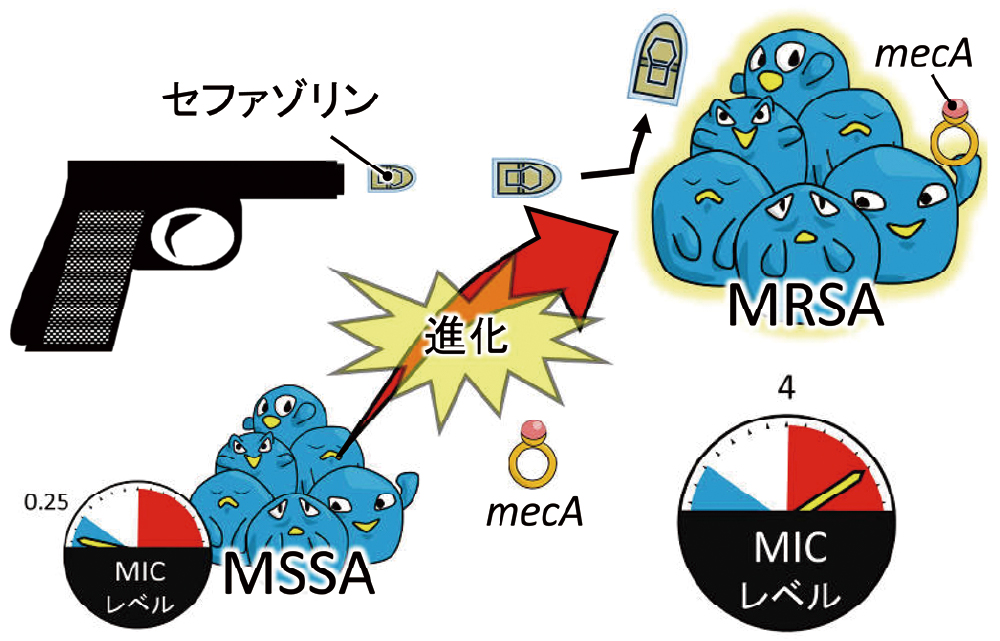
mecAという新たなアイテムをゲットして、メチシリンやセファゾリンさえ効かなくなったのがMRSAです。
■β-ラクタム系薬は、細菌を自爆させる抗菌薬
黄色ブドウ球菌は、グラム陽性菌ですので外膜がなく、細胞膜の外側に分厚い細胞壁を持っています(図10)。細胞膜は、脂質でできており、シャボン玉の膜程度の貧弱な構造です。一方、細胞壁は、デニム生地のように丈夫な構造をしています。特に、黄色ブドウ球菌の場合、細胞内圧が10気圧にもなると言われており、このような高圧に耐えうるのは分厚い細胞壁のお陰です。言い換えると、細胞壁がなくなれば、自身の内圧によって容易に破裂します。ペニシリンが発見された当初は、作用機序が分かっていませんでしたが、β-ラクタム系薬は、細胞壁の合成を阻害することで細菌を自爆に追い込むという、理にかなった抗菌薬であることが分かります。
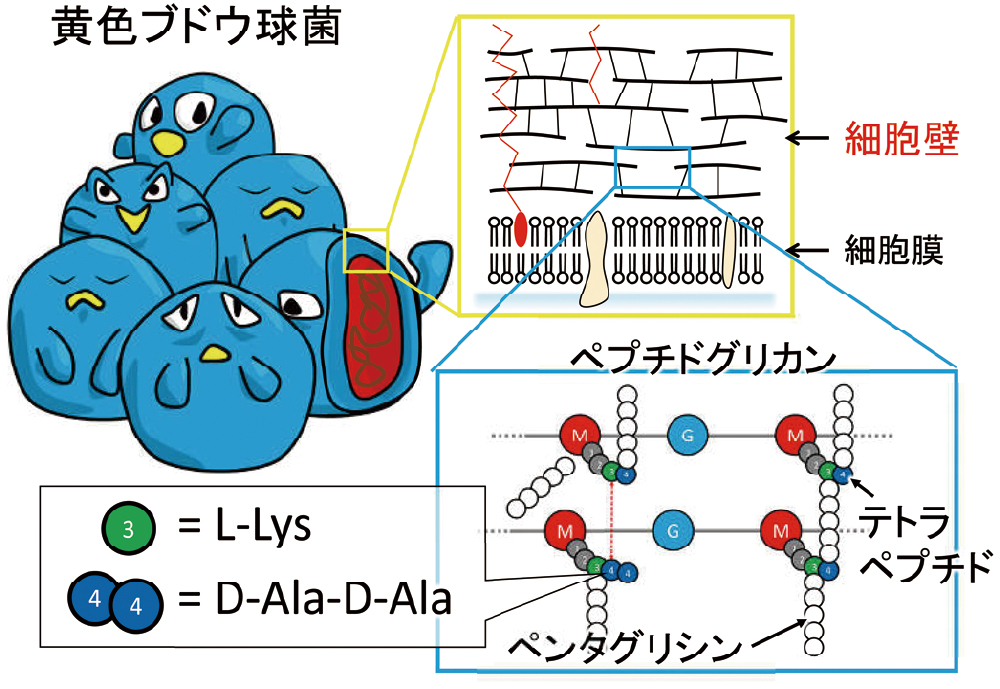
細胞壁は黄色ブドウ球菌の10気圧という細胞内圧に耐えうるために、強靭な網目構造となっています。横糸、縦糸に例えると、横糸はGとMの繰り返し構造となっています。Mから4種類(L-Ala、γ-D-Gln、L-Lys、D-Ala)のアミノ酸残基からなるテトラペプチドが側鎖として出ており、1つの横糸にあるL-Lysと別の横糸にあるD-Alaの間に、ペンタグリシンという縦糸が入ります。縦糸が入る前は、テトラペプチドの先端にもう一つD-Alaがついていますが、この末端のD-Alaが取り除かれることで、テトラペプチドになり、ペンタグリシンによる橋渡し(架橋)が可能になります。
1:L-Ala(L-アラニン)
2:γ-D-Gln(γ-D-グルタミン)
3:L-Lys(L-リシン)
4:D-Ala(D-アラニン)
D-Ala-D-Ala:D-アラニル-D-アラニン
G:N-アセチルグルコサミン
M:N-アセチルムラミン酸
細胞壁の構造をさらにミクロで見てみましょう。ペプチドグリカンという、横糸と縦糸が組み合わさったような網目状の多糖でできています。N-アセチルグルコサミン(GlcNAc)とN-アセチルムラミン酸(MurNAc)をそれぞれGとMとし、その繰り返し構造を横糸で表しています。MurNAcからは、4種類(L-Ala、γ-D-Gln、L-Lys、D-Ala)のアミノ酸残基からなるテトラペプチドが側鎖として出ています。1つのテトラペプチド中のL-Lysと別のテトラペプチド末端のD-Alaとの間に、5つのグリシンからなるペンタグリシンが、縦糸として橋渡し(架橋)することで強靭な網目構造を形成しています。
*Ala=アラニン、Gln=グルタミン、Lys=リシン
■ペニシリンはPBPの活性中心に結合して、D-Ala-D-Alaの解離を邪魔する
PBPは、その名の通り、ペニシリンに結合する蛋白質として同定されました。ペニシリンだけではなく、β-ラクタム系薬の標的となっています。PBPという名称が、本来の機能を分かりにくくしていますが、PBPは細胞壁合成に関わる酵素の1つです。ペンタグリシンという縦糸が架橋する前は、テトラペプチドの先端にもう1つ余分にD-Alaがついており、D-Ala-D-Ala(D-アラニル-D-アラニン)という構造になっています。この末端のD-Alaが取り除かれることで、テトラペプチドになり、ペンタグリシンによる架橋が可能になります。この末端のD-Alaを取り除く酵素こそがPBPです。つまり、PBPがD-Ala-D-Alaを解離させることによって、L-LysとD-Alaの間にペンタグリシンの架橋ができるということです(図11)。
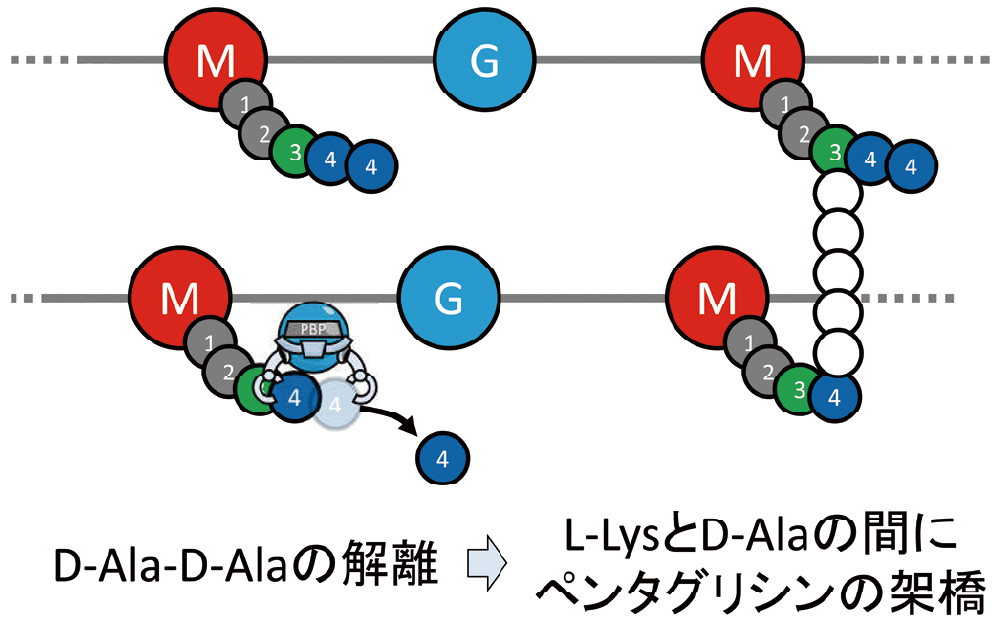
PBPが、D-Ala-D-Alaを解離させることで、末端のD-Alaがとれて、L-LysとD-Alaの間にペンタグリシンの架橋ができます。
PBPの活性中心には、セリン残基があり、セリン残基の側鎖(-CH2OH)とD-Ala-D-Alaとが反応することで、D-Ala-D-Alaの解離が起こります。ところが、ペニシリンとD-Ala-D-Alaは構造が類似しているために、活性中心の-CH2OHにペニシリンが結合します。-CH2OHとD-Ala-D-Alaの結合は可逆的で、反応するたびに、セリン残基は元に戻りますが、-CH2OHとペニシリンの結合は不可逆的です。ペニシリンは、すっぽんのごとくPBPの-CH2OHに食らいついて離れないということになります。このようにして、PBPによるD-Ala-D-Alaの解離を邪魔することで、結果的に細胞壁の合成を阻害します(図12)。
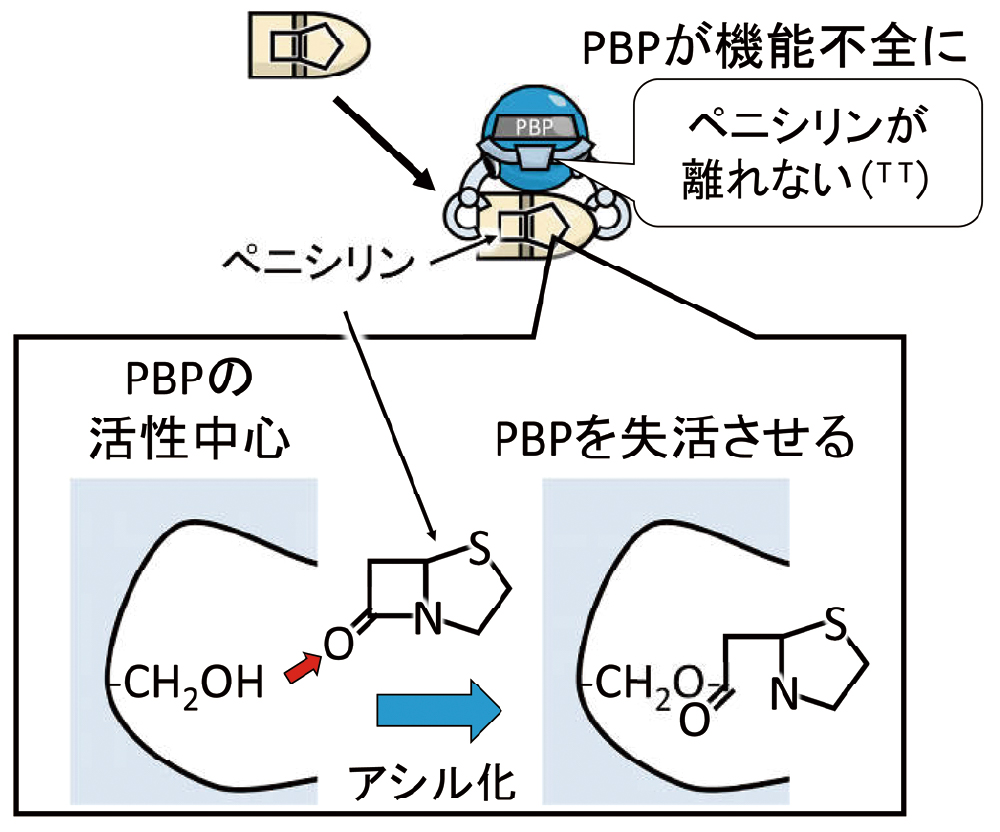
PBPの活性中心では、本来、D-Ala-D-Alaの解離が行われますが、ペニシリンがPBPの活性中心に結合(アシル化)するため、PBPが失活します。一度結合したペニシリンは、すっぽんのように結合し、離れません。
■お助けロボ「ペニシリナーゼ」VS刺客「メチシリン」
黄色ブドウ球菌は、ペニシリンに抵抗するために、お助けロボ「ペニシリナーゼPC1」を発動します。黄色ブドウ球菌が持つペニシリナーゼは、セリン型と呼ばれるβ-ラクタマーゼで、活性中心がPBPとよく似ています(図13)。PBPは、ペニシリンと結合すると離れませんが、PC1は、ペニシリンを「骨抜き」にしてから解放します(図13)。PC1は再利用できるため、ペニシリンを次から次へと破壊し続けることができるようになります。PC1のお陰で、ペニシリンという脅威がいなくなり、PBPは再び本来の働きを取り戻し、細胞壁の合成が可能になります(図13)。
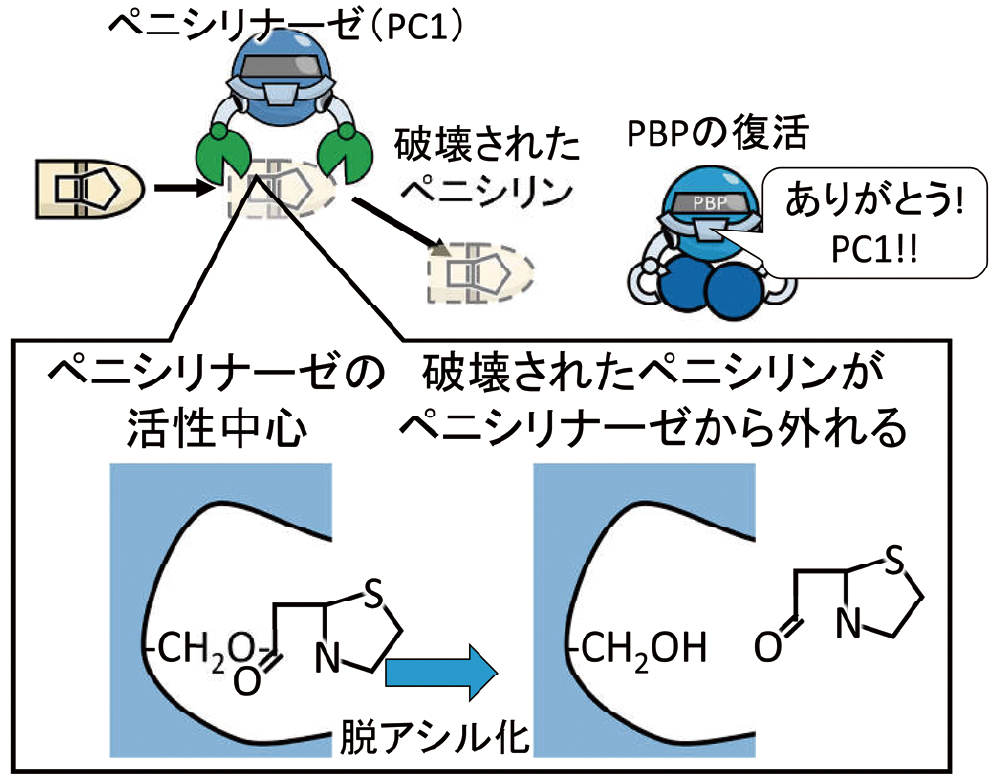
ペニシリナーゼの活性中心は、PBPに似ているので、PBPになりすまして、ペニシリンを破壊します。PBPの場合には、ペニシリンがくっついたままでしたが、ペニシリナーゼは、ペニシリンを「骨抜き」にした後、ペニシリンを解放します(脱アシル化)。そのため、ペニシリナーゼは、次々にペニシリンを破壊し続けることができ、そのおかげで、PBPは本来の機能を果たすことができます。
さて、そこに、刺客である「メチシリン」が送り込まれるとどうなるでしょう。特殊加工されているので、PC1では分解できません。黄色ブドウ球菌は、4種類のPBP(PBP1~4)を持っていますが、いずれにもメチシリンが結合し、やはり、細胞壁の合成が止まります(図14)。
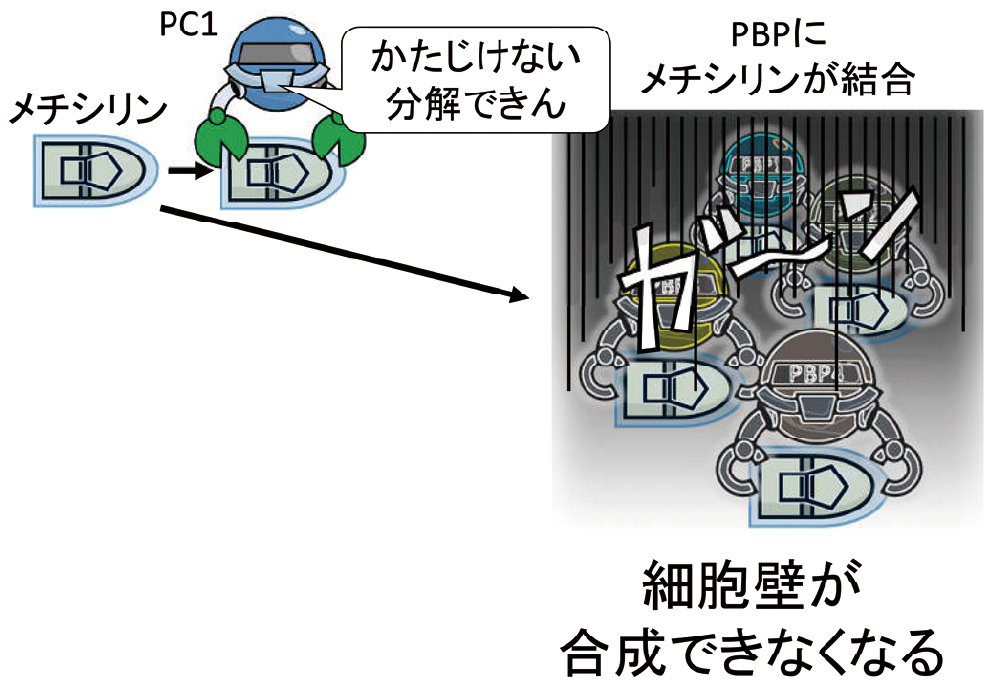
メチシリンは、ペニシリナーゼで分解できないように特殊加工されていますので、PC1では分解されません。黄色ブドウ球菌がもつ4種類のPBP(PBP1~4)には、メチシリンが結合し、細胞壁の合成ができなくなります。
ところが、mecAという遺伝子によって召喚されたお助けロボ「PBP2'」が登場します。
今回のお助けロボは、分解酵素ではありません。前述のようにペニシリン低親和性のPBPです。「ペニシリンが結合しにくいペニシリン結合蛋白質」という意味になりますから、わけがわからなくなりますが、D-Ala-D-Alaとの結合能力を残しつつも、メチシリンが結合しにくい無敵のPBPです。PBP2'は、ペニシリン系薬のみならず、全てのβ-ラクタム系薬と結合しにくくなっています。この状態の黄色ブドウ球菌が、MRSAです(図15)。
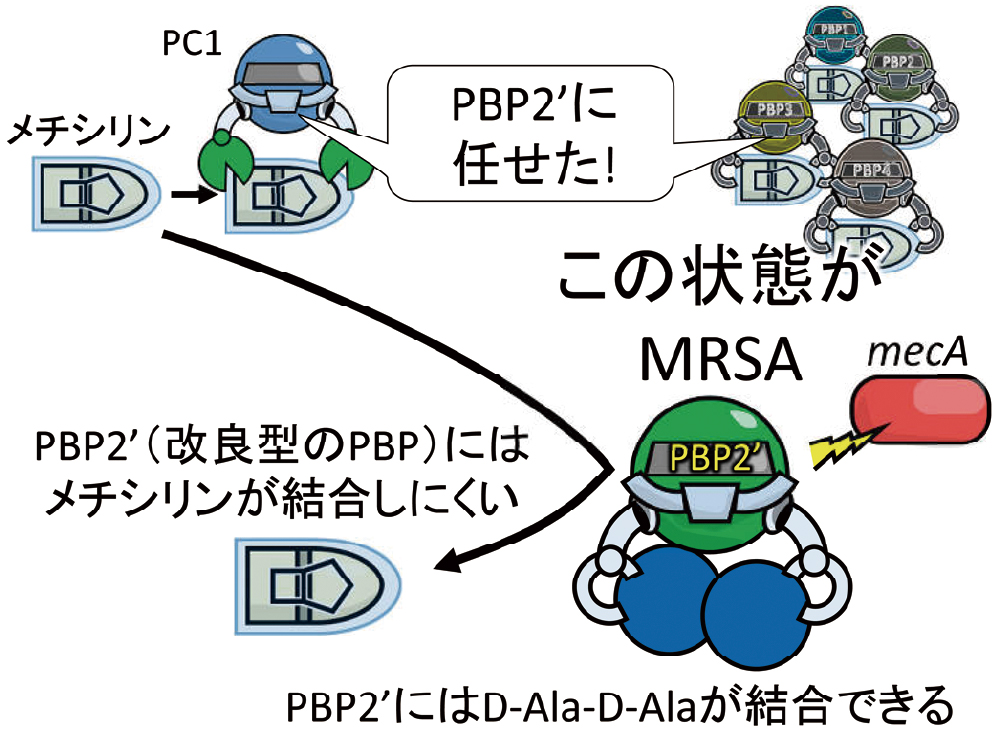
PBP2'は、獲得したmecA遺伝子にコードされた改良型のPBPで、D-Ala-D-Alaへの結合能力を残したまま、メチシリンには結合しません。そのため、再度、細胞壁の合成が可能になります。このPBP2'が発動した状態の黄色ブドウ球菌が、MRSAです。
抗MRSA薬
■抗MRSA薬の位置づけ
抗MRSA薬の開発も進み、2024年現在では6薬剤が使用できます(表2)。抗MRSA薬の説明に進む前に、抗微生物薬*全体のおさらいをしておきます。
抗菌薬は、抗微生物薬の一部であり、意味合いとしては、抗「細菌」薬です(図16)。抗MRSA薬は、もちろん抗菌薬ですが、少し特殊な位置づけになっており、広域抗菌薬と並ぶ特定抗菌薬の一つです。特定抗菌薬の明確な定義はありませんが、使用に際し注意が必要な特に定められた抗菌薬です。つまり、抗MRSA薬も使用に際して注意が必要であるということになり、原則としてMRSAによる感染症のみが適応となります。
*抗微生物薬の厳密な定義はありませんが、本稿では、抗ウイルス薬などまで含めた総称としています。
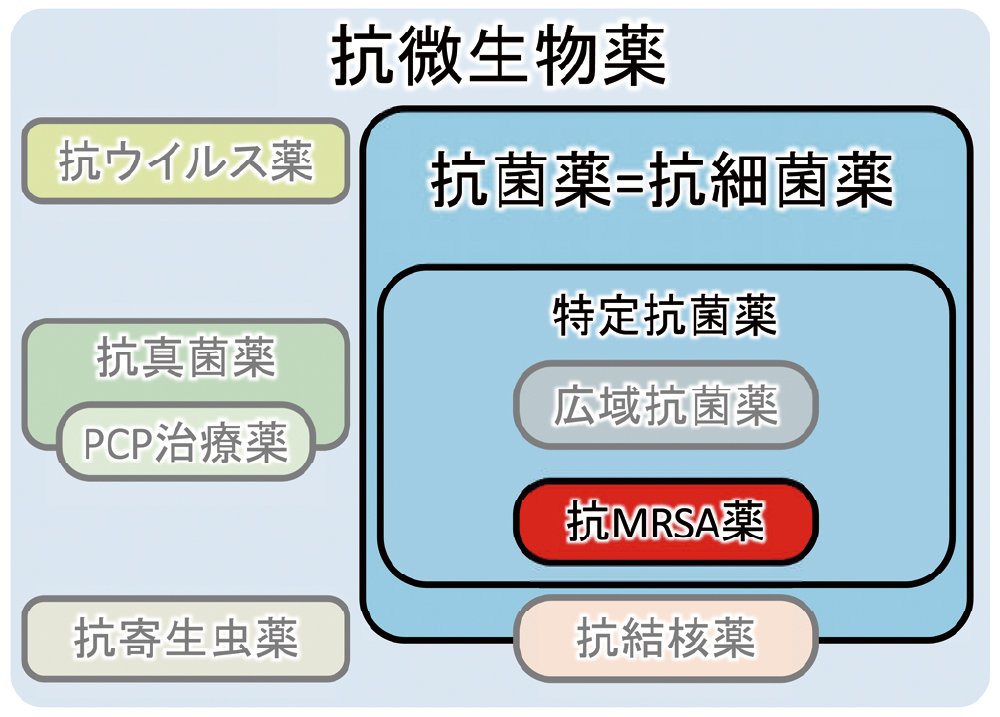
抗MRSA薬は、抗菌薬の中の特定抗菌薬の一部です。
それぞれの特徴も説明しておきます。なお、説明の中で、抗MRSA薬に関する専門用語(☆を付けています)が出てきて分かりづらいかもしれませんが、文の流れを途切れさせないために、それらの用語解説は別途用意しました。
■抗MRSA薬のポイント(表2)
□殺菌的☆か静菌的☆か:リネゾリドとテジゾリドは静菌的、その他は殺菌的です(図17)。□投与経路:リネゾリドとテジゾリドは内服が可能、その他は静注のみ。□TDM☆が必要か: グリコペプチド系薬(バンコマイシン、テイコプラニン)とアミノ グリコシド系薬(アルベカシン)はTDMが必要です。ともに、名称に「グリコ」がついて内耳毒性、腎毒性があることも共通しています。□その他:ダプトマイシンは肺感染症に使用できません。
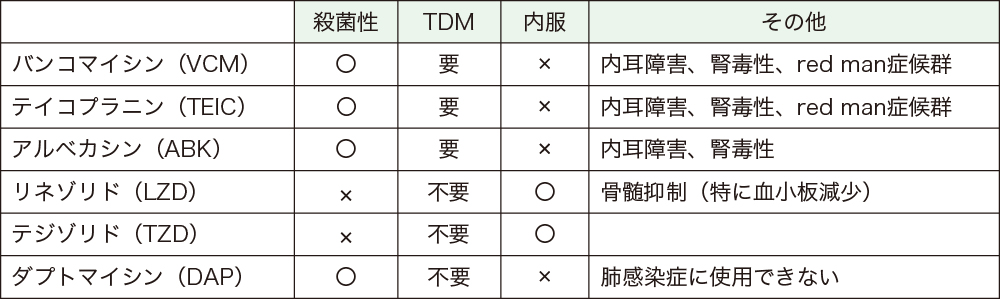
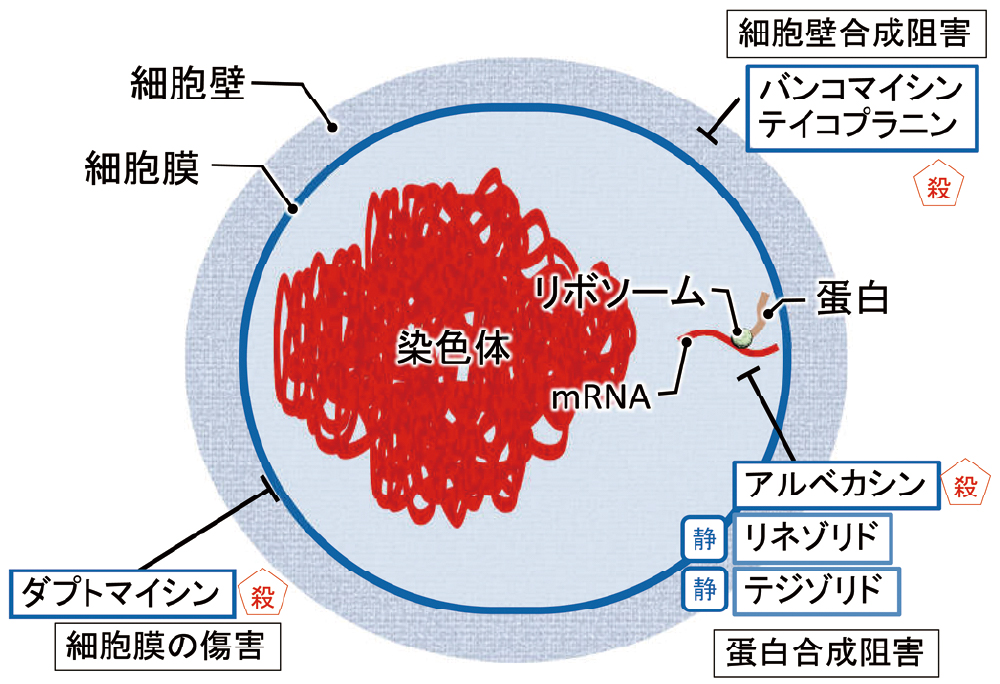
バンコマイシンとテイコプラニンは細胞壁合成阻害、ダプトマイシンは細胞膜の傷害、それ以外は蛋白合成阻害です。
■バンコマイシンとテイコプラニン
グリコペプチド系薬に分類され、殺菌的☆な作用を示します。元祖・抗MRSA薬と言っても過言ではないバンコマイシンは、比較的耐性が起こりにくく、最も長くMRSA治療の第一線で使用されています*。名は体を表すかのごとく、「バン」と一撃です(図18)。ただ、バンコマイシンは、MRSAによく効く代わりに、人も傷つきますので注意が必要です。
最も長くMRSA治療の第一線で使用されているバンコマイシン。MRSAによく効きますが、人も傷つきますので、ご使用は慎重に。
*日本では、バンコマイシン耐性黄色ブドウ球菌(vancomycinresistantStaphylococcus aureus, VRSA)による感染症の報告は2023年時点でありません。ただし、バンコマイシン耐性腸球菌(vancomycin-resistantEnterococci, VRE)が問題となっています。
β-ラクタム系薬と同様に、細胞壁合成を阻害しますが、β-ラクタム系薬とは標的が異なります。β-ラクタム系薬がPBPに結合するのに対して、グリコペプチド系薬はD-Ala-D-Alaに結合します(図19)。使用時は治療薬物モニタリング(therapeutic drug monitoring, TDM)が必要で、有効性と副作用の指標としてトラフ☆が重要になります。
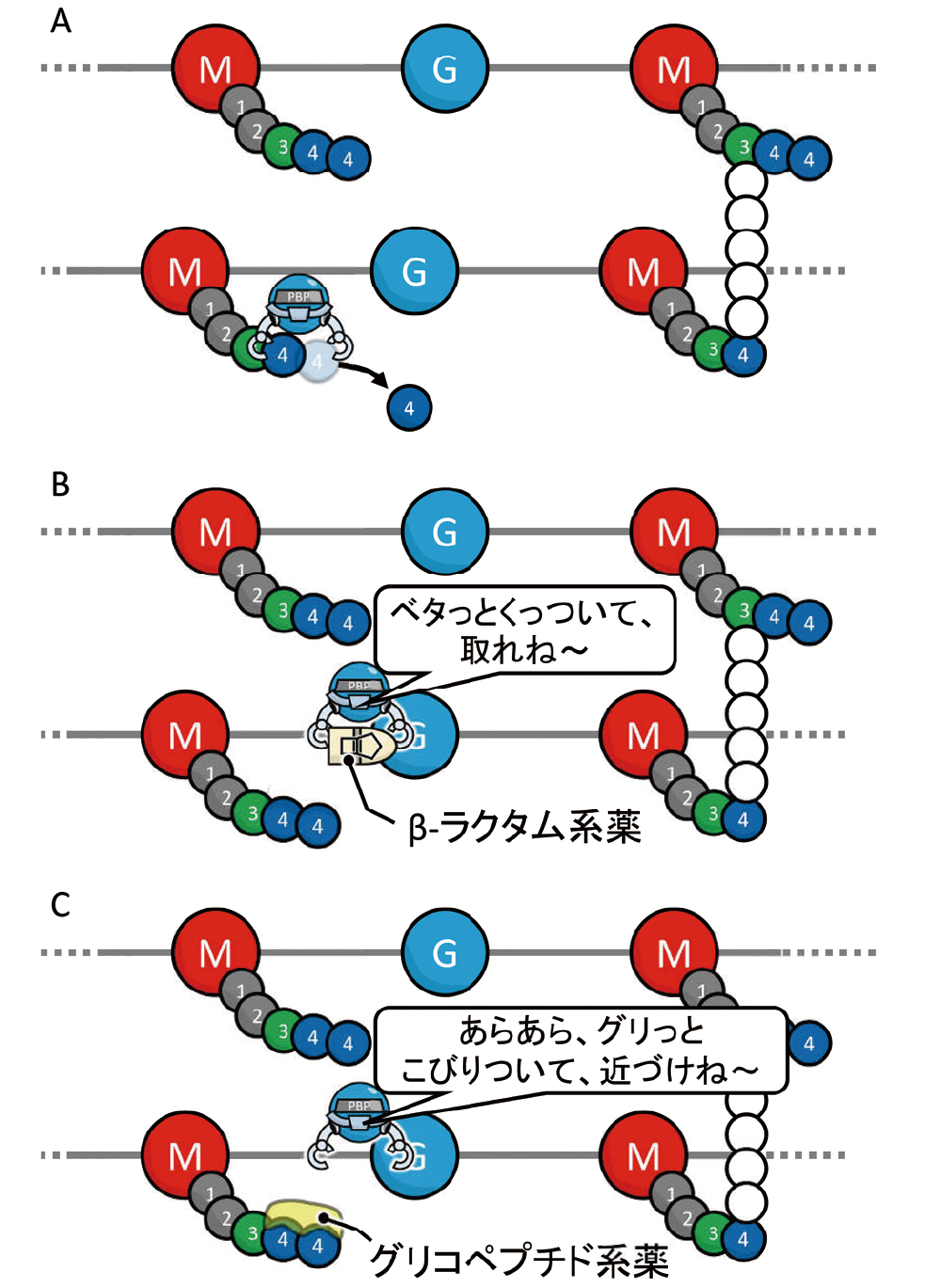
A 抗菌薬がない状態~PBPはD-Ala-D-Alaを解離させ、L-LysとD-Alaの間にペンタグリシンの架橋を行います。Bβ-ラクタム系薬は、PBPに結合して、PBPとD-Ala-D-Alaの結合を阻害します。C グリコペプチド系薬は、D-Ala-D-Alaに結合してPBPとD-Ala-D-Alaの結合を阻害します。
■アルベカシン
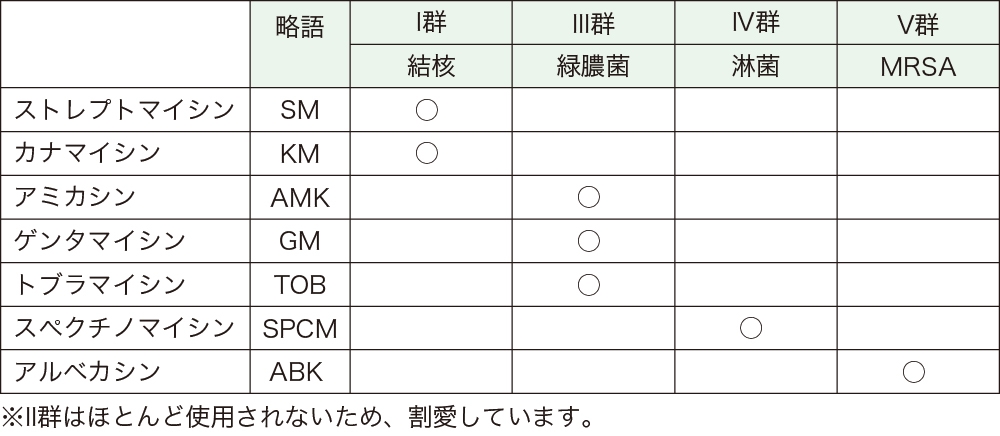
アミノグリコシド系薬*の一つです。アミノグリコシド系薬の標的はリボソームの30Sサブユニットで、蛋白の合成を阻害します。蛋白合成阻害薬は、一般に静菌的☆と言われますが、アミノグリコシド系薬は例外的に殺菌的☆です。アミノグリコシド系薬は、薬剤によってスペクトルが大きく異なるという特徴を持ち、抗MRSA薬として使用できるのはアルベカシンのみです。せっかくですので、抗MRSA薬以外のアミノグリコシド系薬についても参考のために列挙しておきます(表3)。
グリコペプチド系薬と共通点が多く、バイオアベイラビリティ☆はほぼ0、細胞内移行性も不良です。TDMが必要である点や、選択毒性☆が低く、内耳障害・腎毒性という副作用がある点も共通しています。トラフ☆とピーク☆が重要で、それぞれ副作用と有効性の評価の指標になります。ただし、グリコペプチド系薬が時間依存性☆であるのに対して、アルベカシンは濃度依存性☆です。
*アミノ配糖体とも呼ばれます。
■リネゾリドとテジゾリド
オキサゾリジノン系薬に分類され、リボソームの50Sサブユニットに結合し、蛋白合成を阻害します。一般的な蛋白合成阻害薬と同様に、静菌的☆な作用を示します。他の抗MRSA薬と最も異なる特徴は、バイオアベイラビリティ☆が高いということです。つまり、静注だけではなく、内服も可能であるということになります。静注は、原則として入院しているときにしか使えませんが、内服が可能になることで、外来でも投与が可能になります。経口へのスイッチに適した薬剤です。また、同じオキサゾリジノン系薬内でも、若干の違いがあり、その最たるものは、骨髄抑制です。リネゾリドには骨髄抑制がありますが、テジゾリドにはありません。
■ダプトマイシン
環状リポペプチド系薬で、細胞膜を直接傷害します。作用機序としては、最も新しい系統の抗MRSA薬です。殺菌的で、抗MRSA薬の中では、副作用も比較的少ない方です。肺サーファクタントによって不活化されるという弱点があるため、肺の感染症には適応となりません。また、当初は耐性化しにくいと言われていましたが、耐性化の報告もありますので、適正な使用は必要です。
用語説明
☆殺菌的(殺菌性)・静菌的(静菌性)殺菌的は文字通り菌を殺す能力、静菌的とは増殖を抑制するだけで菌を殺す能力がない(もしくは低い)ことを指しています。基準としては、菌数を99.9%減らす場合を殺菌的、それ未満を静菌的としています。ただし、数値はやや緩めに解釈されることもあります。
☆選択毒性菌に対する毒性とヒトに対する毒性を考えたときに、菌にのみ選択的に毒性を示すかどうか、また、その選択性の高さを、選択毒性と呼んでいます(図20)。毒性とついていることで悪そうな印象を与えますが、選択毒性は高いほど良く、低いほど悪いと言えます。抗MRSA薬の中には、選択毒性が低いものがあり、TDMを実施するなど、注意して使用する必要があります。
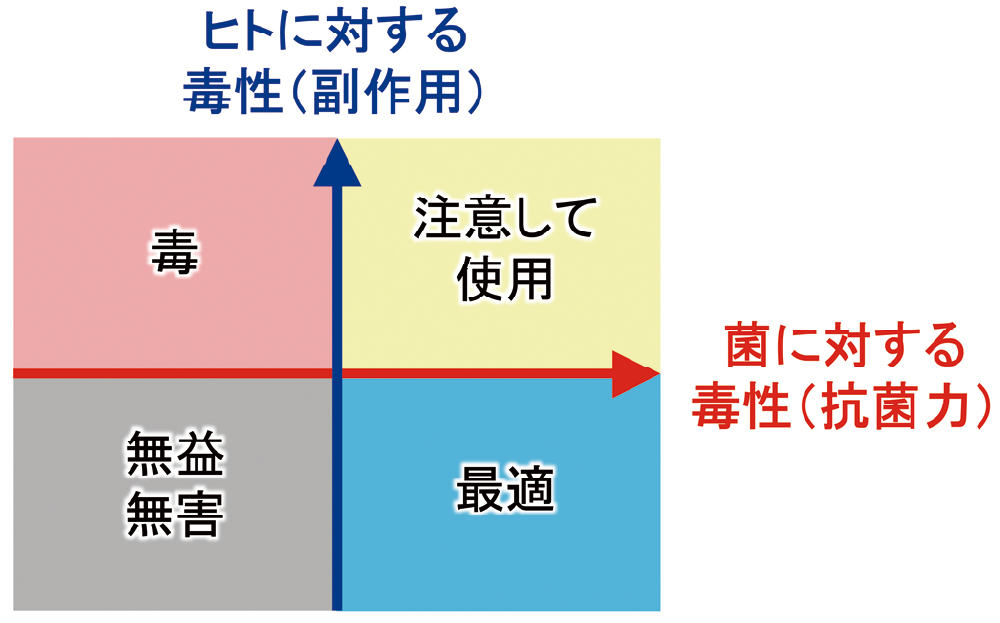
概念としては、「選択毒性=菌に対する毒性/ヒトに対する毒性」で、菌に対する毒性が高いほど、また、ヒトに対する毒性が低いほど、選択毒性は高くなります。
☆治療薬物モニタリング(Therapeutic Drug Monitoring,TDM)薬物の血中濃度を測定し、最適な投与量を調整することで治療効果を最大化し、副作用を最小化する手法です。特にバンコマイシンなど治療域が狭い薬に適用されます。
☆トラフとピーク(図21)トラフは定常状態における最低血中濃度、ピークは、組織分布が完了した時点における血中濃度です。最高血中濃度(Cmax)とピークは似ていますが異なります。
グリコペプチド系薬の場合、トラフが有効性と副作用の指標となり、バンコマイシンでは10~20μg/mL、テイコプラニンでは15μg/mLになるように投与量を調整することが推奨されています*。
一方、アルベカシンは、トラフとピークが重要で、それぞれ副作用と有効性の評価の指標になります。平たく説明すると、トラフはできるだけ低く、ピークはできるだけ高く、ということになります。
トラフの測定は、次の投与直前(投与前30分以内)に採血すればよいため、比較的容易ですが、ピークの測定はやや煩雑です。アルベカシンの場合、ピークの測定は、点滴開始1時間後(30分で投与した場合、終了30分後)に採血を行います。そのような理由もあり、グリコペプチド系薬よりもアルベカシンはやや使いづらく、使用される機会は少なくなっています。また、腎機能によって用量調整が必要で、通常は24時間ごとの投与ですが、腎機能に応じて48時間ごとに投与する場合があります。つまり、
ABKを
ABnormal
Kidneyに使う場合には
ABK48ですね。
*本稿では、簡便のため従来の考え方を示しています。近年は、特に重症例の場合、臨床効果と安全性からAUC/MICによる用量調整が推奨されるようになっています。
☆時間依存性と濃度依存性(図21)抗菌薬の有効性は、「有効濃度を上回っている時間の長さ」もしくは「血中濃度の高さ」のいずれかに依存することが知られています。前者を時間依存性、後者を濃度依存性と呼びます。前者の好例がグリコペプチド系薬、後者の好例がアルベカシンです。どちらもTDMが必要な薬剤ですが、有効性の指標が異なります。
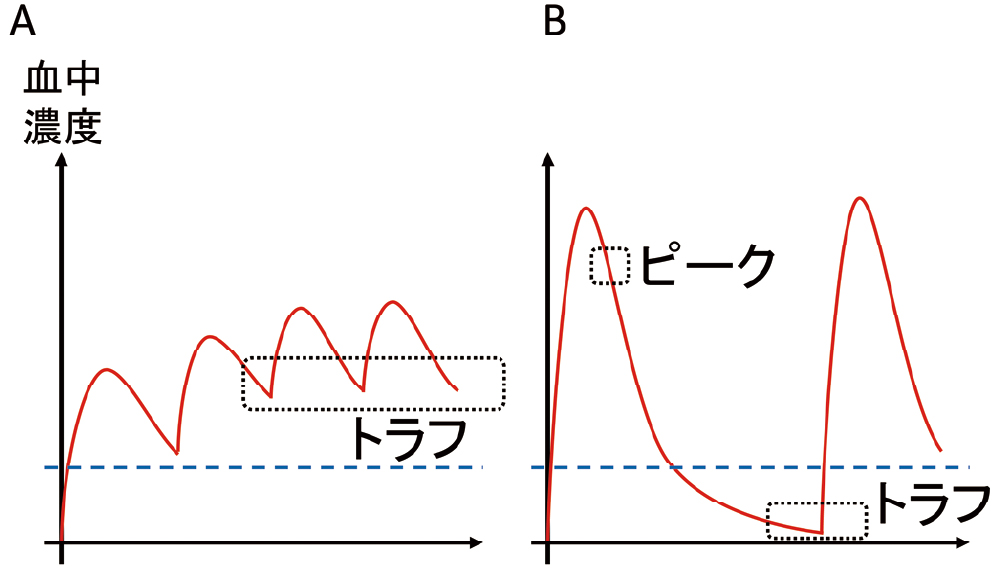
TDMの見るべきところが異なる
グリコペプチド系薬は時間依存性でトラフが有効性の指標になります(A)。一方、アルベカシンの場合には、トラフは副作用のピークは有効性の指標となります(B)。
☆バイオアベイラビリティ(図22)バイオアベイラビリティ(bioavailability, BA)とは、内服した際に、どれくらい体内に取り込まれるのか、静注した場合を100%として考えたときの割合で、生体利用率、生物学的利用能とも呼ばれます。BAが高いほど内服に適しています。抗MRSA薬のうち、リネゾリドとテジゾリド以外は、BAが0に近いので内服ができません。
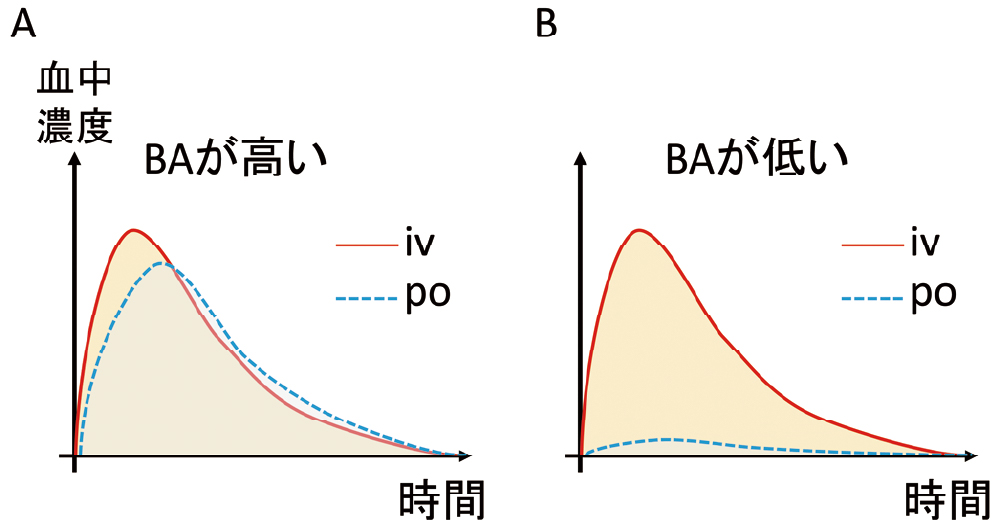
静注(iv)した際の利用率を100%としたときの内服(po)した際の利用率の割合(poでの利用率/ivでの利用率)で表します。図中の曲線下の面積がそれぞれの利用率になります。
参考
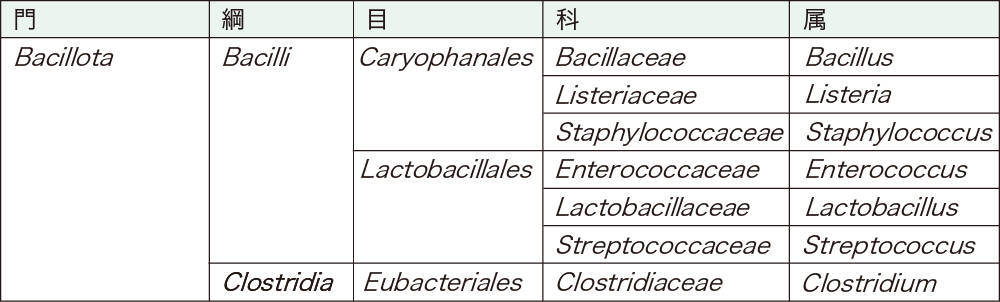
学術的な分類を眺める機会も少ないと思いますので、参考までに、ブドウ球菌がどのあたりに位置付けられるのか表にしてみました(表4)。バチルス門(Bacillota)の代表的な細菌と比較してみると、ブドウ球菌は、レンサ球菌よりもバチルス属やリステリア属に近いことが分かります。
腸球菌(Enterococcus)
■細菌学的特徴
黄色ブドウ球菌のところで出てきましたが、腸球菌はレンサキューキン家の分家です。本家のA群溶連菌(Streptococcus pyogenes)やB群溶連菌(S.agalactiae)と姿はよく似ていますが、本家に比べて病原性は低く、庶民の仲間入りをした印象の細菌です(図23)。
以前はレンサキューキン家のD軍に分類されていましたが、現在は、分家である腸キューキン家(Enterococcus属)になっています。
*キャラクター名として「群」を「軍」という表現にしています。
■地味で玄人好みの腸球菌
臨床的にしばしば分離される細菌ではありますが、病原性が低いため、地味というか、玄人好みの細菌です(あくまでも個人的な感想です)。糞便などから分離されるのは当たり前なので、そのような分離菌はほとんど見向きもされません。また、肺炎球菌や黄色ブドウ球菌は特定の菌種を指しますが、腸球菌は属レベルでひとくくりにされた呼び名で、分類上も「雑草」と同程度に扱われている気がします。属名のEnterococcusは、腸を表すenteroと球菌を表すcoccusの合成で、日本語でもまんまの訳になっています。連鎖状のグラム陽性球菌として、1900年代初頭から知られていましたが、当初はStreptococcus属(Lancefield分類*ではD群に相当)に分類されていました。1984年にE.faecalisとE.faeciumとしてEnterococcus属に分類されました。耐熱性、耐塩性があり、乾燥にも強いといった、Streptococcus属よりも環境中での生息に有利な特徴を持っています。
現時点で80菌種**が知られていますが、ヒトに病原性を示す代表的な菌種は、E.faecalisとE.faeciumがほとんどを占めます。どちらもfeces(糞便、ラテン語のfaex)に由来します。菌の名前とは言え、「金色のブドウ球菌」を意味するStaphylococcus aureusに比べ、若干残念な名前です。ともあれ、名は体を表すということで、糞便中からしばしば分離されるというイメージは痛いほど伝わります(図24)。それ以外の菌種として、かつて稀であったE.casseliflavusやE.gallinarumもVRE感染症の原因菌として近年増えています。尚、casselとflavusはともに黄色を、gallinarumは雌鶏を表します。
*Lancefield分類は、Streptococcus属の細胞壁の多糖体の抗原性による血清学的な分類です。前述のA群、B群もLancefield分類です。
**他の属に再分類されているものも含みます。
両菌種とも、便を表す「feces」に由来します。属名も種名も糞便中から分離されやすいというイメージを伝えてくれます。
E.faeciumの方が耐性傾向が強く、VREも多くがE.faeciumです。
■腸球菌はβ-ラクタム系薬に対する感受性が特徴的
腸球菌といえば、β-ラクタム系薬感受性の特徴がよく知られています。原則として、β-ラクタム系薬は、ペニシリン系薬<セフェム系薬<カルバペネム系薬の順に広域になるというヒエラルキーのようなものがあります。一般に、ペニシリン系薬が有効な菌種には、セフェム系薬も有効です。しかしながら、腸球菌はセフェム系薬にのみ自然耐性を示すため、ペニシリン系薬が有効であってもセフェム系薬が無効な場合があります。このように、腸球菌は、β-ラクタム系薬のヒエラルキーの原理の外側にあるちょっと変わった細菌です。同様に、ペニシリン感受性かつセフェム系薬耐性の性質を示す細菌として、Listeria monocytogenesが知られています。
バンコマイシン耐性腸球菌(vancomycin-resistantEnterococci)
■VREは青の大関
VREは文字通り、バンコマイシン耐性の腸球菌です。感染症の発生はそれほど増えていませんが、分離頻度が少ないながらも年々増加しています。また、治療にも難渋するということで、青の大関に位置付けています。
バンコマイシン(VCM)の耐性機序を理解するには、先に作用機序も知っておく必要があります。ということで、作用機序と耐性機序の説明に進みます。同じグリコペプチド系薬のテイコプラニン(TEIC)もほぼ同様です。
■バンコマイシンの作用機序と耐性機序
細胞壁の主成分であるペプチドグリカンの合成は、PBPが担当しています。PBPはペンタペプチドの末端のD-Alaを切り離し、L-LysとD-Alaの間にペンタグリシンの架橋を行います(図25A)。ところが、VCMなどのグリコペプチド系薬は、D-Ala-D-Alaにこびりついて、PBPの作用を邪魔します(図25B)。そこで、末端のD-AlaをD-Lac(もしくはD-Ser)に変更することで、VCMやTEICの結合を阻止します(図25C)。PBPは末端がD-Lac(もしくは-D-Ser)に変化しても、本来の機能を発揮することができるため、グリコペプチド系薬に耐性になります(図25D)。
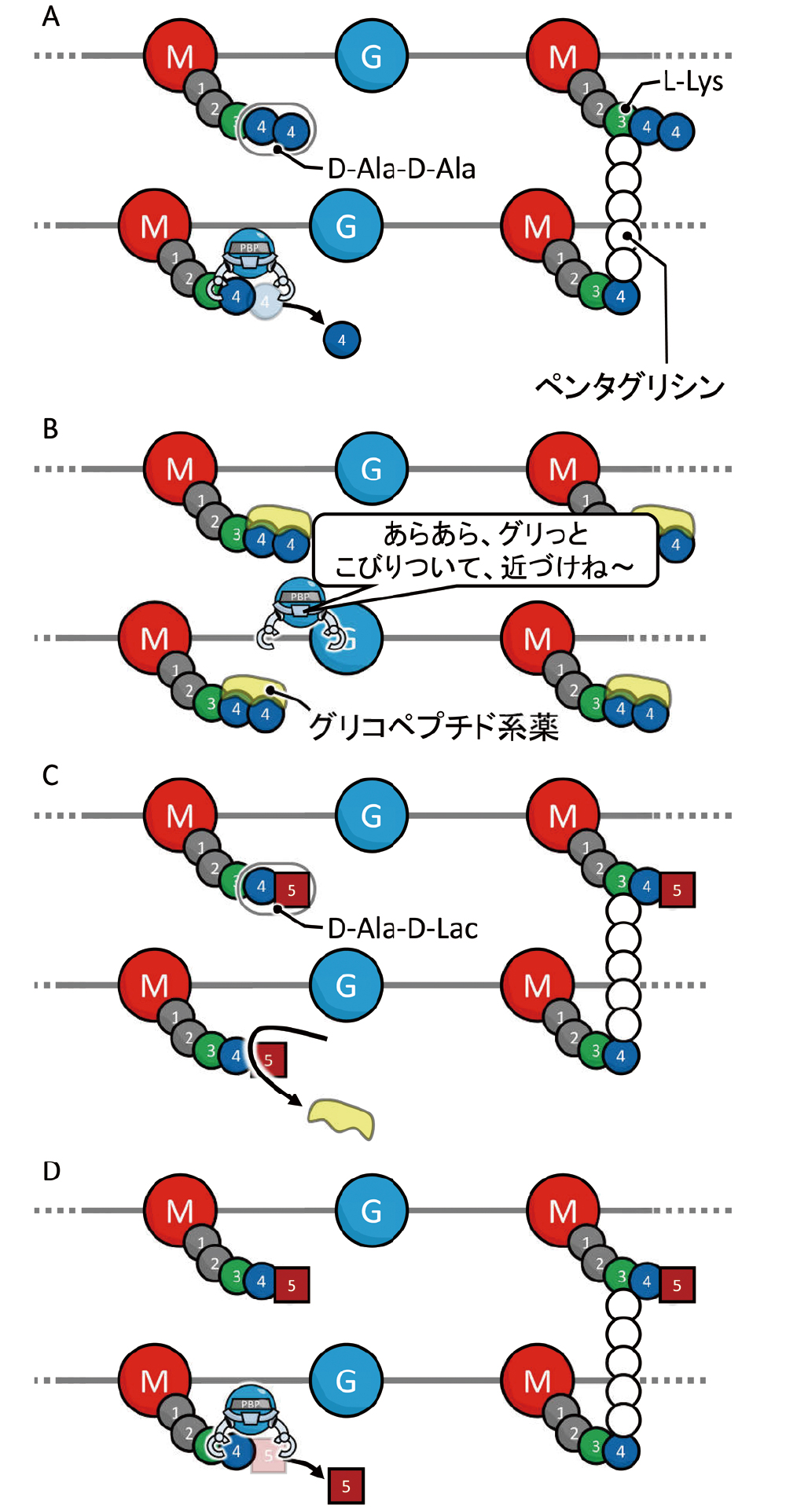
A 抗菌薬がない状態~PBPはD-Ala-D-Alaを解離させ、L-LysとD-Alaの間にペンタグリシンの架橋を行います。B グリコペプチド系薬は、D-Ala-D-Alaに結合してPBPと
D-Ala-D-Alaの結合を阻害します。C D-Ala-D-Alaが、D-Ala-D-LacやD-Ala-D-Serなどに変化し、グリコペプチド系薬が結合できなくなります。D D-Ala-D-Alaが、D-Ala-D-LacやD-Ala-D-Serなどに変化しても、PBPは本来の機能を発揮することができます。
■アイテムゲット型と内蔵型の耐性遺伝子
バンコマイシン(VCM)に対する主な耐性遺伝子として、vanAとvanBが知られています。vanAは主にプラスミド性、vanBは主に染色体性です。つまり、プラスミド性はアイテムゲット型、染色体性は内蔵型と考えるとわかりやすいかもしれません。ただし、染色体性のvanBも腸球菌同士で伝達されることが知られています。vanAとvanBは、ともに、D-AlaとD-Lacを結合させる酵素です(図26)。
*頭文字が小文字で斜体は遺伝子名、頭文字が大文字で正体は蛋白質名を表しています。
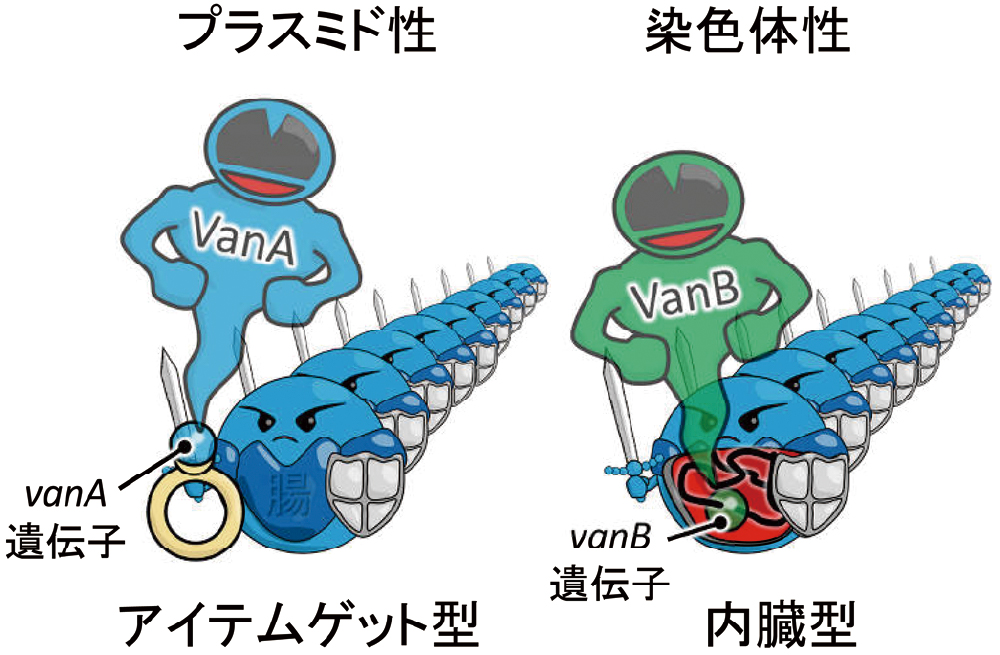
vanAは主にプラスミド性、vanBは主に染色体性です。プラスミドは受け渡しが容易なのでアイテムゲット型、染色体性の場合には元々組み込まれているので内蔵型に喩えています。ただし、染色体性のvanBも腸球菌同士で伝達されることが知られています。
■グリコペプチド系薬によって発現が誘導される
vanAもvanBも誘導型で、グリコペプチド系薬によって誘導されます。ただし、vanAはVCMとテイコプラニン(TEIC)の双方、vanBはVCMのみで誘導されます。vanAやvanBを持っていないか、もしくは持っていてもVCMとTEICがない状況では、Ddl(D-Ala-D-Alaリガーゼ)がD-AlaとD-Alaを結合させます(図27①)。その後、MurF(UDPN-アセチルムラモイルトリペプチド-D-Ala-D-Alaリガーゼ)によって、N-アセチルムラモイルトリペプチドにD-Ala-D-Alaが結合し、N-アセチルムラモイルペンタペプチドが合成されます(図27②)。D-Ala-D-Alaを末端に持つ通常のN-アセチルムラモイルペンタペプチドが細胞壁の「横糸」に取り込まれます(図27③)。結果として、グリコペプチド系薬に感受性となります。
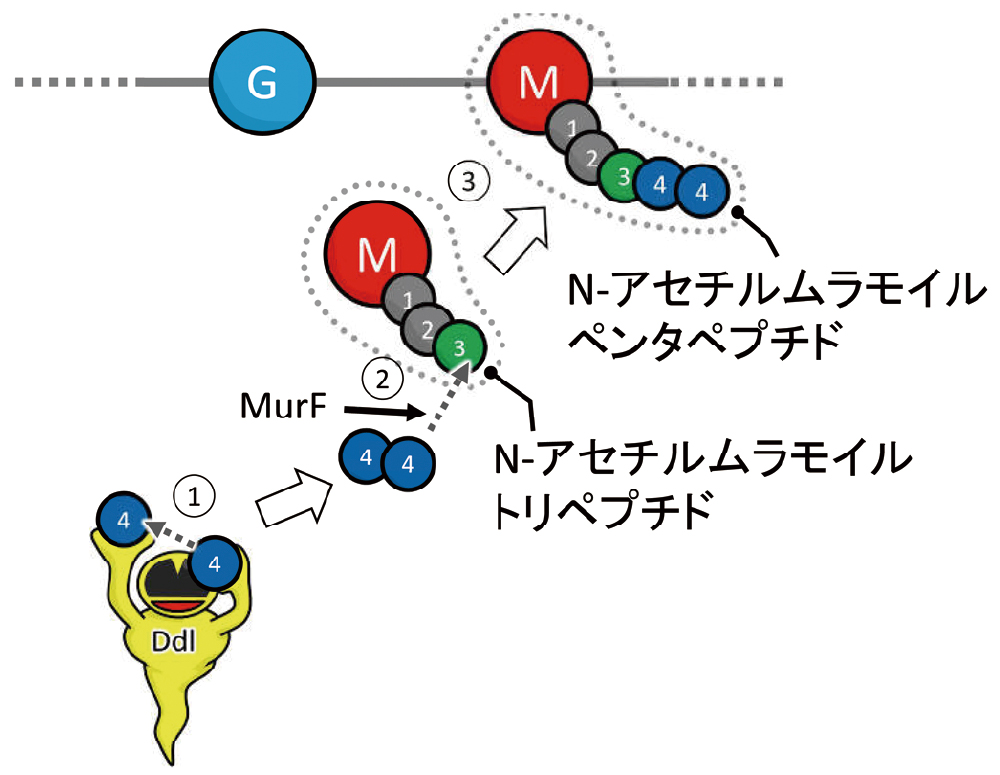
①Ddl(D-Ala-D-Alaリガーゼ)がD-AlaとD-Alaを結合させます。②MurF(UDP-N-アセチルムラモイルトリペプチド-D-Ala-D-Alaリガーゼ)が、N-アセチルムラモイルトリペプチドにD-Ala-D-Alaを結合させます。③通常のN-アセチルムラモイルペンタペプチドが細胞壁の「横糸」に取り込まれ、バンコマイシン感受性の細胞壁の成分となります。
VanAは、Ddlに類似した機能を持っていますが、D-Alaの代わりに、D-Lacを結合させる酵素です。VanAは単独で機能するのではなく、VanS、VanRなどの一連の遺伝子群と共同で働きます。VanSはセンサー、VanRはレギュレーターです。VanSはVCMとTEICのどちらも感知することができます。まず、VanSがこれらの抗菌薬を感知し、リン酸化されます(図28①)。次に、VanSのリン酸基がVanRに転移することで情報が伝達され、リン酸化されたVanRがvanAを含む耐性遺伝子を誘導します(図28②)。誘導されたVanAはD-AlaとD-Lacを結合させます(図28③)。MurFが、N-アセチルムラモイルトリペプチドにD-Ala-D-Lacを結合させます(図28④)。このようにしてできたD-Ala-D-Lacを末端に持つ変異型のN-アセチルムラモイルペンタペプチドが細胞壁の「横糸」に取り込まれ、結果として、バンコマイシンが結合できない、バンコマイシン耐性の細胞壁の成分ができあがります(図28⑤)。
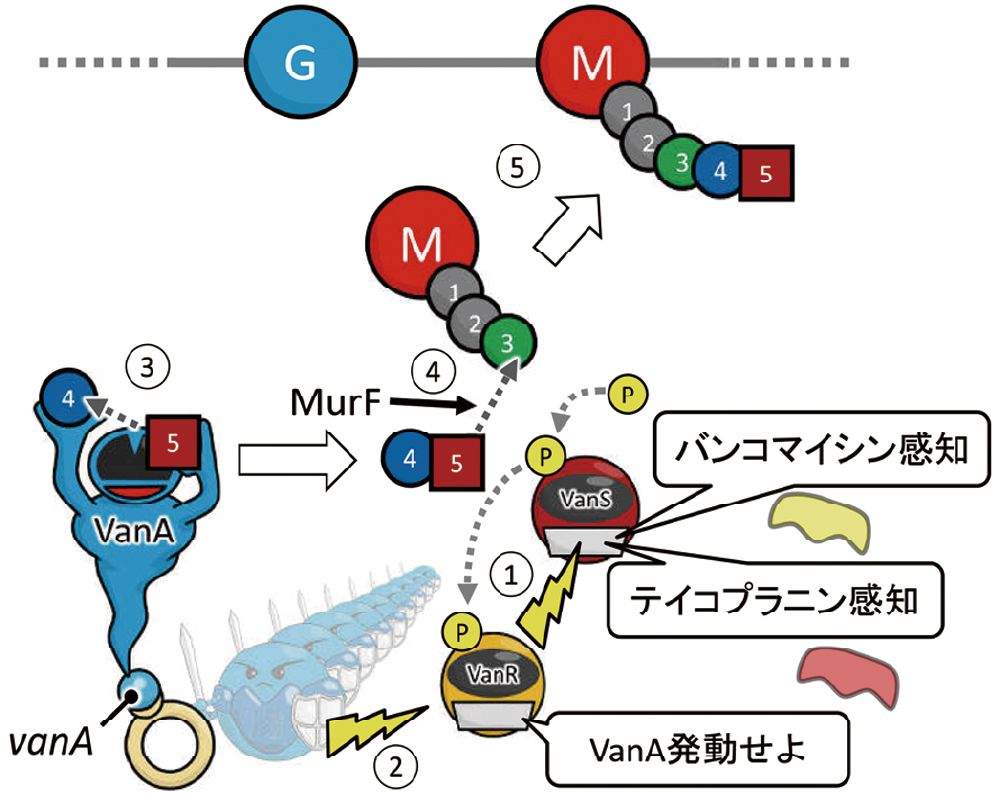
①VanSがバンコマイシンまたはテイコプラニンを感知し、リン酸化が起こります。②VanSのリン酸基がVanRに転移することで情報が伝達され、リン酸化されたVanRがvanAを含む耐性遺伝子を誘導します。③VanAはD-AlaとD-Lacを結合させます。④MurFが、N-アセチルムラモイルトリペプチドにD-Ala-D-Lacを結合させます。⑤D-Ala-D-Lacが末端にあるN-アセチルムラモイルペンタペプチドが細胞壁の「横糸」に取り込まれるため、バンコマイシンが結合できない、バンコマイシン耐性の細胞壁の成分ができあがります。
VanBの場合も同様ですが、センサーとレギュレーターが異なっており、それぞれ、VanSB、VanRBと呼ばれています。VanAの場合と異なり、TEICには反応しないため、VanBタイプの場合にはVCMでのみ誘導されます(図29)。つまり、VCM耐性、TEIC感受性という結果になります。
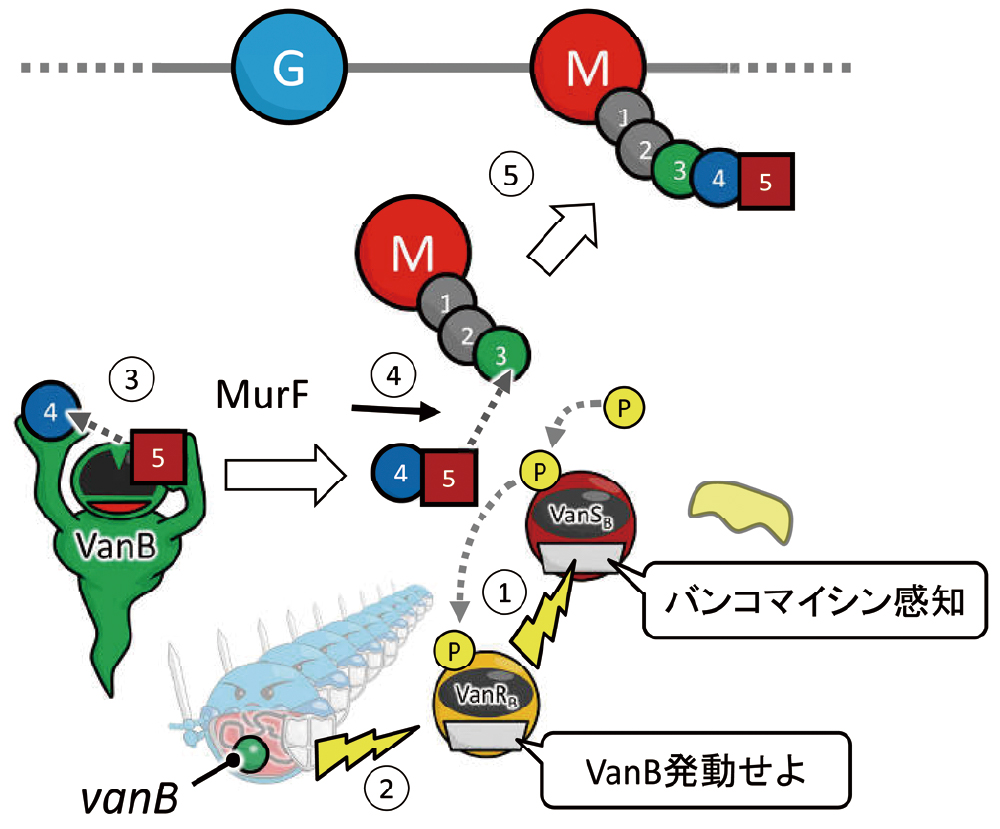
①VanSBがバンコマイシンを感知します。テイコプラニンは感知できません。②VanRBに情報が伝達され、VanRBがvanBを含む耐性遺伝子を誘導します。③~⑤の過程は、VanAの場合と同様です
■バンコマイシン耐性腸球菌の疫学
先述のように、D群Streptococcus属から、Enterococcus属に分類されたのは1984年で、そのわずか4年後、1988年にVREが初めて報告されました(分離は1986年)。1990年代以降、VREの報告が増えています。
腸球菌のみの分離頻度では、E.faecalisの方がE.faeciumよりも多く、およそ2:1の割合です(表5)。しかしながら、VREのうちの多くがE.faeciumで、E.faecalisはVREの10%未満です。また、病原性が低いため分離されても必ずしも感染症の原因になっているとは限りません。VRE感染症が5類全数報告の対象となっているため、感染症の疫学も分かっていますが、感染症に限ってみても、VREの多くがE.faeciumです。国立感染症研究所(2019年)のまとめによれば、VREの70%がE.faeciumとなっています。それ以外の菌種は、E.casseliflavusが9%、E.faecalisが6%、E.gallinarumが5%となっています。
2022年の院内感染対策サーベイランス(JANIS)の報告(入院部門)では、VREが分離されたことのある医療機関の割合は8.6%と、限られた医療機関で分離される傾向にあります。ほぼ100%の医療機関で分離されているメチシリン耐性黄色ブドウ球菌(methicillin-resistantS. aureus, MRSA)とは対照的です。VCMの耐性率は、E.faecalisで0.006%、E.faeciumで2.6%と、諸外国に比べ低率で、比較的稀な耐性菌であると言えます(表5)。しかしながら、施設差や地域差が多いことが知られており、VREの保有率が10%を超えるような施設や地域が報告されています。またVREの院内感染の事例もしばしば報告されており、一旦定着すると、取り除きにくいことから、今後の増加が懸念されています。日本では、2000年から2010年までは右肩上がりで増加し、2009年、2010年は100を超えていましたが、その後若干減少し2011年から2019年までは年間100例を下回っていました。しかしながら、COVID-19が流行し始めた2020年の発生動向調査によると、135例と過去最高となり、2022年の速報値でも131例と高い水準となっています。COVID-19がどの程度影響したのか、因果関係は不明ですが、注目すべき耐性菌の一つとなっています。

■クローンによる集団発生
複数のクローンが知られていますが、ST17から派生したクローンが世界的に広がっていることが知られています。CC17と呼ばれる集団です。耐性機序はVanA型で、日本でもCC17による集団発生が複数報告されています。近年、複数の国で報告が増えている型は、ST1421という遺伝子型です。ST1421は、MLSTに用いる7遺伝子の1つであるpstSを欠損するという特徴を持ち、pstSnullと呼ばれています。日本では、2022年に初めてST1421の分離の報告があり、青森で地域をまたいで流行した株であることが示されています。大阪地区では、非流行地域のある施設において施設内で多クローン性の集団発生が起こったことが報告されています。本事例の株は、全てCC17に属するE.faeciumでしたが、MLSTでは6つ、PFGEでは10以上に分類されています(表6)。共通点として、vanAタイプの遺伝子群を持つ直鎖状プラスミドを保有していました。このプラスミドが、多クローン性の集団発生に寄与した可能性が示唆されます。なお、プラスミドと言えば通常は環状ですが、この報告の場合には直鎖状であった点も興味深いところです。
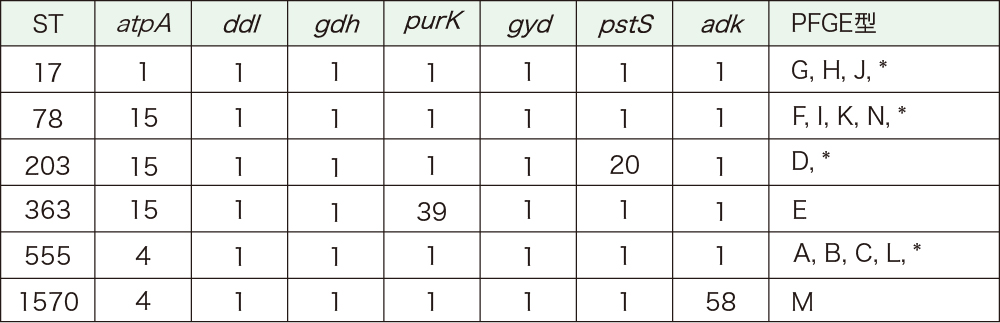
*はPFGE型未定(文献23を基に作成)
コラム
“遊びながら”学べる
ゲームの紹介
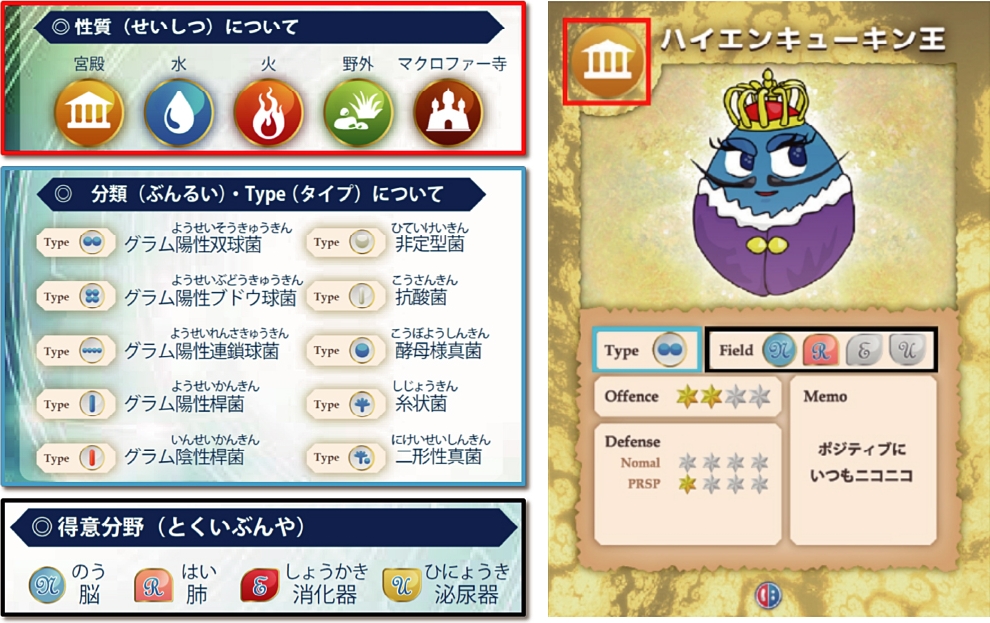
せっかくの機会ですので、「バイキンズ®カード」も紹介させてください(図1)。
図のように菌の性質、病気を起こす臓器、学術的な分類、病原性、薬剤耐性をシンボル化したカードで、遊びながら学べる優れものです。
自分で書いたイラストですので、まさしく、「自画自賛」の産物ですが、ぜひ、一家に一セットいかがでしょうか。
また、無料で遊べるゲームも公開しています。現在、3つほどありまして、第一作は、「Baikins War~UIJIN」です(図2)。抗菌薬の使い方を誤ると、耐性菌が出現するといった本格的なゲームです。短いストーリーですのでお気軽にお試しください。
感染対策などの講習会にお使いいただいても構いません。もちろん、無料です。よろしければ、講習会の様子などをSNSに挙げていただくと光栄です。