K.C.L®点滴液15% 20mL×10アンプル
基本情報
| 発売開始 | 2005年7月 |
|---|---|
| 日本薬局方/ 規制区分 |
処基 |
- 日本薬局方
- 劇薬
- 毒薬
- 向精神薬
- 習慣性医薬品
- 処方箋医薬品
- 後発品
- 基礎的医薬品
- 第2類医薬品(指定第2類医薬品の取扱いはありません)
- 第3類医薬品
製品資料一括ダウンロード
※くすりのしおりはダウンロードされません。
各種コード
容量: 20mL×10アンプル
| 薬価基準収載医薬品コード | 3229400A1032 | |
|---|---|---|
| 個別医薬品(YJ)コード | 3229400A1032 | |
| レセプト電算処理コード |
銘柄別 620002577 統一名 000000000 |
|
| HOT番号 | 1073331010102 | |
| JANコード | 4987211305529 | |
| 統一商品コード | 211-305529 | |
| GS-1コード | 調剤包装単位コード | (01)04987211405526 |
|---|---|---|
| 販売包装単位コード | (01)14987211305526 | |
| 元梱包装単位コード | (01)24987211305523 |
本製品に関するお知らせ
- すべて
- 包装変更・その他
- 使用上の注意改訂等
-
包装・表示K.C.L.®点滴液15% 仕様変更のお知らせ
-
使用上の注意「K.C.L.®点滴液15%・エリキシル(10w/v%)」使用上の注意改訂のお知らせ
-
使用上の注意K.C.L.®エリキシル(10w/v%)・K.C.L.®点滴液15% 使用上の注意改訂のお知らせ 2020年4月
-
包装・表示K.C.L.®点滴液15% 可変表示済み個装箱を掲載しました(Lot;9X101~)2019年12月
-
包装・表示K.C.L.®点滴液15%資材変更のお知らせ (① 開封口の形状を変更 ② GS1可変情報追加により、製造番号・使用期限の書体・印字サイズの変更)(Lot.9X101~)2019年12月
-
包装・表示K.C.L.®点滴液15% 新バーコード表示対応済み個装箱及び調剤ラベルを掲載しました。(Lot;5Y251~)2016年1月
-
使用上の注意K.C.L.®点滴液15%使用上の注意改訂のお知らせ(【自主改訂】「相互作用」の「併用注意」 一部改訂、追記)2012年11月
-
包装・表示K.C.L.®点滴液15%包装変更のお知らせ(① 箱・ラベルの製造番号表記方法(インクジェット方式からレーザーマーカー方式に変更)、② 箱表記、③ 箱形状、④ 箱サイズの変更)2012年11月
-
包装・表示製造番号桁数変更のお知らせ 2012年2月
-
包装・表示K.C.L.®点滴液15% 仕様変更のお知らせ
-
包装・表示K.C.L.®点滴液15% 可変表示済み個装箱を掲載しました(Lot;9X101~)2019年12月
-
包装・表示K.C.L.®点滴液15%資材変更のお知らせ (① 開封口の形状を変更 ② GS1可変情報追加により、製造番号・使用期限の書体・印字サイズの変更)(Lot.9X101~)2019年12月
-
包装・表示K.C.L.®点滴液15% 新バーコード表示対応済み個装箱及び調剤ラベルを掲載しました。(Lot;5Y251~)2016年1月
-
包装・表示K.C.L.®点滴液15%包装変更のお知らせ(① 箱・ラベルの製造番号表記方法(インクジェット方式からレーザーマーカー方式に変更)、② 箱表記、③ 箱形状、④ 箱サイズの変更)2012年11月
-
包装・表示製造番号桁数変更のお知らせ 2012年2月
本製品に関するよくあるご質問
- 血管外漏出時の対処法は?
本剤に特有の対処法はありません。注射剤が血管外漏出した際は、患部を冷やす(冷罨法)などの一般的な対処法と同様の処置をお願いします1)。
一般的な対処法の例2)
1.点滴を中止し、薬液を吸引する。(薬液が明らかに溜まっている場合)
2.漏出数時間後:患部の冷却
3.消炎鎮痛作用のある外用薬(湿布、軟膏等)、ステロイド外用薬の使用参考資料
1)葛西英子:日本看護技術学会誌 2014;13(3):230-6.
https://www.jstage.jst.go.jp/article/jsnas/13/3/13_230/_pdf/-char/ja
2)診断と治療 1999;87(増刊号):289.
- 遮光保存するのはなぜですか?
曝光によりリボフラビンリン酸エステルナトリウムが分解し沈殿が発生するため、遮光保存をお願いします。
参考資料
電子添文:20.取り扱い上の注意
- 点滴中の遮光は必要か?
希釈後の光に対する安定性のデータはありませんが、調製当日、点滴中の曝光によるリボフラビンリン酸エステルナトリウムの分解の程度は低く、遮光は必要無いと考えられます。
- 投与速度を半分にすれば、濃度を倍にしても良いですか?
電子添文1)の6. 用法及び用量は、「その液の濃度は0.3w/v%(カリウムとして40mEq/L)以下として、1分間8mLを超えない速度で静脈内注射する。」ですので、
0.3w/v%(カリウムとして40mEq/L)を超える濃度は承認外となります。
なお、濃度が40mEq/L以上になると血管痛の報告2)があります。
参考資料
1)電子添文:6.用法及び用量
2)木村 里緒、他: 腎と透析 2004;56(4):542-5.【M0490129】
お役立ちツール
各コンテンツ(動画・PDFなど)は、ダウンロードしてお使いいただけます。また、各資材は本サイトから発注できます。
一部ポスターを除き、編集・改変などはご遠慮ください。一部コンテンツは、medパスでのログインまたは新規登録が必要です。
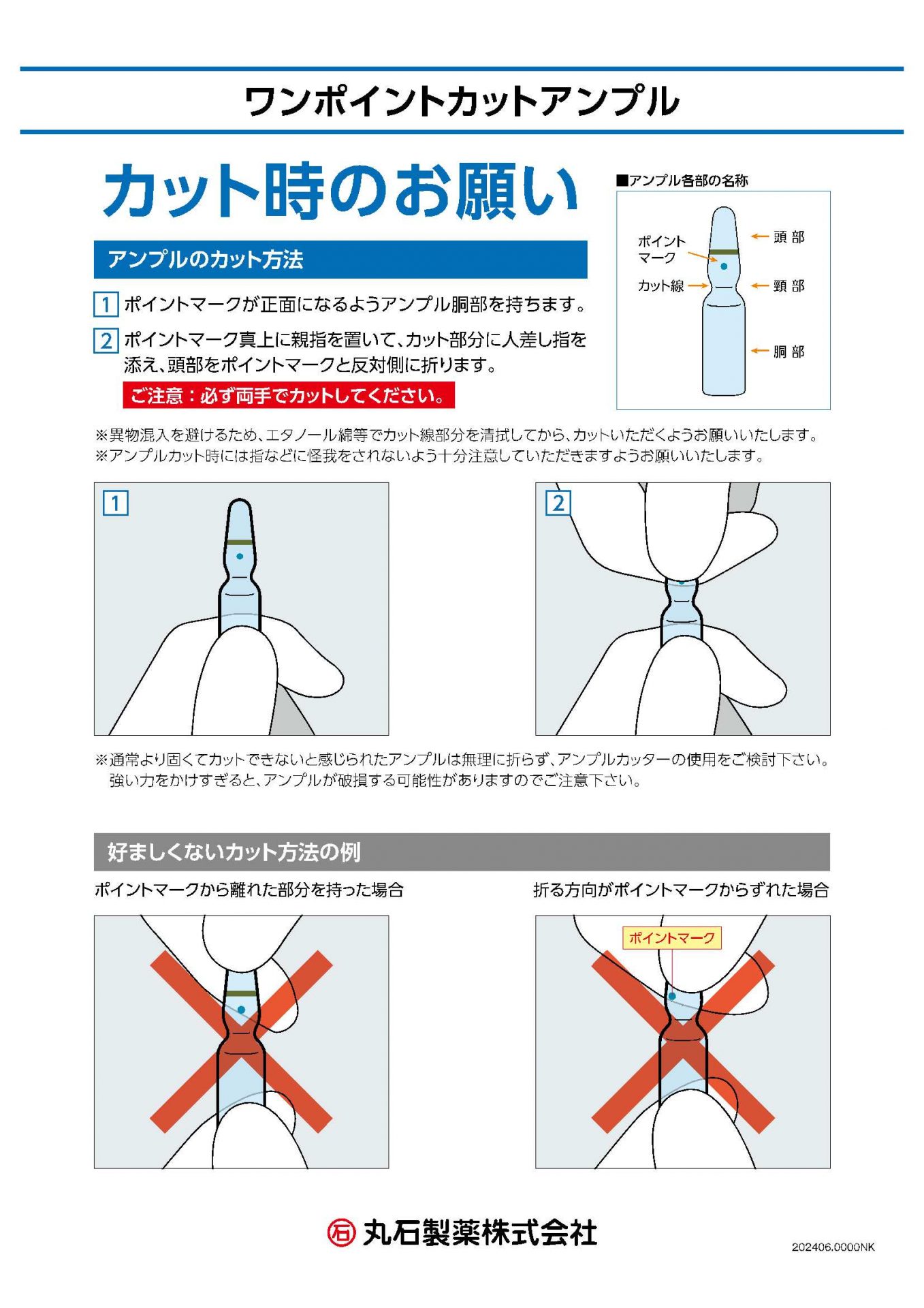
ワンポイントカットアンプル ーカット時のお願いー
(2024年06月03日)
くすりのしおり(日)
くすりのしおり(英)
資材をカートへ入れました。