国内工場で原薬から製剤・包装までの製造を実施
2002年より販売しているマグミット®錠の原料である酸化マグネシウムは、古来より塩の産地として栄えてきた香川県坂出市にて製塩の副産物である「にがり」から製造しています。
日本標準商品分類番号:872344・872355|薬価基準収載

2002年より販売しているマグミット®錠の原料である酸化マグネシウムは、古来より塩の産地として栄えてきた香川県坂出市にて製塩の副産物である「にがり」から製造しています。
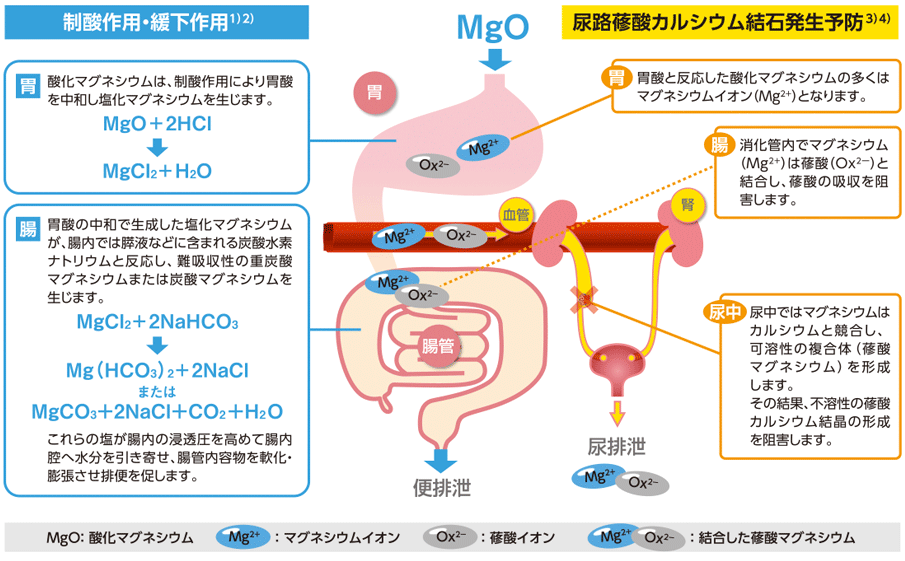
【下記疾患における制酸作用と症状の改善】
胃・十ニ指腸潰瘍、胃炎(急・慢性胃炎、薬剤性胃炎を含む)、上部消化管機能異常(神経性食思不振、いわゆる胃下垂症、胃酸過多症を含む)
【便秘症】
【尿路蓚酸カルシウム結石の発生予防】
【制酸剤として使用する場合】
酸化マグネシウムとして、通常成人1日0.5~1.0gを数回に分割経口投与する。
【緩下剤として使用する場合】
酸化マグネシウムとして、通常成人1日2g を食前又は食後の3回に分割経口投与するか、又は就寝前に1回投与する。
【尿路蓚酸カルシウム結石の発生予防に使用する場合】
酸化マグネシウムとして、通常成人1日0.2 〜 0.6g を多量の水とともに経口投与する。
なお、いずれの場合も年齢、症状により適宜増減する。
【緩下剤として使用する場合】
通常、1歳以上の小児には酸化マグネシウムとして、通常成人1日20〜80mg/kgを食後の2回に分割経口投与する。
【緩下剤として使用する場合】
小児は1日40mg/kgを開始用量の目安とし、患者の状態に応じて適宜増減すること。[17.1.1参照]
識別性向上のための工夫
・製品名「マグミット」と有効成分の含量を両面に印字し、
規格別の文字色を採用しています。

製剤設計
・マグミット®錠は水中に投入すると速やかに崩壊し、細かい粒子になります。
| 試験結果 | マグミット®錠100mg | マグミット®錠250mg | マグミット®錠330mg | マグミット®錠500mg |
| 平均崩壊時間(n=6) | 6秒 | 8秒 | 8秒 | 10秒 |
試験方法:日本薬局方 崩壊試験法 即放性製剤の項を準用して設定した試験方法により、錠剤が崩壊するまでの時間を測定した。
マグミット製薬社内資料:マグミット®錠100mgの製剤品質評価、マグミット®錠シリーズの製剤品質評価

試験方法:常温の水道水180mlにマグミット®錠330mgを投入し、静置した状態で錠剤が崩壊する様子を観察した。
※水なしで服用できるOD錠ではありません。
※服用感には個人差があります。また、速効性を保証するものではありません。
マグミット®錠100mg
・用量調整、携帯性を考慮した直径6mmの小型錠剤です。
・服用性の向上を目的に、酸化マグネシウム特有の味をマスキングするため、甘味剤を添加しています。
本剤の投与により、高マグネシウム血症があらわれることがあります。
腎機能が正常な場合や通常用量以下の投与であっても、重篤な転帰をたどる例が報告されていますので、以下の点に留意してください。
・必要最小限の使用にとどめること。
・長期投与または高齢者へ投与する場合には、定期的に血清マグネシウム濃度を測定するなど特に注意すること。
・高マグネシウム血症の症状(嘔吐、徐脈、筋力低下、傾眠等)があらわれた場合には服用を中止し、直ちに受診するよう患者に指導すること。
血清マグネシウム値と高マグネシウム血症時の症状 5) 6)
| 血清Mℊ濃度 | 症状 |
| 4.9mg/dL~ | 悪心・嘔吐・起立性低血圧、徐脈、皮膚潮紅、筋力低下、傾眠、全身倦怠感、無気力、腱反射の減弱など |
| 6.1~12.2mg/dL~ | ECG異常(PR、QT延長)など |
| 9.7mg/dL~ | 腱反射消失、随意筋麻痺、嚥下障害、房室ブロック、低血圧など |
| 18.2mg/dL~ | 昏睡、呼吸筋麻痺、血圧低下、心停止など |
副作用等の注意事項等情報については最新の電子添文をご参照ください。
〈参考文献〉
1)第十八改正 日本薬局方解説書 C-2112-2117(2021) / 2)山口 寿 最新医学8(4):397-405(1953) / 3)第十八改正 日本薬局方医薬品情報 JPDI 2021 / 4)山口 聡 ほか 泌尿器外科(11):1043-1049(1996) / 5)中村 孝司 日本医事新報(3540):177-178(1992) / 6)木村 琢磨 JIM 18(11):942-943(2008)
Qマグミット®錠は、いつから「便秘症」において1歳以上の小児の用法及び用量が追加されたのですか?
A2025年8月25日付で追加承認されました。(追加で発売となった100mgを含むマグミット®錠の全ての規格とマグミット®細粒83%)
Qマグミット®錠100mgは、いつから販売されているのですか?
A2025年10月29日(水)から販売しております。
Qマグミット®錠100mgは、後発品医薬品ではないのですか?
Aマグミット®錠 250mg 330mg 500mg は先発医薬品のない後発品医薬品ですが、マグミット®錠100mgは、先発医薬品として分類されています。
Qマグミット®錠100mgは、新医薬品の投薬期間制限(14日間を限度とする。)が適用されますか?
(掲示事項等告示第10第2号(一)に規定する新医薬品に係る投薬期間制限)
A新医薬品に係る投薬期間制限(14日間を限度とする。)は適用されません。
(既に薬価収載後1年以上を経過している「マグミット錠 200mg、同錠 250mg、同錠 330mg、同錠 500mg 及び同細粒 83%」と有効成分が同一であり、今般、既収載品において便秘症に係る1歳以上の小児における用法・用量が追加されたことに伴い、当該用法・用量に必要となる製剤として承認された剤形追加医薬品であるため)(令和7年10月21日付保医発1021 第9号:使用薬剤の薬価(薬価基準)の一部改訂等について)
Qマグミット®錠100mgは、成人患者にも使用可能ですか?
A適応上は処方可能ですが、薬価基準の一部改正に伴う留意事項において「本製剤は、既収載品において便秘症に係る1歳以上の小児における用法・用量が追加されたことに伴い、当該用法・用量に必要となる製剤として承認された剤形追加医薬品であることから、成人患者への本製剤の使用の必要性については慎重に判断すること。」との記載があることから、成人患者への使用については慎重にご判断の程よろしくお願いいたします。(使用薬剤の薬価(薬価基準)の一部改訂等について:令和7年10月21日付保医発1021第9号)
Qマグミット®錠 100mg、250mg、330mg、500mgの錠剤サイズを教えてください。
A白色・円形の素錠。(マグミット®錠 電子添文 2025年10月改訂(第3版))
| 販売名 | 外形 | 直径 | 厚さ | 質量 | 文字色 |
| マグミット®錠 100mg |
 |
6mm | 3.4mm | 120mg | 橙 |
| マグミット®錠 250mg |
 |
8mm | 4.4mm | 300mg | 緑 |
| マグミット®錠 330mg |
 |
9mm | 4.7mm | 396mg | 青 |
| マグミット®錠 500mg |
 |
10.5mm | 5.1mm | 600mg | ピンク |
Q胃酸分泌抑制剤を使用している患者でも効果はありますか?
Aマグミット®錠が緩下作用を発現するには、胃酸と反応する必要があります。そのため、胃の全摘や胃酸分泌抑制剤の使用により胃酸の分泌が低下している場合には十分な効果が得られない可能性があります。これは、胃内のpH上昇により、マグミット®錠の有効成分である酸化マグネシウムの溶解度が低下するためと考えられます。
Qマグミット®錠と併用することで高マグネシウム血症を起こしやすくなる薬剤はありますか?
A活性型ビタミンD3製剤、炭酸リチウム製剤との併用により高マグネシウム血症を起こす恐れがあるとされています。これらの薬剤との併用にはご注意いただき、定期的な血清マグネシウム濃度の測定を行って下さい。
Q血清マグネシウム濃度の測定はどれくらいの頻度で行えばよいですか?
A血清マグネシウム濃度の測定頻度に明確な基準はありません。患者さんの状態(腎機能、投与量、投与期間など)から判断をお願い致します。腎機能低下のある患者さん、高齢の患者さん、酸化マグネシウムとの併用により高マグネシウム血症を起こす恐れがある薬剤を服用されている患者さんでは特にお気をつけください。
Qマグミット®錠の一包化の際に参考となる資料はありますか?
A配合変化への注意喚起を行うため、マグミット®錠との配合変化の一例を示すマグミット®錠配合変化一覧表がございます。一包化は、極力避けてくださいますようお願い致します。
›› こちら(PDF)