伝達麻酔ポプスカイン0.25%注(バッグ250mg/100mLを除く)ポプスカイン0.5%注
「禁忌を含む使用上の注意」等は以下の製品情報をご参照ください。
ポプスカイン®0.25%注 25mg/10mL 製品情報はこちらをご参照下さい
ポプスカイン®0.25%注 シリンジ 25mg/10mL 製品情報はこちらをご参照下さい
ポプスカイン®0.5%注 50mg/10mL 製品情報はこちらをご参照下さい
ポプスカイン®0.5%注 シリンジ50mg/10mL 製品情報はこちらをご参照下さい
国内第Ⅲ相比較臨床試験(伝達麻酔:腕神経叢ブロック)
〔0.25%ブピバカイン塩酸塩を対照とした無作為化二重盲検並行群間比較試験〕7),8)
- 7)丸石製薬株式会社 社内資料 : 第Ⅲ相比較臨床試験(伝達麻酔(腕神経叢ブロック))(MR8A2-13)(承認時評価資料)
- 8)髙崎 眞弓他 : 麻酔と蘇生 2011;47(sup):93-108. [利益相反 : 丸石製薬株式会社の依頼によるMR8A2の第Ⅲ相臨床試験]
試験概要
- 目的
-
伝達麻酔(腋窩部腕神経叢ブロック)により上肢手術を受ける患者を対象に、ポプスカイン0.25%注の知覚神経遮断効果について、0.25%ブピバカイン塩酸塩注射液を対照薬として、有効性に関して非劣性の検証を行うとともに、安全性についても検討した。
- 対象
-
伝達麻酔(腋窩部腕神経叢ブロック)により上肢(肘関節と手関節の中間部より遠位)の手術を受ける患者 : 61例(ポプスカイン0.25%注群31例、0.25%ブピバカイン塩酸塩群30例)〔61例全例がFAS及び安全性解析対象であり、55例(ポプスカイン0.25%注群29例、0.25%ブピバカイン塩酸塩群26例)が有効性のPPS解析対象であった。〕
- 投与薬剤・投与量
-
ポプスカイン0.25%注群 : ポプスカイン0.25%注 40mL(100mg)
0.25%ブピバカイン塩酸塩群 : 0.25%ブピバカイン塩酸塩注射液 40mL(100mg)
- 投与方法
-
超音波プローブを腋窩部高位で上腕の長軸と垂直に当て、正中、尺骨、橈骨及び筋皮神経の同定を行った。プローブの外側縁中央から、神経ブロック針をプローブの長軸方向と平行に刺入し、針先を各神経にできるだけ接近させた。各薬剤の注入は、上記4神経に対して行うこととし、投与量は各神経10mLとした。その際、各薬剤がそれぞれ対象となる神経周囲を取り囲むように、ブロック針を動かしながら2~3mLずつ分割注入した。
- 評価項目
-
- 解析計画
-
主要評価項目は、Δ上乗せによる非劣性の検証(2標本t検定、Δ=1時間)を行った。副次評価項目1)、2)は記述統計量を算出、 3)は「有効」以上の割合を算出した。
有効性
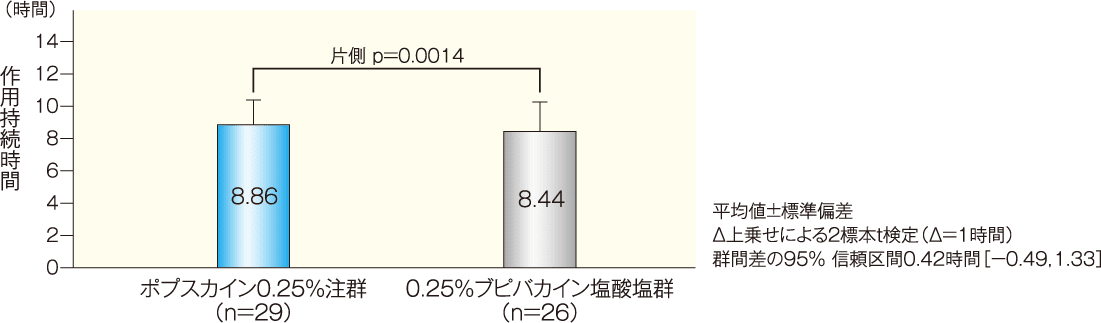
[主要評価項目]知覚神経遮断における痛覚消失効果の平均作用持続時間:PPS
知覚神経遮断における痛覚消失効果の平均作用持続時間(平均値±標準偏差)*は、ポプスカイン0.25%注群8.86±1.53時間、ブピバカイン塩酸塩群8.44±1.82時間であり、ポプスカイン0.25%注群の0.25%ブピバカイン塩酸塩群に対する非劣性が検証された(片側 p=0.0014、Δ上乗せによる2標本t検定、Δ=1時間)。両群間の差とその95%信頼区間は0.42時間[-0.49,1.33]であった。
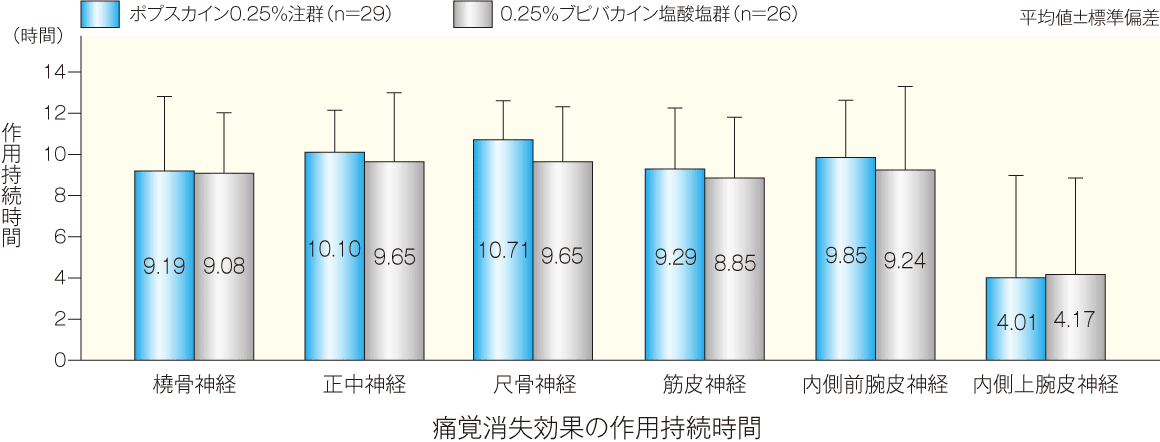
橈骨、正中、尺骨、筋皮、内側前腕皮及び内側上腕皮の6つの各神経支配領域での作用持続時間の平均値を示す。
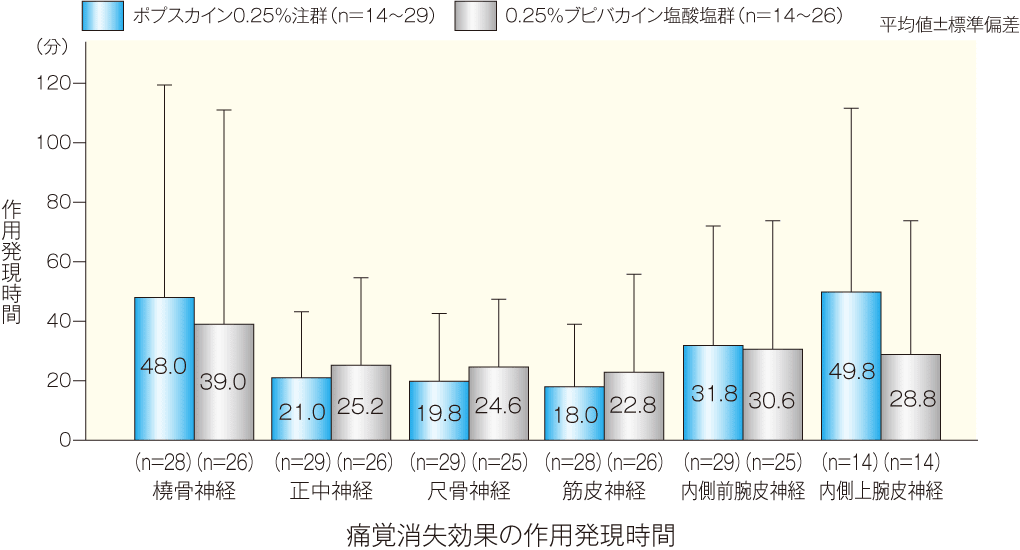
[副次評価項目]知覚神経遮断における痛覚消失効果(各神経支配領域での作用発現時間、作用持続時間):PPS
橈骨、正中、尺骨、筋皮、内側前腕皮及び内側上腕皮の6つの各神経支配領域の中で最も多く手術が施行された部位の正中神経領域において、痛覚消失効果の作用発現時間(平均値±標準偏差)は、ポプスカイン0.25%注群21.0±22.2分、0.25%ブピバカイン塩酸塩群25.2±29.4分であった。観察期間中に痛覚消失効果の作用発現が確認された症例について、内側上腕皮神経ではポプスカイン0.25%注群29例中14例(48.3%)、0.25%ブピバカイン塩酸塩群26例中14例(53.8%)であった。
痛覚消失効果の作用持続時間(平均値±標準偏差)は、正中神経領域においてポプスカイン0.25%注群10.10±2.05時間、0.25%ブピバカイン塩酸塩群9.65±3.35時間であった。内側上腕皮神経では、ポプスカイン0.25%注群4.01±4.97時間、0.25%ブピバカイン塩酸塩群4.17±4.68時間であった。
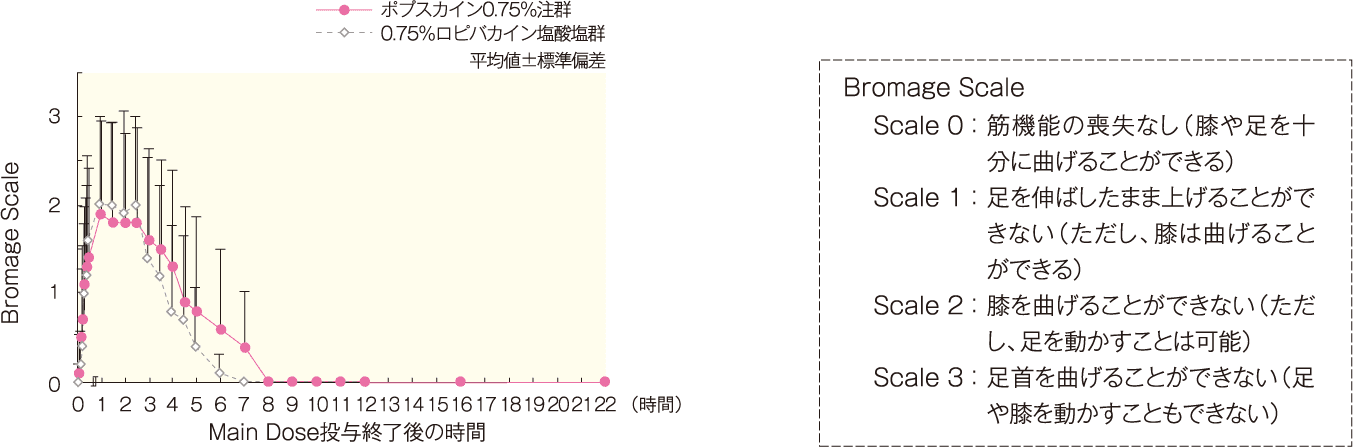
評価方法 : 橈骨神経、正中神経、尺骨神経、筋皮神経、内側前腕皮神経及び内側上腕皮神経支配領域における知覚神経遮断効果をpin-prick法にて以下に示す4段階で評価した。測定時期は、投与前及び投与後10, 20, 30, 40, 60分、2, 3, 4, 5,6, 7, 8, 9, 10, 11, 12, 24時間(判定基準の「1. 効果なし」に戻るまで2時間ごとに確認)。なお、痛覚消失とは「3. 痛覚消失」あるいは「4. 感覚消失」である状態を示すものである。
〔知覚神経遮断効果判定基準(pin-prick法)〕
1. 効果なし : 各薬剤投与前と変化なし、 2. 痛覚鈍麻 : 痛みを感じるが投与前ほどではない、 3. 痛覚消失(analgesia) : 触覚はあるが痛みは感じない、 4. 感覚消失(anesthesia) : 触覚も痛みも感じない
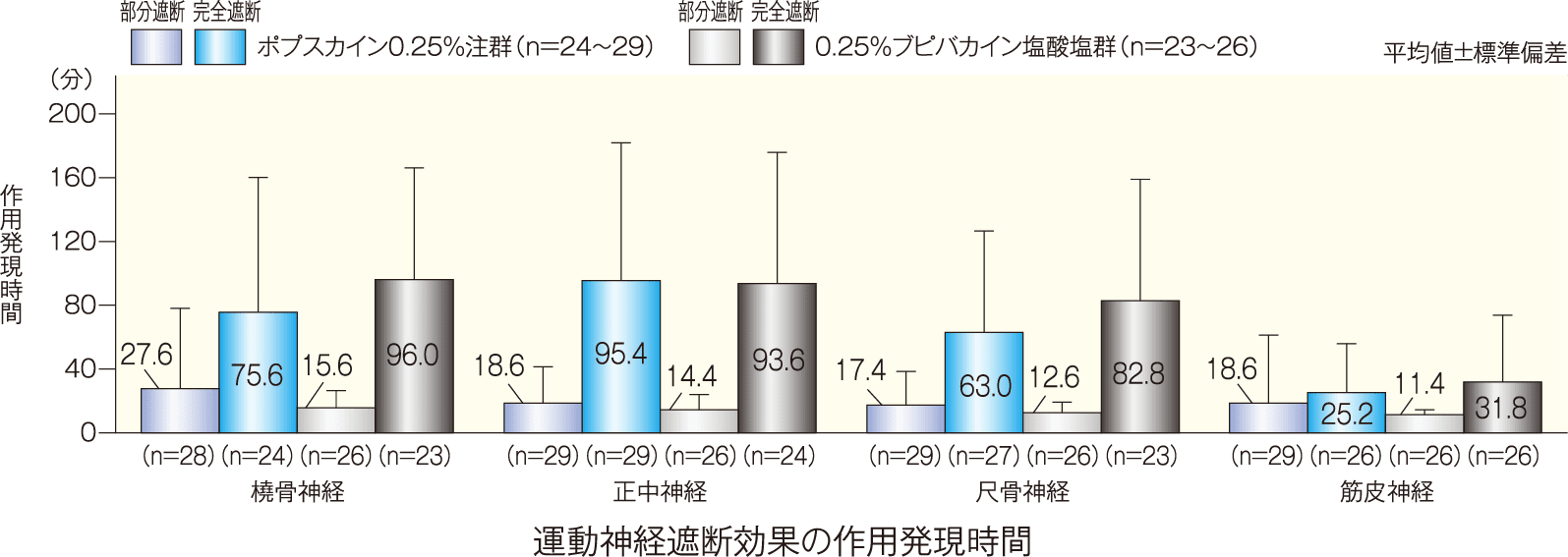
[副次評価項目]運動神経遮断効果(部分、完全)(各神経支配領域での作用発現時間、作用持続時間):PPS
橈骨神経、正中神経、尺骨神経及び筋皮神経支配領域のうち、正中神経領域における運動神経遮断効果の作用発現時間(平均値±標準偏差)は、部分遮断がポプスカイン0.25%注群で18.6±22.8分、0.25%ブピバカイン塩酸塩群で14.4±9.6分、完全遮断がポプスカイン0.25%注群で95.4±86.4分、0.25%ブピバカイン塩酸塩群で93.6±82.2分であった。
正中神経領域における運動神経遮断効果の作用持続時間(平均値±標準偏差)は、部分遮断がポプスカイン0.25%注群で11.00±1.13時間、0.25%ブピバカイン塩酸塩群で10.83±3.14時間、完全遮断がポプスカイン0.25%注群で6.72±3.67時間、0.25%ブピバカイン塩酸塩群で5.83±3.45時間であった。
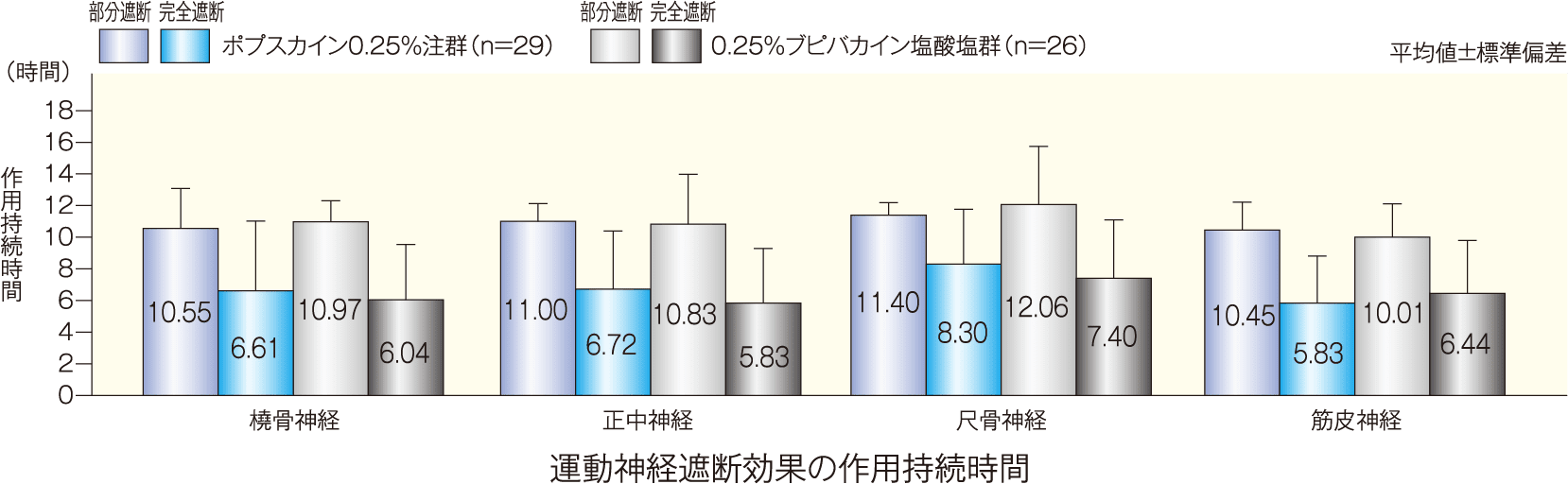
評価方法 : 橈骨神経、正中神経、尺骨神経及び筋皮神経支配領域における運動能をそれぞれ以下に示す基準により3段階で評価した。測定時期は、投与前及び投与後10,20,30,40,60分、2,3,4,5,6,7,8,9,10,11,12,24時間(判定基準の「1.運動神経遮断なし」に戻るまで2時間ごとに確認)。
〔運動神経遮断効果判定基準〕
- ①橈骨神経(手関節を背屈させる能力)
-
1. 運動神経遮断なし : 通常の力で手関節の背屈ができる、 2. 部分運動神経遮断あり : 手関節の背屈はできるが、筋力が低下している、 3. 完全運動神経遮断あり : 手関節の背屈ができない
- ②正中神経(母指と示指によって丸を作る能力)
-
1. 運動神経遮断なし : 通常の力で丸を作ることができる、 2. 部分運動神経遮断あり : 丸を作ることはできるが、筋力が低下している、 3. 完全運動神経遮断あり : 丸を作ることができない
- ③尺骨神経(指を揃えて手刀を作った状態から小指を外転させる能力)
-
1. 運動神経遮断なし : 通常の力で小指を外転させることができる、 2. 部分運動神経遮断あり : 小指を外転させることはできるが、筋力が低下している、 3. 完全運動神経遮断あり : 小指を外転させることができない
- ④筋皮神経(肘関節を屈曲させる能力)
-
1. 運動神経遮断なし : 普通に肘の屈曲ができる、 2. 部分運動神経遮断あり : 肘の屈曲はできるが、筋力が低下している、 3. 完全運動神経遮断あり : 肘の屈曲ができない
[副次評価項目]手術施行に対する評価(「有効」以上の割合):FAS
手術施行に対する評価について、「有効」以上の割合は、ポプスカイン0.25%注群96.8%(31例中30例)、0.25%ブピバカイン塩酸塩群93.3%(30例中28例)であった。
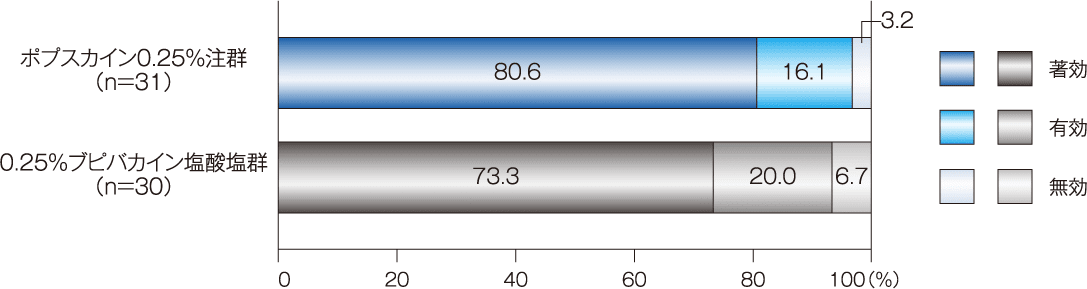
手術施行に対する評価基準
- 「著効」: 本剤のみの投与により手術が可能であった
- 「有効」: 鎮痛薬を併用することによって手術が可能であった
- 「無効」: 各薬剤による遮断の効果が認められず、全身麻酔に切り替えた
安全性
副作用等
本試験において、ポプスカイン0.25%注群で安全性評価対象症例31例中1例2件、0.25%ブピバカイン塩酸塩群で安全性評価対象症例30例中5例5件の副作用が認められた。副作用はポプスカイン0.25%注群で頭痛1例(3.2%)及び悪心1例(3.2%)、0.25%ブピバカイン塩酸塩群で嘔吐2例(6.7%)、血圧低下2例(6.7%)及び感覚鈍麻1例(3.3%)であった。両群とも高度な副作用*、重篤な副作用、投与中止に至った有害事象および死亡した症例は認められなかった。
処置を必要とし、治療継続が不可能なもの
|
ポプスカイン0.25%注群(n=31) |
0.25%ブピバカイン塩酸塩群(n=30) |
| 副作用発現例数 |
1 (3.2%) |
5 (16.7%) |
| 副作用発現件数 |
2 |
5 |
| 神経系障害 |
頭痛 |
1 (3.2%) |
- |
| 感覚鈍麻 |
- |
1 (3.3%) |
| 消化器系 |
悪心 |
1 (3.2%) |
- |
| 嘔吐 |
- |
2 (6.7%) |
| 臨床検査 |
血圧低下 |
- |
2 (6.7%) |
数値:例数.():発現率
- 承認効能・効果
ポプスカイン0.25%注 : 術後鎮痛、伝達麻酔(バッグ250mg/100mLを除く)
ポプスカイン0.5%注 : 伝達麻酔
ポプスカイン0.75%注 : 硬膜外麻酔
国内第Ⅲ相一般臨床試験(伝達麻酔:腕神経叢ブロック)
〔ポプスカイン0.5%注における非盲検非対照試験〕9),10)
- 9)丸石製薬株式会社 社内資料 : 第Ⅲ相一般臨床試験(伝達麻酔(腕神経叢ブロック))(MR8A2-14)(承認時評価資料)
- 10)髙崎 眞弓他 : 麻酔と蘇生 2011;47(sup):109-18. [利益相反 : 丸石製薬株式会社の依頼によるMR8A2の第Ⅲ相臨床試験]
試験概要
- 目的
-
伝達麻酔(腋窩部腕神経叢ブロック)により上肢手術を受ける患者を対象に、ポプスカイン0.5%注の有効性及び安全性について検討した。
- 対象
-
伝達麻酔(腋窩部腕神経叢ブロック)により上肢(肘関節と手関節の中間部より遠位)の手術を受ける患者 : 24例
〔24例全例がFAS及び安全性解析対象であり、有効性解析対象であった。〕
- 投与薬剤・投与量
-
ポプスカイン0.5%注 30mL(150mg)
- 投与方法
-
超音波プローブを腋窩部高位で上腕の長軸と垂直に当て、正中、尺骨、橈骨及び筋皮神経の同定を行った。プローブの外側縁中央から、神経ブロック針をプローブの長軸方向と平行に刺入し、針先を各神経にできるだけ接近させた。薬剤の注入は、上記4神経に対して行うこととし、投与量は正中神経、尺骨神経及び橈骨神経は各8mL、筋皮神経は6mLとした。その際、薬剤がそれぞれ対象となる神経周囲を取り囲むように、ブロック針を動かしながら2~3mLずつ分割注入した。
- 評価項目
-
- 解析計画
-
主要評価項目は、記述統計量及び95%信頼区間を算出した。副次評価項目1)、 2)は記述統計量を算出、 3)は「有効」以上の割合を算出した。
有効性
[主要評価項目]知覚神経遮断における痛覚消失効果の平均作用持続時間:FAS
知覚神経遮断における痛覚消失効果の平均作用持続時間(平均値±標準偏差)*は、9.09±2.91時間であり、95%信頼区間は7.86~10.31時間であった。
橈骨、正中、尺骨、筋皮、内側前腕皮及び内側上腕皮の6つの各神経支配領域での作用持続時間の平均値を示す。
[副次評価項目]知覚神経遮断における痛覚消失効果(各神経支配領域での作用発現時間、作用持続時間):FAS
橈骨、正中、尺骨、筋皮、内側前腕皮及び内側上腕皮の6つの各神経支配領域の中で最も多く手術が施行された部位の正中神経領域における痛覚消失効果の作用発現時間(平均値±標準偏差)は、27.6±30.6分であった。観察期間中に痛覚消失効果の作用発現が確認された症例について、内側上腕皮神経では24例中14例(58.3%)であった。
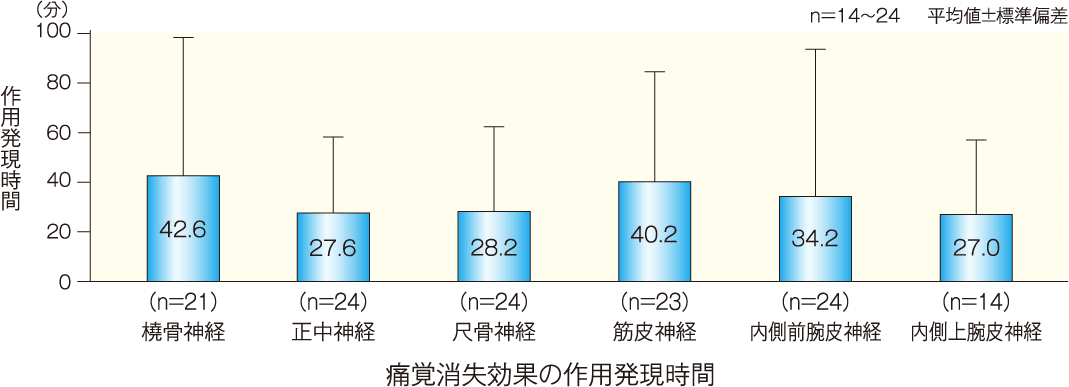
痛覚消失効果の作用持続時間(平均値±標準偏差)は、正中神経領域において10.75±1.59時間であった。内側上腕皮神経では、3.51±4.65時間であった。
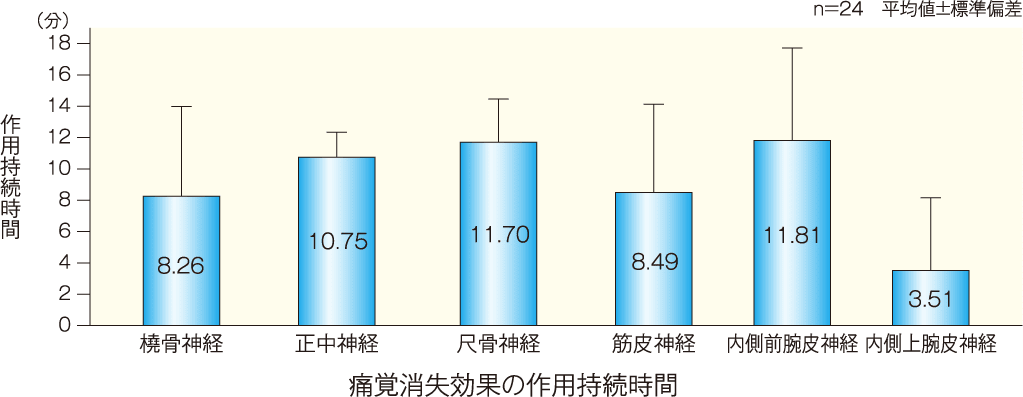
評価方法 : 橈骨神経、正中神経、尺骨神経、筋皮神経、内側前腕皮神経及び内側上腕皮神経支配領域における知覚神経遮断効果をpin-prick法にて以下に示す4段階で評価した。測定時期は、投与前及び投与後10, 20, 30, 40, 60分、2, 3, 4,5, 6, 7, 8, 9, 10, 11, 12, 24時間(判定基準の「1. 効果なし」に戻るまで2時間ごとに確認)。なお、痛覚消失とは「3. 痛覚消失」あるいは「4. 感覚消失」である状態を示すものである。
〔知覚神経遮断効果判定基準(pin-prick法)〕
1. 効果なし : 各薬剤投与前と変化なし、 2. 痛覚鈍麻 : 痛みを感じるが投与前ほどではない、 3. 痛覚消失(analgesia) : 触覚はあるが痛みは感じない、 4. 感覚消失(anesthesia) : 触覚も痛みも感じない
[副次評価項目]運動神経遮断効果(部分、完全)(各神経支配領域での作用発現時間、作用持続時間):FAS
橈骨神経、正中神経、尺骨神経及び筋皮神経支配領域のうち、正中神経領域における運動神経遮断効果の作用発現時間(平均値±標準偏差)は、部分遮断が19.8±22.8分、完全遮断が64.2±59.4分であった。
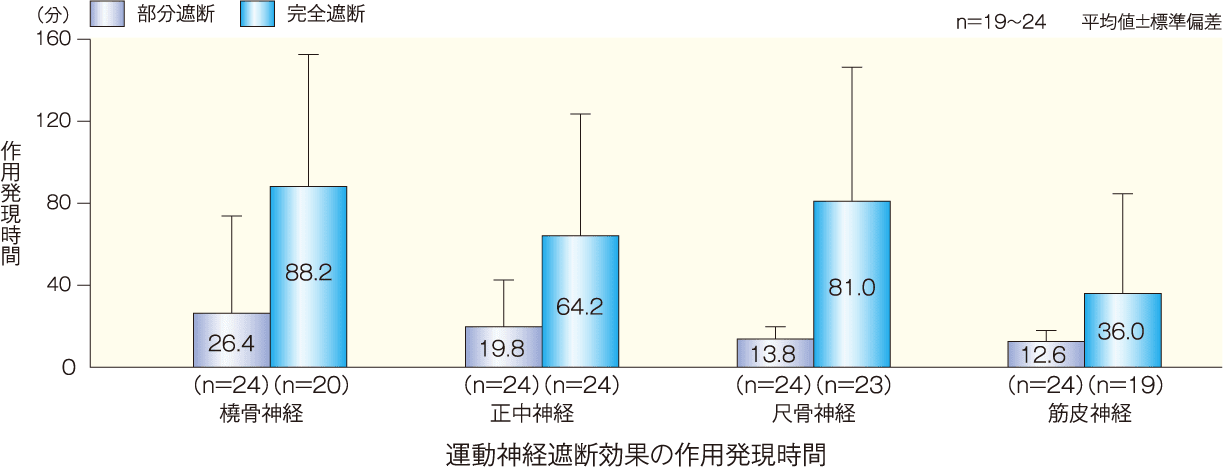
正中神経領域における運動神経遮断効果の作用持続時間(平均値±標準偏差)は、部分遮断が11.67±2.84時間、完全遮断が9.31±2.46時間であった。
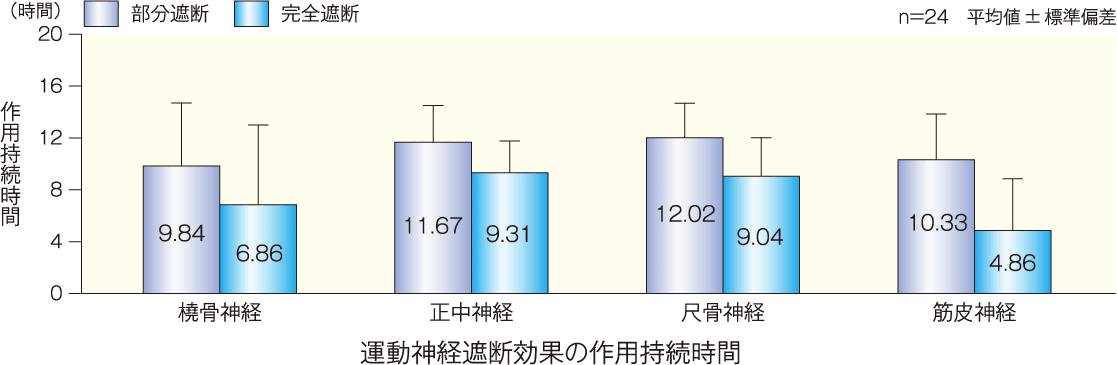
評価方法 : 橈骨神経、正中神経、尺骨神経及び筋皮神経支配領域における運動能をそれぞれ以下に示す基準により3段階で評価した。測定時期は、投与前及び投与後10,20,30,40,60分、2,3,4,5,6,7,8,9,10,11,12,24時間(判定基準の「1.運動神経遮断なし」に戻るまで2時間ごとに確認)。
〔運動神経遮断効果判定基準〕
- ①橈骨神経(手関節を背屈させる能力)
-
1. 運動神経遮断なし : 通常の力で手関節の背屈ができる、 2. 部分運動神経遮断あり : 手関節の背屈はできるが、筋力が低下している、 3. 完全運動神経遮断あり : 手関節の背屈ができない
- ②正中神経(母指と示指によって丸を作る能力)
-
1. 運動神経遮断なし : 通常の力で丸を作ることができる、 2. 部分運動神経遮断あり : 丸を作ることはできるが、筋力が低下している、 3. 完全運動神経遮断あり : 丸を作ることができない
- ③尺骨神経(指を揃えて手刀を作った状態から小指を外転させる能力)
-
1. 運動神経遮断なし : 通常の力で小指を外転させることができる、 2. 部分運動神経遮断あり : 小指を外転させることはできるが、筋力が低下している、 3. 完全運動神経遮断あり : 小指を外転させることができない
- ④筋皮神経(肘関節を屈曲させる能力)
-
1. 運動神経遮断なし: 普通に肘の屈曲ができる、 2. 部分運動神経遮断あり: 肘の屈曲はできるが、筋力が低下している、 3. 完全運動神経遮断あり : 肘の屈曲ができない
[副次評価項目]手術施行に対する評価(「有効」以上の割合):FAS
手術施行に対する評価について、「有効」以上の割合は91.7%(24例中22例)であった。
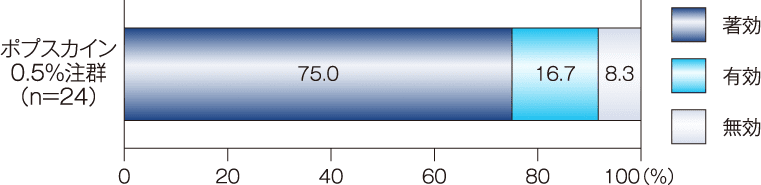
手術施行に対する評価基準
- 「著効」:本剤のみの投与により手術が可能であった
- 「有効」:鎮痛薬を併用することによって手術が可能であった
- 「無効」:各薬剤による遮断の効果が認められず、全身麻酔に切り替えた
安全性
副作用等
本試験において、安全性評価対象症例24例中2例3件の副作用が認められた。副作用は、悪心1例(4.2%)、血圧低下1例(4.2%)及び酸素飽和度低下1例(4.2%)で、高度な副作用*、重篤な副作用、投与中止に至った有害事象および死亡した症例は認められなかった。
処置を必要とし、治療継続が不可能なもの
|
ポプスカイン0.5%注群 (n=24) |
| 副作用発現例数 |
2 (8.3%) |
| 副作用発現件数 |
3 |
| 消化器系 |
悪心 |
1 (4.2%) |
| 臨床検査 |
血圧低下 |
1 (4.2%) |
| 酸素飽和度低下 |
1 (4.2%) |
数値:例数.():発現率
- 承認効能・効果
ポプスカイン0.25%注 : 術後鎮痛、伝達麻酔(バッグ250mg/100mLを除く)
ポプスカイン0.5%注 : 伝達麻酔
ポプスカイン0.75%注 : 硬膜外麻酔
国内第Ⅲ相一般臨床試験(伝達麻酔:指神経ブロック)
〔ポプスカイン0.25%注における非盲検非対照試験〕11),12)
- 11)丸石製薬株式会社 社内資料 : 第Ⅲ相一般臨床試験(伝達麻酔(指神経ブロック))(MR8A2-15)(承認時評価資料)
- 12)髙崎 眞弓他 : 麻酔と蘇生 2011;47(sup):119-27. [利益相反 : 丸石製薬株式会社の依頼によるMR8A2の第Ⅲ相臨床試験]
試験概要
- 目的
-
伝達麻酔(指神経ブロック)により指部の手術を受ける患者を対象に、ポプスカイン0.25%注の有効性及び安全性について検討した。
- 対象
-
伝達麻酔(指神経ブロック)により指部の手術(対象疾患 : 手指の骨折、脱臼、脱臼骨折、指先部損傷、腱損傷、骨腫瘍及び軟部腫瘍)を受ける患者 : 9例 〔9例全例がFAS及び安全性解析対象であり、有効性解析対象例数であった。〕
- 投与薬剤・投与量
-
ポプスカイン0.25%注 4mL(10mg)
- 投与方法
-
体位は仰臥位とした。刺入部の皮膚を消毒し、基節骨基部の背側から24Gブロック針を刺入した。麻酔したい指の橈側の背側皮下に薬剤を1mL注入して背側枝をブロックした。次いでブロック針をそのまま掌側へ進め、皮膚を貫通しないように注意しながら掌側皮下に薬剤を1mL注入して掌側枝をブロックした。次に尺側に対しても同様の麻酔を行い、合計で4mLを投与した。
- 評価項目
-
- 解析計画
-
主要評価項目は、記述統計量の算出及び95%信頼区間を算出した。副次評価項目1)は記述統計量の算出、 2)は「有効」の割合を算出した。
有効性
[主要評価項目]知覚神経遮断における痛覚消失効果の平均作用持続時間:FAS
知覚神経遮断における痛覚消失効果の平均作用持続時間(平均値±標準偏差)は、9.46±1.98時間であり、95%信頼区間は7.94~10.99時間であった。
[副次評価項目]知覚神経遮断における痛覚消失効果(作用発現時間):FAS
知覚神経遮断における痛覚消失効果の作用発現時間(平均値±標準偏差)は、12.0±7.8分であった。
評価方法 : 薬剤を投与した指の指先部における知覚神経遮断効果をpin-prick法にて以下に示す4段階で評価した。測定時期は、投与前及び投与後5,10,20,30分、1,2時間、以後、麻酔効果が消失(判定基準の「1. 効果なし」に戻ること)するまで1時間ごと。なお、痛覚消失とは「3. 痛覚消失」あるいは「4. 感覚消失」である状態を示すものである。
〔知覚神経遮断効果判定基準(pin-prick法)〕
1. 効果なし : 薬剤投与前と変化なし、 2. 痛覚鈍麻 : 痛みを感じるが投与前ほどではない、 3. 痛覚消失(analgesia) : 触覚はあるが痛みは感じない、 4. 感覚消失(anesthesia) : 触覚も痛みも感じない
[副次評価項目]手術施行に対する評価(「有効」の割合):FAS
手術施行に対する評価について、「有効」の割合は、77.8%(9例中7例)であった。
手術施行に対する評価基準
- 「有効」 : 本剤のみの投与により手術が可能であった
- 「無効」 : 薬剤による遮断の効果が認められず、全身麻酔に切り替えた
安全性
副作用等
本試験において、安全性評価対象症例9例中副作用は認められなかった。
- 承認効能・効果
ポプスカイン0.25%注 : 術後鎮痛、伝達麻酔(バッグ250mg/100mLを除く)
ポプスカイン0.5%注 : 伝達麻酔
ポプスカイン0.75%注 : 硬膜外麻酔
国内第Ⅲ相一般臨床試験(伝達麻酔:下肢末梢神経ブロック)
〔ポプスカイン0.25%注における非盲検非対照試験〕13),14)
- 13)丸石製薬株式会社 社内資料 : 第Ⅲ相一般臨床試験(伝達麻酔(下肢末梢神経ブロック))(MR8A2-16)(承認時評価資料)
- 14)髙崎 眞弓他 : 麻酔と蘇生 2011;47(sup):129-39. [利益相反 : 丸石製薬株式会社の依頼によるMR8A2の第Ⅲ相臨床試験]
試験概要
- 目的
-
伝達麻酔(下肢末梢神経ブロック)と全身麻酔の併用により下肢手術を受ける患者を対象に、ポプスカイン0.25%注の有効性及び安全性について検討した。
- 対象
-
伝達麻酔(下肢末梢神経ブロック)と全身麻酔の併用による下肢手術(人工膝関節置換術、膝前十字靭帯再建術、半月板手術(切除術、縫合術)、骨内異物除去術、関節形成術、膝関節滑膜切除術、観血的骨接合術)を受ける患者 : 20例
〔20例全例がFAS及び安全性解析対象であり、有効性解析対象であった。〕
- 投与薬剤・投与量
-
ポプスカイン0.25%注 1神経ブロック当たり40mL(100mg)を上限とし、総量60mL(150mg)を上限とした投与
- 投与方法
-
下肢末梢神経ブロック(大腿神経ブロック、大腰筋筋溝ブロック、坐骨神経ブロック)を単一にて実施、もしくは複数のブロックの併用にて実施した。各々の神経ブロックを実施する際には超音波プローブにて目的とする神経を描出し、必要に応じてメピバカイン塩酸塩で穿刺部位の浸潤麻酔を行ったのち、神経ブロック針を刺入し、ブロック針の先端を目的とする神経にできるだけ接近させ、薬剤を投与した。その際、薬剤が神経周囲を取り囲むように、ブロック針を動かし、吸引試験を行いながら3~5mLずつ分割注入した。坐骨神経ブロックについては臀下部アプローチ、前方アプローチ、膝窩アプローチの3種のアプローチ部位があるため、いずれかのアプローチ方法を選択し、薬剤を投与した。
|
大腿神経 総量ブロック |
坐骨神経ブロック |
総量 |
| 全体 |
臀下部アプローチ |
膝窩アプローチ |
| 症例数 |
20 |
20 |
10 |
10 |
20 |
| 投与容量(mL) |
27.5±3.8 |
28.1±3.6 |
30.0±0.0 |
26.2±4.4 |
55.6±6.4 |
| 投与量(mg) |
68.8±9.5 |
70.3±9.1 |
75.0±0.0 |
65.5±11.1 |
139.0±16.1 |
平均値±標準偏差、坐骨神経ブロックの前方アプローチは該当症例なし
- 評価項目
-
- 解析計画
-
主要評価項目及び副次評価項目1)は測定値ごとに、副次評価項目2)は神経支配領域ごとに症例の割合を算出した。副次評価項目3)は、集計し、記述統計量も算出した。
評価方法 : 腰部神経叢領域(大腿神経、伏在神経、外側大腿皮神経)及び坐骨神経領域(総腓骨神経、脛骨神経)の各神経支配領域における知覚神経遮断効果をpin-prick法にて以下に示す4段階で評価した(全身麻酔中はその限りではなかった)。
測定時期は、投与前及び投与後10,20,30,40分、覚醒確認時、投与後3,4,6,8,10,24時間(効果が消失していない場合は判定基準の「1. 効果なし」に戻るまで2時間ごとに確認)。なお、覚醒確認時の測定時点が投与後3,4,6,8,10時間の規定の測定時期の±15分以内である場合は、覚醒確認時の観察を省略できることとした。なお、痛覚消失とは「3. 痛覚消失」あるいは「4. 感覚消失」である状態を示すものである。
〔知覚神経遮断効果判定基準〕
1. 効果なし : 薬剤投与前と変化なし、 2. 痛覚鈍麻 : 痛みを感じるが投与前ほどではない、 3. 痛覚消失(analgesia) : 触覚はあるが痛みは感じない、 4. 感覚消失(anesthesia) : 触覚も痛みも感じない
〔知覚神経遮断効果の評価を行う神経支配領域(神経ブロック別)〕
大腿神経ブロック : 大腿神経 ・ 伏在神経、坐骨神経ブロック : 総腓骨神経 ・ 脛骨神経
本試験において施行された下肢末梢神経ブロックは、20例全ての症例で大腿神経ブロックと坐骨神経ブロックの併用であり、評価すべき神経支配領域は大腿神経、伏在神経、総腓骨神経及び脛骨神経の4つの神経支配領域であった。(大腰筋筋溝ブロックは施行されなかった。)
有効性
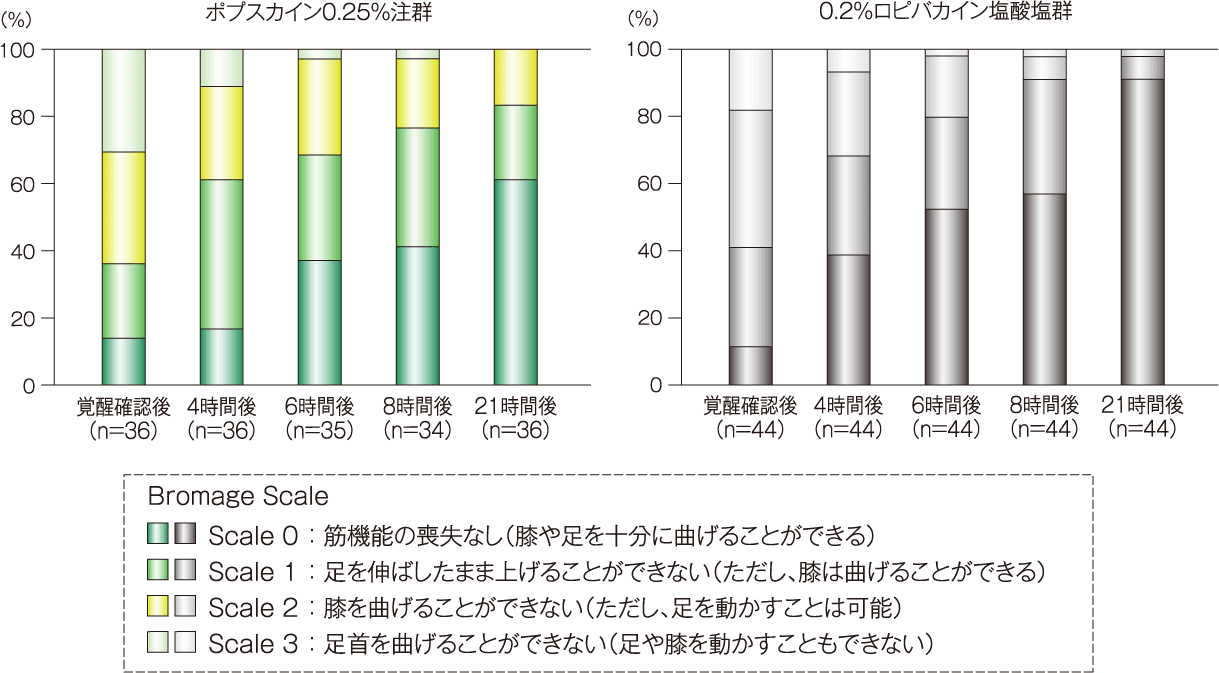
[主要評価項目]評価すべきすべての神経支配領域で痛覚消失効果が認められた症例の割合(投与後3,4,6,8,10時間、覚醒確認時):FAS
施行された下肢末梢神経ブロックに関して評価すべきすべての神経支配領域(大腿神経、伏在神経、総腓骨神経及び脛骨神経)において痛覚消失効果が認められた症例の割合*は、薬剤投与後3時間で92.9%、4時間で89.5%、6時間で80.0%、8時間で75.0%、10時間で75.0%であった。
また、手術時間(平均値±標準偏差)は1.6±0.6時間であり、全身麻酔からの覚醒確認時には、95.0%の症例で痛覚消失効果を示した。
該当する時点のデータが得られなかった症例を除く
[副次評価項目]評価すべきすべての神経支配領域で痛覚消失効果が認められた症例の割合(投与後10,20,30,40分、24時間、覚醒確認後2,4,6,8時間):FAS
施行された下肢末梢神経ブロックに関して評価すべきすべての神経支配領域(大腿神経、伏在神経、総腓骨神経及び脛骨神経)において痛覚消失効果が認められた症例の割合*は、薬剤投与後40分で85.0%に達し、投与後24時間には5.0%となった。また、覚醒確認時から起算した場合の痛覚消失効果が認められた症例の割合は、覚醒確認後2時間で90.0%、4時間で80.0%、6時間で75.0%、8時間で64.3%であった。
該当する時点のデータが得られなかった症例を除く
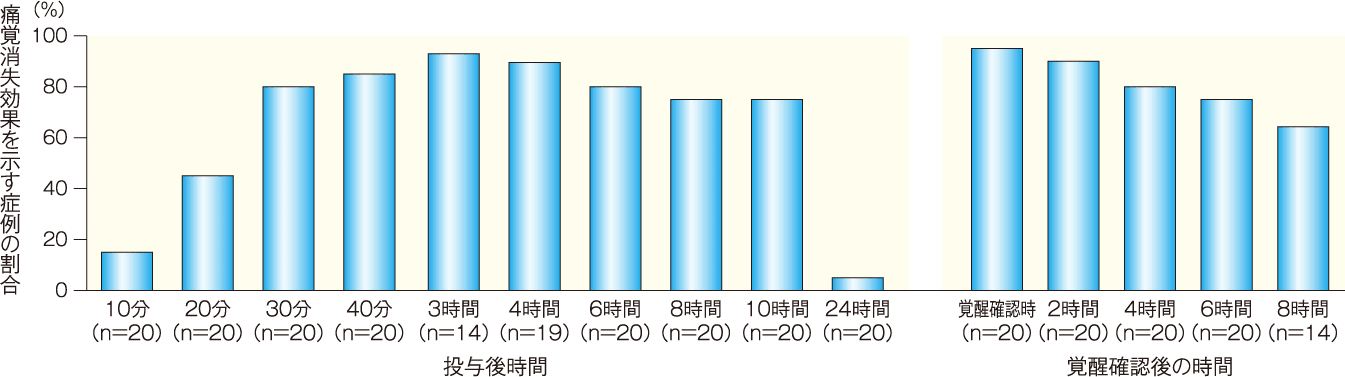
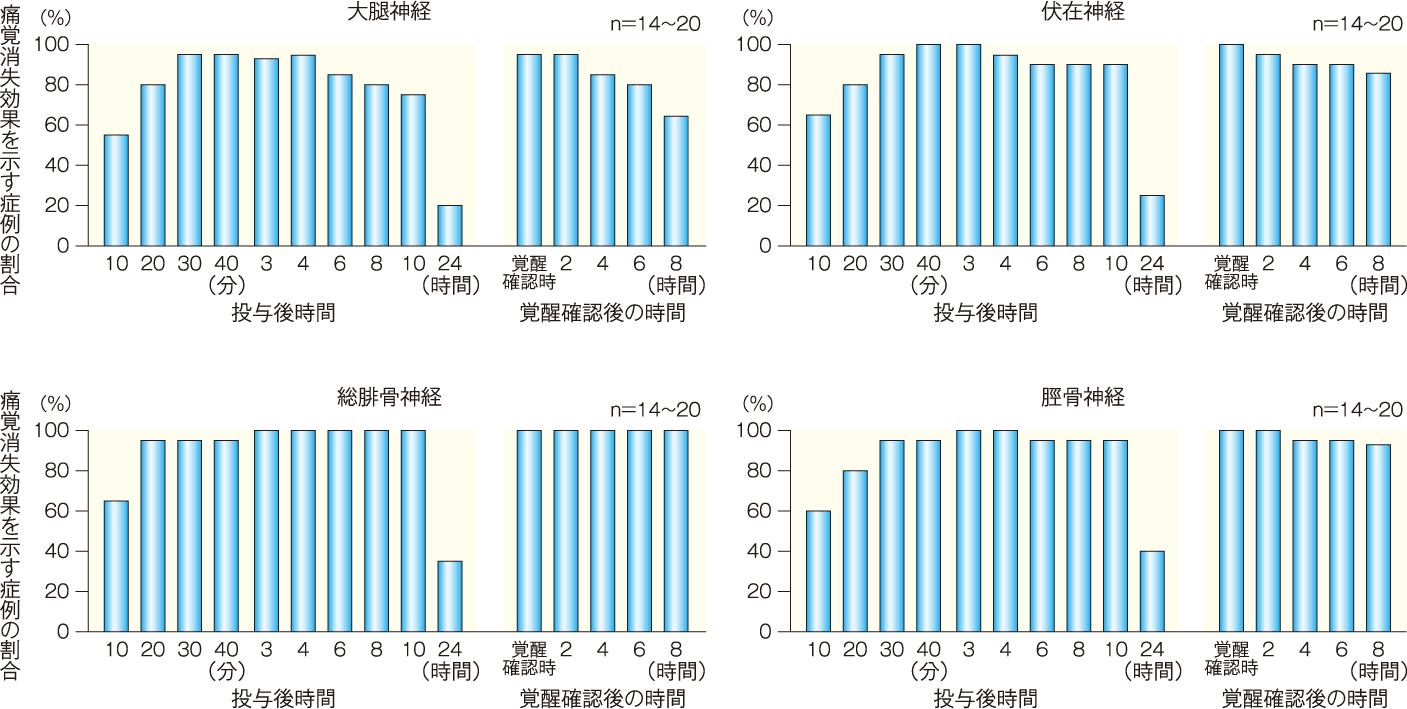
[副次評価項目]各神経支配領域における痛覚消失効果を示す症例の割合(投与後10,20,30,40分、3,4,6,8,10,24時間、覚醒確認時、覚醒確認後2,4,6,8時間):FAS
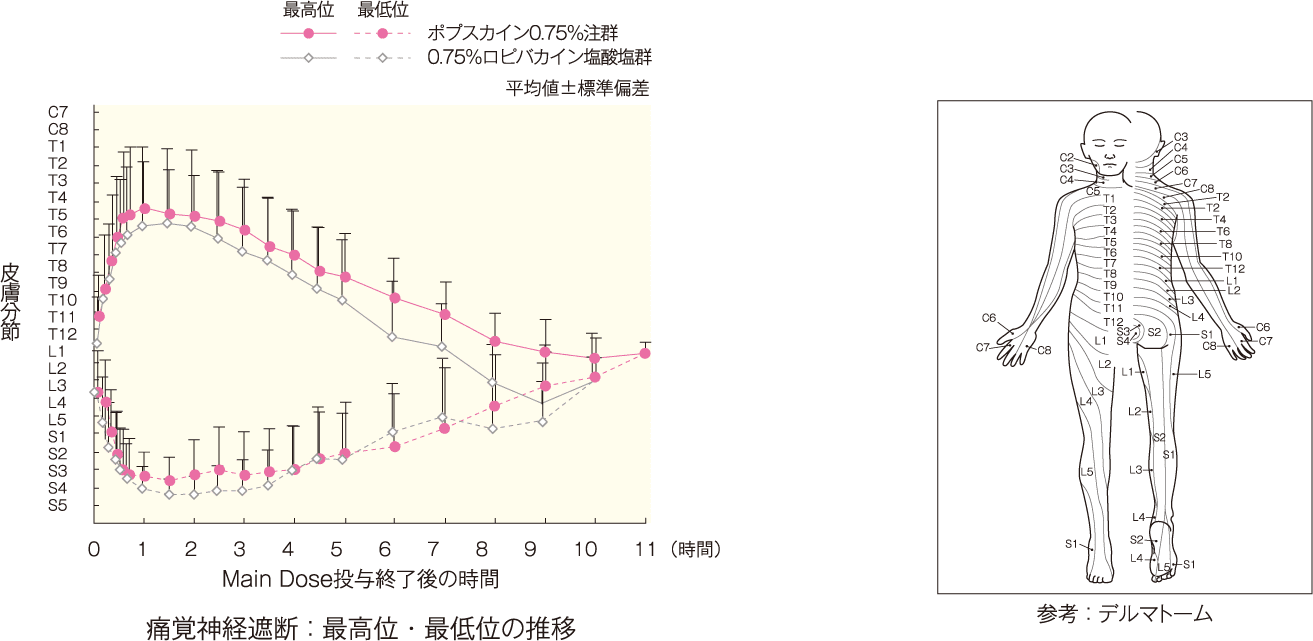
大腿神経、伏在神経、総腓骨神経及び脛骨神経の各神経支配領域における痛覚消失効果を示す症例の割合*は、すべての神経支配領域において、薬剤投与後40分で95%以上を示した。伏在神経では投与後3時間まで、総腓骨神経及び脛骨神経では投与後10時間まで95%以上を示した。
また、覚醒確認後の測定時期においては、大腿神経及び伏在神経では覚醒確認時から覚醒確認後2時間まで、総腓骨神経では覚醒確認時から覚醒確認後8時間まで、脛骨神経では覚醒確認時から覚醒確認後6時間まで95%以上を示した。
該当する時点のデータが得られなかった症例を除く
[副次評価項目]評価すべきすべての神経支配領域及び各神経支配領域における痛覚消失効果の発現時期・消失時期:FAS
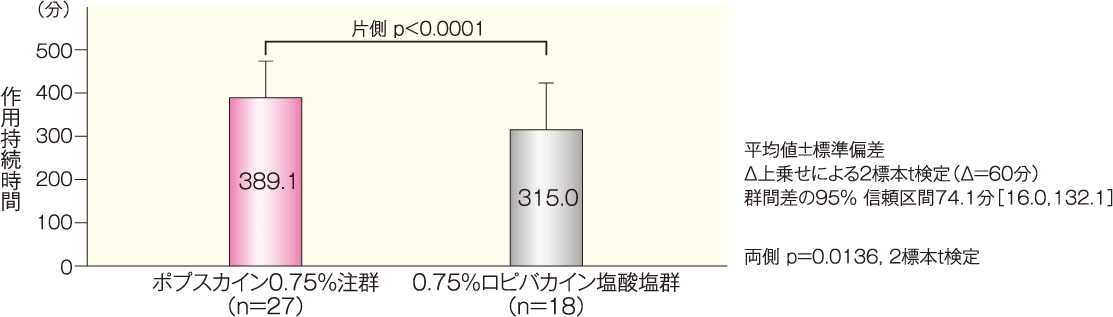
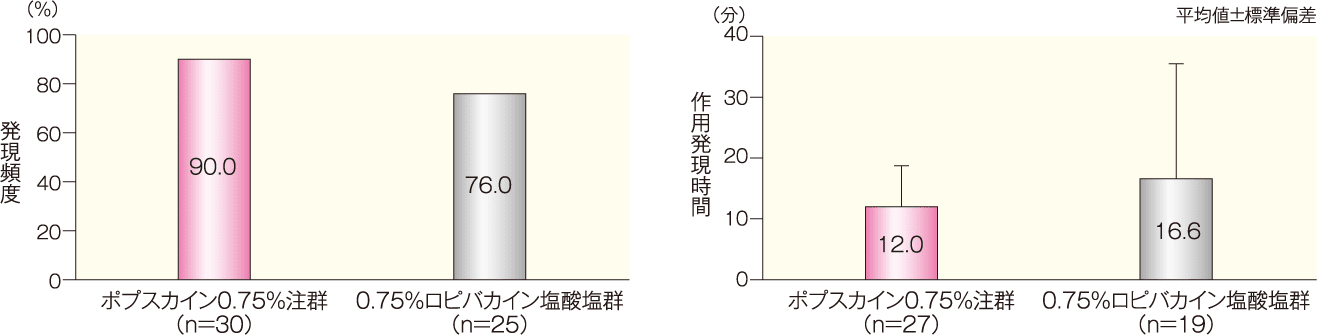
施行された下肢末梢神経ブロックに関して評価すべきすべての神経支配領域(大腿神経、伏在神経、総腓骨神経及び脛骨神経)において、痛覚消失効果の発現時期(すべての神経支配領域で痛覚消失効果が認められた時点)(平均値±標準偏差)は40.2±49.8分、消失時期(4つの神経支配領域のうち一つでも痛覚消失効果が認められなくなった時点)(平均値±標準偏差)は9.63±4.66時間であった。
大腿神経、伏在神経、総腓骨神経及び脛骨神経の各神経支配領域において、痛覚消失効果の発現時期は15.6分から23.4分であり、消失時期は13.16時間から16.60時間であった。
|
発現時期 |
消失時期 |
| n |
平均値±標準偏差 |
n |
平均値±標準偏差 |
| 評価すべきすべての神経支配領域 |
19* |
40.2±49.8分 |
19* |
9.63±4.66時間 |
| 大腿神経 |
19** |
15.6±7.8分 |
19** |
13.16±7.93時間 |
| 伏在神経 |
20 |
16.2±9.6分 |
20 |
13.35±7.83時間 |
| 総腓骨神経 |
20 |
21.6±37.8分 |
20 |
16.30±8.95時間 |
| 脛骨神経 |
20 |
23.4±37.8分 |
20 |
16.60±9.27時間 |
* : 評価すべきすべての神経支配領域のうち一つでも痛覚消失効果が認められなかった症例を除く
** : 痛覚消失効果が認められなかった症例を除く
安全性
副作用等
本試験において、安全性評価対象症例20例中3例3件の副作用が認められた。副作用は、嘔吐2例(10.0%)及び悪心1例(5.0%)で、高度な副作用*、重篤な副作用、投与中止に至った有害事象および死亡した症例は認められなかった。
処置を必要とし、治療継続が不可能なもの
|
ポプスカイン0.25%注群 (n=20) |
| 副作用発現例数 |
3 (15.0%) |
| 副作用発現件数 |
3 |
| 消化器系 |
悪心 |
1 (5.0%) |
| 嘔吐 |
2 (10.0%) |
数値:例数.():発現率
- 承認効能・効果
ポプスカイン0.25%注 : 術後鎮痛、伝達麻酔(バッグ250mg/100mLを除く)
ポプスカイン0.5%注 : 伝達麻酔
ポプスカイン0.75%注 : 硬膜外麻酔




















 」を記載しています。
」を記載しています。