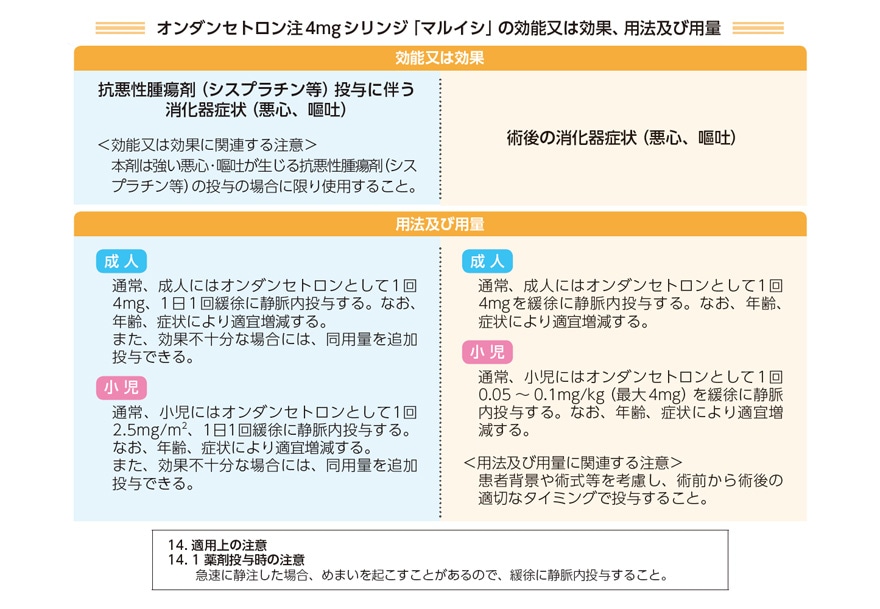
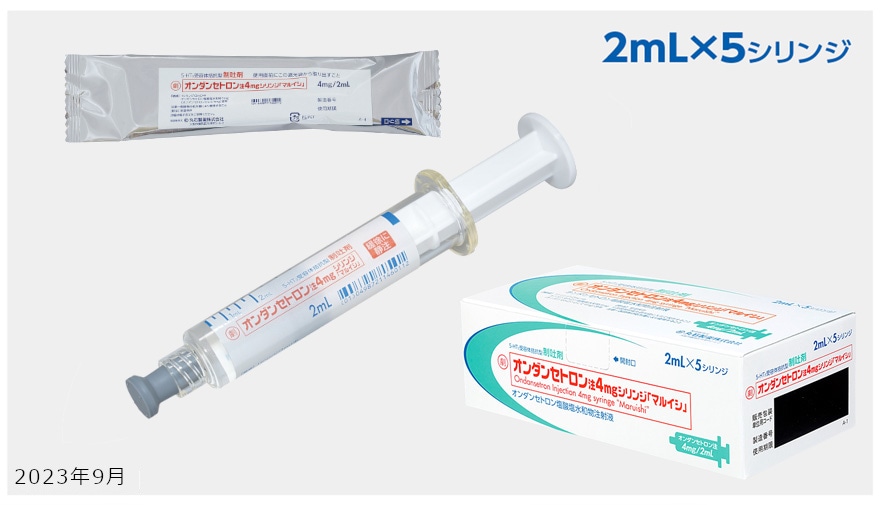
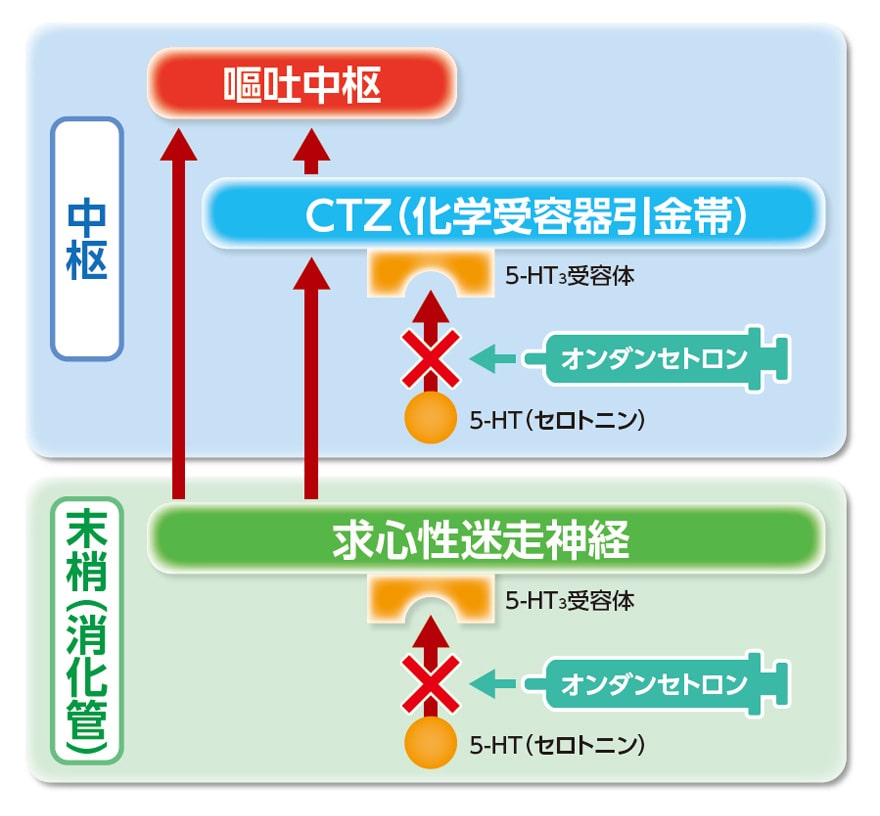
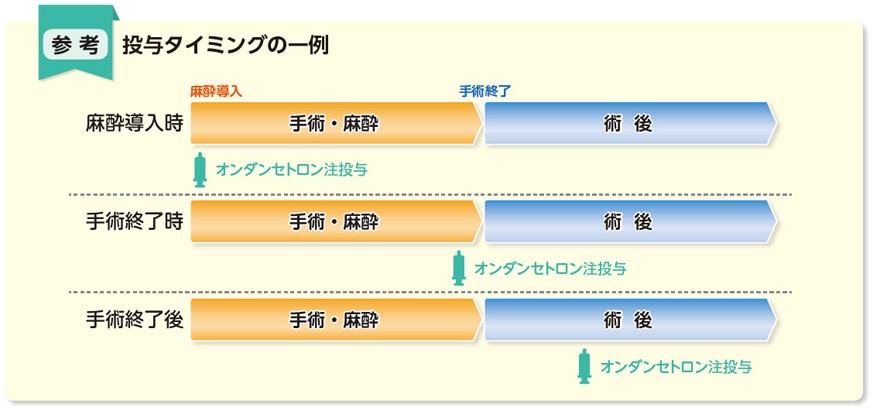
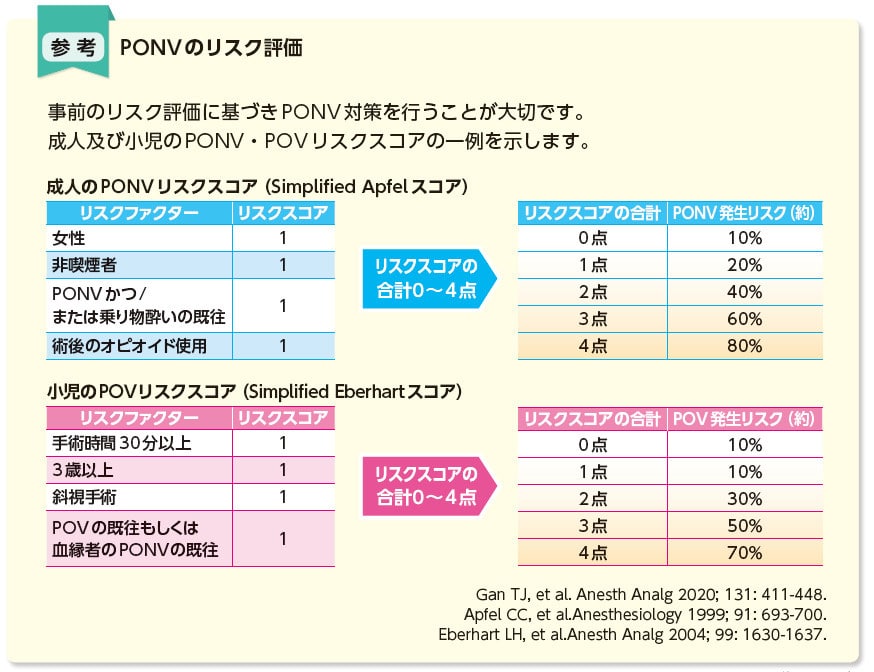
2022年2月25日にオンダンセトロン注4mgシリンジ「マルイシ」に適応が追加されました。ここでは適応追加された「術後の消化器症状(悪心、嘔吐)」の内容を中心にオンダンセトロン注4mgシリンジ「マルイシ」をご紹介いたします。
医療関係者の皆さまへ
このウェブサイトは、日本国内の医療関係者(医師、薬剤師、看護師など)を対象に、
医療用医薬品などを適正にご使用いただくための情報を提供しています。
一般の方および日本国外の医療関係者に対する情報提供を目的としたものではありませんのでご了承ください。
医療関係者でない方はこちらからコーポレートサイトをご覧ください。