1. 警告
呼吸及び循環動態の連続的な観察ができる設備を有し、緊急時に十分な措置が可能な施設において、本剤の薬理作用を正しく理解し、小児の麻酔前投薬での鎮静における患者管理に熟練した医師のもとで使用すること。呼吸抑制及び呼吸停止を引き起こすことがあり、速やかな処置が行われないために死亡又は低酸素脳症に至った症例が報告されている。[8.1、8.2、9.1.1、9.1.2、11.1.1 参照]
2. 禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 急性閉塞隅角緑内障の患者[抗コリン作用により眼圧が上昇し、症状を悪化させることがある。]
2.3 重症筋無力症のある患者[重症筋無力症の症状を悪化させるおそれがある。]
2.4 HIVプロテアーゼ阻害剤(リトナビルを含有する薬剤、ホスアンプレナビル、ダルナビルを含有する薬剤)、 コビシスタットを含有する薬剤、ニルマトレルビル・リトナビル及びロナファルニブを投与中の患者[10.1 参照]
2.5 ショックの患者、昏睡の患者、バイタルサインの抑制がみられる急性アルコール中毒の患者[呼吸抑制や血圧低下等の症状を悪化させるおそれがある。]
本剤の有効成分であるミダゾラムは、イミダゾベンゾジアゼピン誘導体であり、γ-アミノ酪酸(GABA)受容体のベンゾジアゼピン結合部位に結合し、間接的にGABAの作用を増強することにより催眠、鎮静、抗不安作用を示すと考えられています。ミダゾラムは、1982年にスイスで注射剤として最初に承認されて以来、米国、英国をはじめ世界各国で使用されています。本邦ではミダゾラム注射液(ドルミカム®注射液10mg)が催眠鎮静剤注1として、ミダゾラム静注液及びミダゾラム口腔用液が抗けいれん剤注2として承認を取得しており、現在臨床使用されています。
手術や麻酔は患者にとって大きなストレスであり、特に小児患者においては、保護者との分離不安により啼泣、興奮を引き起こし麻酔導入及び気管挿管が困難になるだけではなく、分泌物による気道閉鎖、嘔吐による誤嚥及び不整脈等を引き起こすことがあります。このため、小児患者の不安軽減及び麻酔導入を円滑に施行する目的で使用される麻酔前投薬は、非常に重要です。また、麻酔前投薬においては効果発現が速やかで持続時間の短い鎮静薬が適しており、小児患者においては投与時に侵襲を伴う投与経路ではなく経口投与可能な薬剤が求められています。
ミダゾラムは経口投与した場合も作用発現が速く、消失半減期も短いため1-2) 、麻酔前投薬の薬剤として海外(米国、英国など)ではミダゾラム経口液剤が麻酔前投薬として承認されています。本邦においてはミダゾラム注射剤が麻酔前投薬として承認されていますが、その投与経路は侵襲を伴う筋肉内投与のみの承認であり注1 、経口投与可能な製剤は承認されていない注2ことから、本邦の医療現場では注射剤をシロップ剤に院内で製剤化して用いている状況がありました。
このような状況を踏まえ、日本小児麻酔学会より麻酔前投薬を効能又は効果としたミダゾラムシロップ剤の開発要望が厚生労働省へ提出され、2018年7月4日に開催された「医療上の必要性の高い未承認薬・適応外薬検討会議」にて医療上の必要性が高いと評価されました。丸石製薬株式会社(以下、当社)は2019年4月1日付でアステラス製薬株式会社より、「ドルミカム®注射液10mg」の製造販売承認を承継したことから、当社はミダゾラムシロップ剤開発の医療上の意義に鑑み、製剤開発を行い、2021年8月に厚生労働省より開発要請を受けたことから、本剤の小児に対する「麻酔前投薬」の適応の取得を目的とした開発に着手しました。
今般、国内第Ⅱ/Ⅲ相臨床試験(MR19A13A-2試験)において小児患者における麻酔前投薬として本剤の有効性及び安全性が検討されたことから、2024年12月25日付で特定用途医薬品注3の指定を受け、2025年3月6日に製造販売承認申請を行い、2025年9月19日に小児に対する「麻酔前投薬」を効能又は効果として製造販売承認を取得しました。
| 注1) | 催眠鎮静剤: | ミダゾラム注射液(ドルミカム®注射液10mg) |
| 効能又は効果: | 「麻酔前投薬」、「全身麻酔の導入及び維持」、「集中治療における人工呼吸中の鎮静」、「歯科・口腔外科領域における手術及び処置時の鎮静」 | |
| 注2) | 抗けいれん剤: | ミダゾラム静注液及びミダゾラム口腔用液 |
| 効能又は効果: | 「てんかん重積状態」 | |
| 注3) | 特定用途医薬品: | 小児に対する用法又は用量が設定されていないなど、医療上のニーズが著しく充足されていない医薬品の研究開発の促進に寄与すること目的に創設された制度で、医療上特にその必要性が高いことなど、指定の条件に合致することを薬事審議会の意見を聴いて厚生労働大臣が指定する。指定された医薬品はPMDA相談や審査などで優先した取扱いを受けることができる。 |
1)Coté CJ,et al.Anesth Analg 2002:94(1):37-43[DMC2020009]
2)M D Reed,et al.J Clin Pharmacol;2001;41(12):1359-1369[DMC2010687]
| 4. | 効能又は効果 麻酔前投薬 |
| 5. | 効能又は効果に関連する注意 生後6ヵ月未満の小児における有効性及び安全性は確立していない。 |
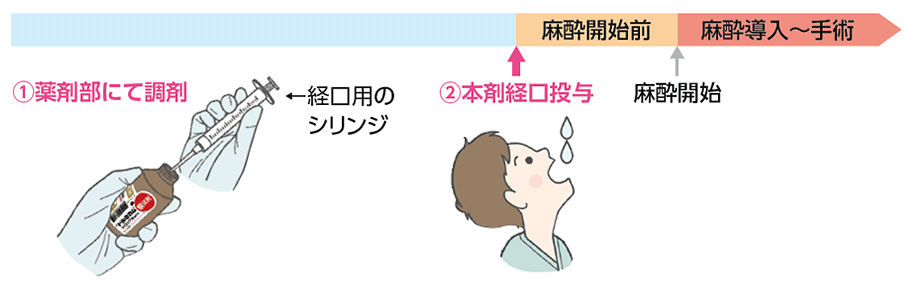
| 6. | 用法及び用量 通常、小児にはミダゾラムとして1回0.25〜1.0mg/kg(最大用量20mg))を麻酔開始前に経口投与する。 |
| 7. | 用法及び用量に関連する注意(抜粋) |
| 7.3 | ミダゾラムに対する反応は個人差があり、患者の年齢、感受性、全身状態及び併用薬等を考慮して、過度の鎮静を避けるべく投与量を決定すること。特に、衰弱患者、心不全患者、肝機能障害患者及び麻酔薬、鎮痛薬(麻薬性及び非麻薬性鎮痛薬)、局所麻酔薬、中枢神経系抑制薬等を併用する場合は、投与量を減じること。作用が強くあらわれやすい。[9.1.3-9.1.5、9.3、10.2、16.6.1、16.6.3参照] |
| 9. | 特定の背景を有する患者に関する注意(抜粋) |
| 9.7 | 小児等 |
| 9.7.1 | 生後6ヵ月未満の小児を対象とした臨床試験は実施していない。 |
| 9.7.2 | 小児等において、激越、不随意運動(強直性/間代性痙攣、筋振戦を含む)、運動亢進、敵意、激しい怒り、攻撃性、発作性興奮、暴行などの逆説反応が起こりやすいとの報告がある。 |
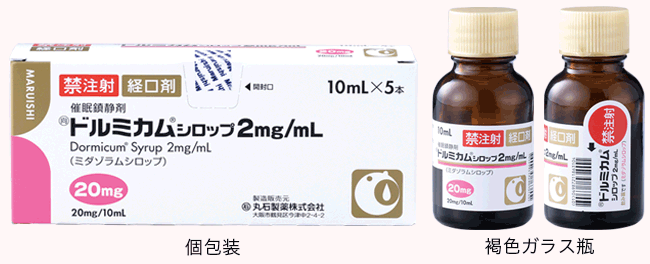
| 販売名 | ドルミカム®シロップ 2mg/mL |
| 有効成分 | 1mL中 ミダゾラム 2mg |
| 添加剤 | D-ソルビトール液、濃グリセリン、リン酸二水素ナトリウム水和物、安息香酸ナトリウム、エデト酸ナトリウム水和物、スクラロース、ph調節剤、香料 |
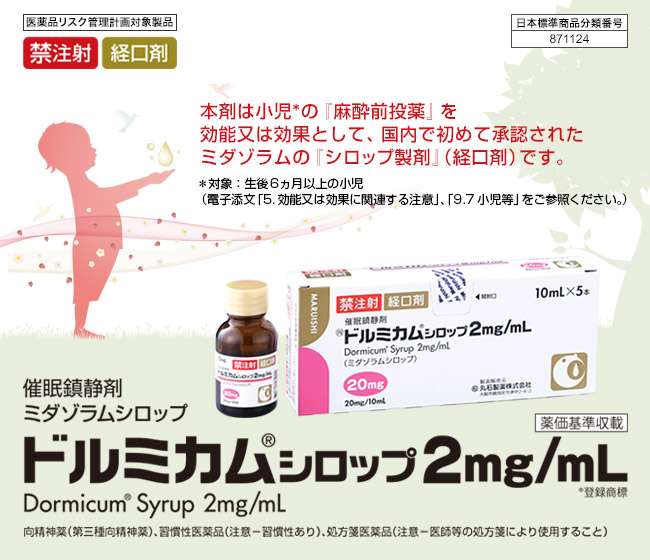
| 性状・ 包装 |
無色澄明のシロップ剤で、ストロベリー様のにおいがある。10mL×5本[褐色ガラス瓶]


|
呼吸及び循環動態の連続的な観察ができる設備を有し、緊急時に十分な措置が可能な施設において、本剤の薬理作用を正しく理解し、小児の麻酔前投薬での鎮静における患者管理に熟練した医師のもとで使用すること。呼吸抑制及び呼吸停止を引き起こすことがあり、速やかな処置が行われないために死亡又は低酸素脳症に至った症例が報告されている。
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
急性閉塞隅角緑内障の患者
重症筋無力症のある患者
HIVプロテアーゼ阻害剤(リトナビルを含有する薬剤、ホスアンプレナビル、ダルナビルを含有する薬剤)、コビシスタットを含有する薬剤、ニルマトレルビル・リトナビル及びロナファルニブを投与中の患者
ショックの患者、昏睡の患者、バイタルサインの抑制がみられる急性アルコール中毒の患者
本剤投与において必要な施設体制
呼吸及び循環動態の連続的な観察ができる設備を有する
緊急時に十分な措置が可能な施設
準備が必要な医療機器(年齢や体格に応じたもの)、薬剤
パルスオキシメータ
血圧計
酸素吸入器
吸引器具
挿管器具等の人工呼吸のできる器具
昇圧剤等の救急蘇生剤
フルマゼニル(ベンゾジアゼピン受容体拮抗剤)
本剤投与において必要な人員配置・管理体制
本剤の薬理作用を正しく理解し、小児の麻酔前投薬での鎮静における患者管理に熟練した医師のもとで使用すること
小児の基本的蘇生措置に精通した医師の監視下で、患者が完全に回復するまで患者の呼吸及び循環動態を継続的に観察すること
術後は全身状態に注意し、基本的運動・平衡機能の回復等に基づき帰宅可能と判断できるまで患者を管理下に置くこと
過量投与により、過鎮静、傾眠、錯乱、昏睡等が起こる可能性がある
本剤の過量投与が明白又は疑われた場合には、必要に応じてフルマゼニル(ベンゾジアゼピン受容体拮抗剤)の投与を考慮すること
フルマゼニルの作用持続時間は本剤よりも短く、鎮静等の本剤の作用が再度あらわれるおそれがある
開栓後は汚染防止のため、使用の都度必ず密栓し室温で保存すること
本剤は経口投与のみに使用し、注射しないこと
| 効能又は効果 | 麻酔前投薬 | ||||||||
| 効能又は効果に 関連する注意 |
生後6ヵ月未満の小児における有効性及び安全性は確立していない。 | ||||||||
| 用法及び用量 | 通常、小児にはミダゾラムとして1回0.25〜1.0mg/kg(最大用量20mg)を麻酔開始前に経口投与する。 | ||||||||
| 用法及び用量に 関連する注意 |
|
| 用量 | 患者の体重(8〜50kg) | |||||
| 8kg | 10kg | 20kg | 30kg | 40kg | 50kg | |
| 0.25mg/kg | 1.0mL (2.0mg) |
1.25mL (2.5mg) |
2.5mL (5.0mg) |
3.75mL (7.5mg) |
5.0mL (10.0mg) |
6.25mL (12.5mg) |
| 0.5mg/kg | 2.0mL (4.0mg) |
2.55mL (5.0mg) |
5.0mL (10.0mg) |
7.5mL (15.5mg) |
10.0mL (20.0mg) |
10.0mL (20.0mg) |
| 1.0mg/kg | 4.0mL (8.0mg) |
5.0mL (10.0mg) |
10.0mL (20.0mg) |
10.0mL (20.0mg) |
10.0mL (20.0mg) |
10.0mL (20.0mg) |
※ 経口投与量(上段の数値は本剤の投与量、下段の(括弧内)の数値はミダゾラムとしての量)
小児患者を対象としたドルミカム®シロップ2mg/mL(以下、本剤)の有効性及び安全性を検討する第Ⅱ/Ⅲ相臨床試験 3)
3)社内資料(承認時評価資料):国内第Ⅱ/Ⅲ相臨床試験(MR19A13A-2試験)(2025年9月19日承認、CTD2.7.6.3)
| 主目的 | 小児患者を対象として、本剤0.25mg/kg、0.5mg/kg 又は1.0mg/kg(最大用量20mg)を単回経口投与したときの鎮静効果を評価した。 |
| 副次目的 | 小児患者を対象として、本剤0.25mg/kg、0.5mg/kg 又は1.0mg/kg(最大用量20mg)を単回経口投与したときの以下の有効性及び安全性を評価した。 ・抗不安作用 ・マスク導入に対する協力度 |
| 探索的目的 | 小児患者における本剤の味の受容性を評価した。 |
多施設共同、無作為化、単回投与、非盲検
マスク導入による全身麻酔施行下での予定手術患者 72例
| 解析対象集団 | |||
| 年齢区分 | 0.25mg/kg群 | 0.5mg/kg群 | 1.0mg/kg群 |
| 生後6ヵ月以上~2歳未満 | 5例 | 6例 | 7例 |
| 2歳以上~6歳未満 | 11例 | 12例 | 13例 |
| 6歳以上~16歳未満 | 6例 | 6例 | 6例 |
| 計 | 22例 | 24例 | 26例 |
| 1) | 同意取得時の年齢が生後6ヵ月以上16歳未満の日本人患者(二親等以内の親族がすべて日本人、性別不問) |
| 2) | 本治験の参加に先立ち、十分な説明の後、法的保護者の文書による同意が得られた患者。なお、7歳以上の患者の場合、可能な限り患者本人よりアセントも取得することが望ましい。 |
| 3) | 米国麻酔学会(ASA)分類Ⅰ~Ⅲの患者 |
| 4) | 妊娠可能な女性の場合、妊娠中又は妊娠している可能性がなく、授乳中でないこと |
本剤0.25mg/kg、0.5mg/kg 又は1.0mg/kg(最大用量20mg)を麻酔前投薬として術前(マスク導入30分以上前)に単回経口投与したときの鎮静効果、有効性及び安全性、味の受容性を評価した。
すべての選択基準を満たし、除外基準に抵触しない症例に対して、年齢区分(生後6ヵ月以上2歳未満、2歳以上6歳未満、6歳以上16歳未満)を層別因子とした動的割付法を用いて、3投与群(0.25mg/kg群、0.5mg/kg群又は1.0mg/kg群)の比率が1:1:1 になるように無作為に割り付けた。本剤投与終了前後の規定時点における鎮静度スコア及び不安度スコア、並びにマスク導入時の協力度スコアの評価により、有効性の評価を行った。
安全性の評価としては、本剤投与開始後から最終観察時点までに発現した有害事象の収集、本剤投与前後での臨床検査、バイタルサイン、SpO2及び呼吸数の測定及び心電図の記録を実施した。また、本剤投与終了直後に本剤の味の受容性の評価を行った。
[主要有効性評価項目]
本剤投与終了後30分以内に鎮静度スコアが3以上に達した被験者の割合
[副次有効性評価項目]
| 1) | 本剤投与終了後30分以内に不安度スコアが3以上に達した被験者の割合 |
| 2) | 保護者との分離時における不安度スコアが3以上であった被験者の割合 |
| 3) | マスク導入時における協力度スコアが3以上であった被験者の割合 |
| 4) | 鎮静度スコアが3以上に到達するまでの時間 |
| 5) | 不安度スコアが3以上に到達するまでの時間 |
味の受容性評価が2以上であった被験者の割合
| 1) | 有害事象及び副作用 |
| 2) | 臨床検査 |
| 3) | バイタルサイン(収縮期血圧、拡張期血圧、脈拍数) |
| 4) | SpO2、呼吸数 |
| 5) | 心電図 |
解析対象集団は最大の解析対象集団(FAS)とした。補足的解析として治験実施計画書適合集団(PPS)を対象とした解析を行い、結果の頑健性を検討した。
[主要有効性評価項目]
3投与群を併合した全被験者における、「本剤投与終了後30分以内に鎮静度スコアが3以上に達した被験者」の割合及び割合の両側95%信頼区間(CI)を算出した。このとき、両側95%CIの下限値と有効割合の閾値として設定した65%を比較し、95%CIの下限値が有効割合閾値(65%)を上回ることにより有効と判定した。
また、投与群ごとの「本剤投与終了後30分以内に鎮静度スコアが3以上に達した被験者」の割合及び割合の両側95%CI を算出した。投与群及び年齢群ごとについても集計した(サブグループ解析)。
[副次有効性評価項目]
各評価項目については3投与群を併合した全被験者の割合及び割合の両側95%CIを算出した。また投与群及び年齢群ごとについても集計した(サブグループ解析)。
解析対象集団はFASとした。3投与群を併合した全被験者における、「味の受容性評価が2以上であった被験者」の割合及び割合の両側95%CIを算出した。また、投与群ごとについても集計した(サブグループ解析)。
解析対象集団は安全性解析対象集団(SS)とした。有害事象は試験治療下における有害事象(TEAE)とし、医薬品規制調和国際会議(ICH)国際医薬用語集(MedDRA)にてコーディングした。
有害事象名は器官別大分類(SOC)及び基本語(PT)ごとに分類し、投与群ごとに発現頻度を集計した。副作用についても同様に行った。重篤な有害事象は詳細を記述するとした。臨床検査の各時点の検査値は、連続変数については記述統計量を用いて投与群ごとに要約した。また、投与前後値のシフトテーブルを投与群ごとに作成した。
バイタルサインは、測定値及び投与前からの変化量について、投与群ごとに記述統計量を用いて要約した。SpO2及び呼吸数は、測定値及び投与前からの変化量について、投与群ごとに記述統計量を用いて要約した。心電図の異常の有無について、投与群ごとに該当例数及びその割合を算出した。
| 鎮静度スコア | |||
| 基準 | 説明 | スコア | |
| 警戒している/活動的な | 興奮/激越、動いている、身体又は口頭で不安/心配を訴える(大声又は高音で泣く) | 1 | |
| 動揺している/用心深い | 泣いている、親や保護者から離れない | 2 | |
| 落ち着いた | 穏やかな、ボーっとした、指示や穏やかな刺激に容易に反応する | 3 | |
| うとうとした | 容易に覚醒する、軽い揺さぶりや刺激に反応する | 4 | |
| 眠っている | 覚醒しない、揺さぶりや刺激に反応しない | 5 | |
| 不安度スコア | |||
| 基準 | 説明 | スコア | |
| 不十分 | 怖がっている、闘争的な、泣き叫んでいる、拘束されている | 1 | |
| 普通 | 心配そうな、中等度の不安 | 2 | |
| よい | 少し心配そうな、見知らぬ人でも簡単に落ち着く、闘争的ではない | 3 | |
| 非常によい | 恐怖心や不安な様子を示さない | 4 | |
| 該当なし | 患者は寝ている | - | |
| 協力度スコア | |||
| 基準 | 説明 | スコア | |
| 不十分 | 介入を強く拒否する | 1 | |
| 普通 | 介入するためにかなりの努力が必要 | 2 | |
| よい | 嫌々介入を受け入れる | 3 | |
| 非常によい | 容易に介入を受け入れる | 4 | |
| 該当なし | 患者は寝ている | - | |
| 説明 | スコア |
| 完全に拒否する、吐き出す | 1 |
| 不満を言うが服用する | 2 |
| 顔をしかめて服用する | 3 |
| 容易に/ためらうことなく服用する | 4 |
本剤投与終了後30分以内に鎮静度スコアが3以上に達した被験者の割合
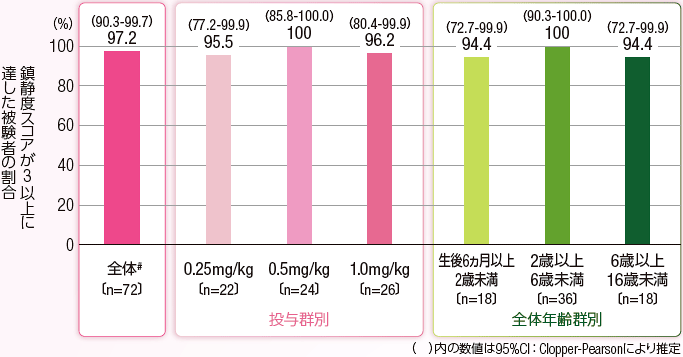
鎮静度スコアが3以上に達した被験者の割合及び割合の両側95%CIは、3投与群を併合した全被験者で97.2%(70/72例)(95%CI:90.3-99.7)であり、両側95%CIの下限値(90.3%)は治験実施計画書において有効割合の閾値として設定した65%を上回った(Clopper-Pearsonにより推定)。
投与群ごとでは、0.25mg/kg群、0.5mg/kg群、1.0mg/kg群でそれぞれ95.5%(21/22例)、100%(24/24例)、96.2%(25/26例)であった。
1)本剤投与終了後30分以内に不安度スコアが3以上に達した被験者の割合
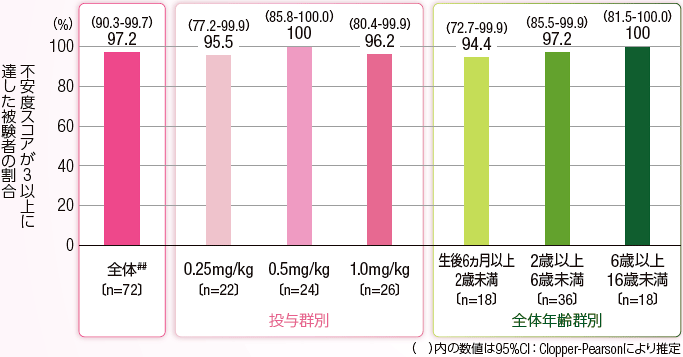
不安度スコアが3以上に達した被験者の割合は上に記した図の通りであり、3投与群を併合した全被験者で97.2%(70/72例)であった。
2)保護者との分離時における不安度スコアが3以上であった被験者の割合
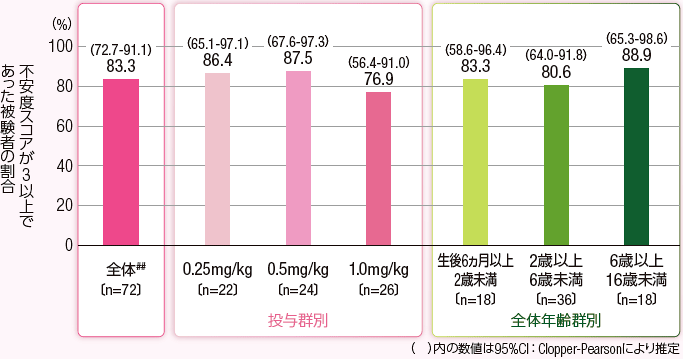
保護者との分離時における不安度スコアが3以上であった被験者の割合は上に記した図の通りであり、3投与群を併合した全被験者で83.3%(60/72例)であった。
3)マスク導入時における協力度スコアが3以上であった被験者の割合
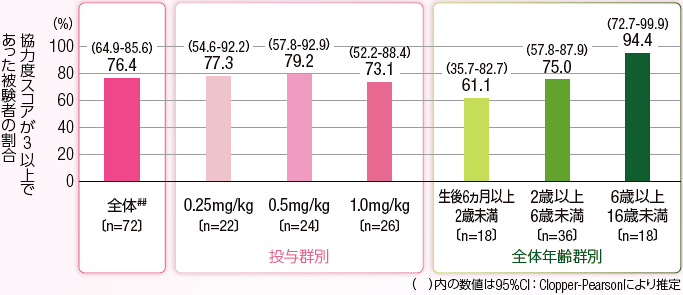
マスク導入時における協力度スコアが3以上であった被験者の割合は上に記した図の通りであり、3投与群を併合した全被験者で76.4%(55/72例)であった。
4)鎮静度スコアが3以上に到達するまでの時間・5)不安度スコアが3以上に到達するまでの時間
本剤投与前の鎮静度又は不安度の各スコアが2以下であった被験者が初めてスコア3以上に到達した時間は、3投与群を併合した全被験者で、本剤投与終了後10分であった被験者が最も多かった(鎮静度:50.0%(13/26例)、不安度:38.2%(13/34例))。また、本剤投与終了後30分までに鎮静度は92.3%(24/26例)、不安度は94.1%(32/34例)の被験者でスコアが初めて3以上に到達した。
味の受容性評価が2以上であった被験者の割合
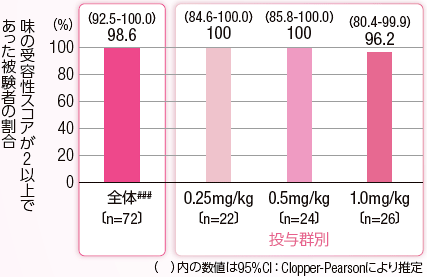
味の受容性評価スコアが2以上であった被験者の割合は3投与群を併合した全被験者で98.6%(71/72例)、投与群ごとでは、0.25mg/kg群、0.5mg/kg群、1.0mg/kg群でそれぞれ100%(22/22例)、100%(24/24例)、96.2%(25/26例)であり、いずれの投与群でも味の受容性は良好であった。
有害事象及び副作用
| 投与群 | 0.25mg/kg群 (n=22) |
0.5mg/kg群 (n=24) |
1.0mg/kg群 (n=26) |
合計 (n=72) |
|
| 発現例数(発現率) | 0(0) | 5(20.8) | 1(3.8) | 6(8.3) | |
| 代謝および栄養障害 | 0(0) | 2(8.3) | 0(0) | 2(2.8) | |
| ・高カリウム血症 | 0(0) | 1(4.2) | 0(0) | 1(1.4) | |
| 有 | ・低血糖 | 0(0) | 1(4.2) | 0(0) | 1(1.4) |
| 害 | 呼吸器、胸郭および縦隔障害 | 0(0) | 1(4.2) | 0(0) | 1(1.4) |
| 事 | ・咳嗽 | 0(0) | 1(4.2) | 0(0) | 1(1.4) |
| 象 | 臨床検査 | 0(0) | 1(4.2) | 1(3.8) | 2(2.8) |
| ・酸素飽和度低下 | 0(0) | 1(4.2) | 1(3.8) | 2(2.8) | |
| 傷害、中毒および処置合併症 | 0(0) | 1(4.2) | 0(0) | 1(1.4) | |
| ・麻酔からの覚醒遅延 | 0(0) | 1(4.2) | 0(0) | 1(1.4) | |
| 発現例数(発現率) | 0(0) | 2(8.3) | 0(0) | 2(2.8) | |
| 副 | 代謝および栄養障害 | 0(0) | 1(4.2) | 0(0) | 1(1.4) |
| 作 | ・高カリウム血症 | 0(0) | 1(4.2) | 0(0) | 1(1.4) |
| 用 | 傷害、中毒および処置合併症 | 0(0) | 1(4.2) | 0(0) | 1(1.4) |
| ・麻酔からの覚醒遅延 | 0(0) | 1(4.2) | 0(0) | 1(1.4) |
MedDRA Version 26.0
有害事象及び副作用の発現頻度は上に記した表の通りであった。有害事象は、0.5mg/kg群の20.8%(5/24例)及び1.0mg/kg群の3.8%(1/26例)に認められ、そのうち副作用は0.5mg/kg群の8.3%(2/24例)に認められた。
本試験において死亡に至った有害事象、その他重篤な有害事象及び本剤投与の中止に至った有害事象は認められなかった。
4)社内資料(承認時評価資料):国内薬物動態試験(MR19A13A-1試験)(2025年9月19日承認、CTD2.7.6.1)
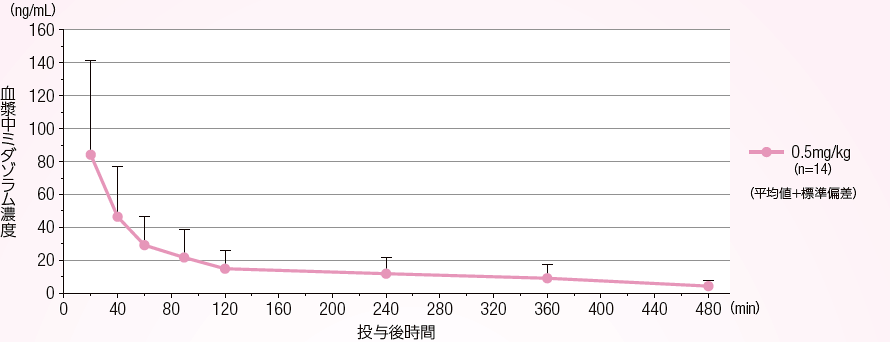
ミダゾラムの血漿中濃度(単回投与)
本剤単回経口投与後のミダゾラムの血漿中薬物濃度推移(平均値+標準偏差)は以下の通りであった。血漿中ミダゾラム濃度のTmax(中央値(最小-最大))は0.33(0.30-1.50)時間であった。また、T1/2(平均値±標準偏差)は2.13±0.84時間であり、速やかに効果が消失することが示唆された。
| Cmax(ng/mL) | Tmax(h) | T1/2(h) | AUC0-inf(ng・h/mL) | CLtot(L/h/kg) |
| 85.44±56.17 (n=14) |
0.33 (0.30-1.50) (n=14) |
2.13±0.84 (n=11) |
150.0±70.5 (n=11) |
4.08±1.88 (n=11) |
(平均値±標準偏差、Tmaxは中央値(最小-最大))
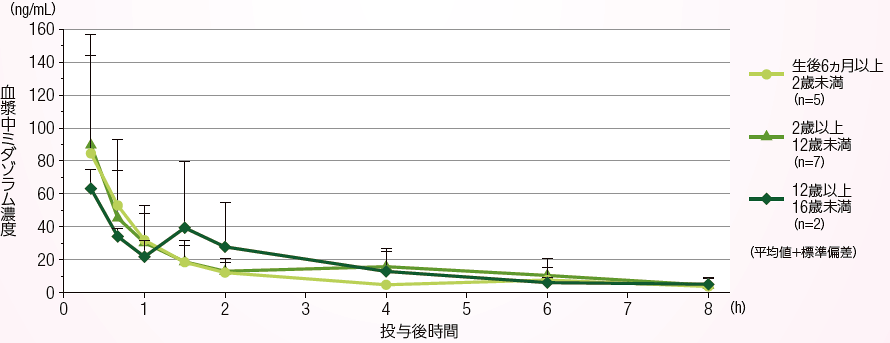
年齢群別でのミダゾラムの血漿中濃度
年齢群別の本剤単回経口投与後のミダゾラムの血漿中薬物濃度の推移(平均値+標準偏差)は以下の通りであった。
| 年齢区分 | Cmax(ng/mL) | Tmax(h) | T1/2(h) | AUC0-inf(ng・h/mL) | CLtot(L/h/kg) |
| 生後6ヵ月以上~2歳未満 | 84.94±59.14 (n=5) |
0.32(0.30-0.37) (n=5) |
2.56±1.14 (n=5) |
122.6±54.4 (n=4) |
4.54±1.42 (n=4) |
| 2歳以上~12歳未満 | 90.27±66.29 (n=7) |
0.32(0.30-0.33) (n=7) |
1.62±0.36 (n=5) |
166.9±79.5 (n=5) |
3.80±2.34 (n=5) |
| 12歳以上~16歳未満 | 69.80±2.40 (n=2) |
0.92(0.33-1.50) (n=2) |
2.57±0.38 (n=2) |
162.5±104.0 (n=2) |
3.87±2.48 (n=2) |
(平均値±標準偏差、Tmaxは中央値(最小-最大))
| 対象 | 生後6ヵ月以上~16歳未満の日本人患者のうち、全身麻酔施行下での手術予定患者14例 |
| 方法 | 本剤0.5mg/kg(最大用量20mg)を麻酔開始前に単回経口投与し、血漿中ミダゾラムの濃度推移及び薬物動態パラメータを評価した。 |
6. 用法及び用量
通常、小児にはミダゾラムとして1回0.25~1.0mg/kg(最大用量20mg)を麻酔開始前に経口投与する。
※ 製品のご使用に際しましては、最新の電子添文をご確認ください。